Đề kiểm tra cuối kì 2 Hóa 8 có đáp án (Mới nhất)
Đề kiểm tra cuối kì 2 Hóa 8 có đáp án (Mới nhất) (Đề 12)
-
733 lượt thi
-
4 câu hỏi
-
0 phút
Danh sách câu hỏi
Câu 1:
Hoàn thành sơ đồ chuyển hoá sau. Cho biết mỗi phản ứng đó thuộc loại phản ứng nào đã học.
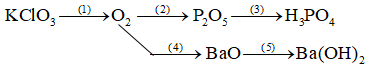
 Xem đáp án
Xem đáp án
(1)
(2)
(3) P2O5 + 3H2O → 2H3PO4
(4)
(5) BaO + H2O → Ba(OH)2
Câu 3:
Cho 2,4 gam kim loại canxi phản ứng với 68,76 gam nước thu được dung dịch Y và khí hiđro. Dẫn toàn bộ lượng khí hiđro trên qua ống sứ đựng sắt(II) oxit dư, đun nóng.
a) Chất tan trong dung dịch Y là gì? Tính nồng độ phần trăm của dung dịch Y
b) Xác định khối lượng kim loại sắt sinh ra trong ống sứ.
 Xem đáp án
Xem đáp án
a)
Phương trình hoá học: Ca + 2H2O → Ca(OH)2 + H2
Chất tan trong dung dịch Y là Ca(OH)2
Theo phương trình hoá học:
→
= 2,4 + 68,76 – 0,12 = 71,04 (g)
Nông độ phần trăm của dung dịch Y là:
b) Phương trình hoá học:
Theo phương trình hoá học:
→ mFe = 0,06.56 = 3,36(g)
Câu 4:
Hòa tan hoàn toàn 11,34 gam nhôm và 4,32 gam magie vào dung dịch axit sunfuric.
a) Tính thể tích khí hiđro (đktc) thu được sau khi phản ứng xảy ra.
b) Xác định nồng độ mol các chất tan có trong dung dịch thu được sau phản ứng. Biết dung dịch này có thể tích là 300 ml.
 Xem đáp án
Xem đáp án
Phương trình hoá học:
2Al + 3H2SO4 → Al2(SO4)3 + 3H2↑ (1)
Mg + H2SO4 → MgSO4 + H2↑ (2)
Theo phương trình hoá học (1):
Theo phương trình hoá học (2):
Tổng số mol khí H2 thoát ra là: 0,63 + 0,18 = 0,81 (mol)
Thể tích khí hiđro (đktc) thu được sau khi phản ứng xảy ra là: 0,81.22,4 = 18,144 (lít)
b) Đổi 300 ml = 0,3 l
Các chất tan có trong dung dịch thu được sau phản ứng là: Al2(SO4)3 và MgSO4
Theo phương trình hoá học (1):
→
Theo phương trình hoá học (2):
→