Methane cháy tỏa nhiệt lớn nên được dùng làm nhiên liệu. Khi trộn methane và oxygen với tỉ lệ thích hợp thì sẽ tạo ra hỗn hợp nổ
175
17/04/2023
Mở đầu trang 88 Hóa học 10: Methane cháy tỏa nhiệt lớn nên được dùng làm nhiên liệu. Khi trộn methane và oxygen với tỉ lệ thích hợp thì sẽ tạo ra hỗn hợp nổ.
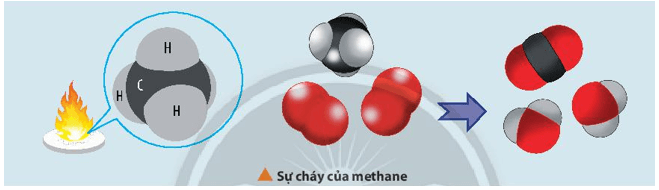
Biến thiên enthalpy của phản ứng trên được tính toán dựa trên các giá trị nào?
Trả lời
CH4(g) + 2O2(g) CO2(g) + 2H2O(l)
Biến thiên enthalpy của phản ứng cháy của methane có thể được tính theo hai cách:
- Cách 1: Dựa vào nhiệt tạo thành chuẩn của các chất.
∆r = ∆f(CO2) + 2.∆f(H2O) – ∆f(CH4) – 2.∆f(O2)
- Cách 2: Dựa vào năng lượng liên kết của các chất.
∆r = Eb(CH4) + 2.Eb(O2) – Eb(CO2) – 2.Eb(H2O)
∆r = 4.Eb(C-H) + 2.Eb(O=O) – 2. Eb(C=O) – 2.2.Eb(O-H)
Xem thêm các bài giải SGK Hoá học lớp 10 Chân trời sáng tạo hay, chi tiết khác:
Bài 12: Phản ứng oxi hóa – khử và ứng dụng trong cuộc sống
Bài 13: Enthalpy tạo thành và biến thiên enthalpy của phản ứng hóa học
Bài 14: Tính biến thiên enthalpy của phản ứng hóa học
Bài 15: Phương trình tốc độ phản ứng và hằng số tốc độ phản ứng
Bài 16: Các yếu tố ảnh hưởng đến tốc độ phản ứng hóa học
Bài 17: Tính chất vật lí và hóa học các đơn chất nhóm VIIA

