Giải Hoá Học 10 Bài 15: Phương trình tốc độ phản ứng và hằng số tốc độ phản ứng
Lời giải:
Để đánh giá mức độ nhanh hay chậm của một phản ứng hóa học ta dùng đại lượng tốc độ phản ứng hóa học.
- Tốc độ phản ứng của phản ứng hóa học là đại lượng đặc trưng cho sự biến thiên nồng độ của một trong các chất phản ứng hoặc sản phẩm trong một đơn vị thời gian.
- Tốc độ phản ứng kí hiệu là v, có đơn vị: (đơn vị nồng độ)/ (đơn vị thời gian).
+ Xét phản ứng đơn giản có dạng: aA + bB → cC + dD
+ Mối quan hệ giữa nồng độ và tốc độ tức thời của phản ứng hóa học được biểu diễn bằng biểu thức:
+ Trong đó:
k là hằng số tốc độ phản ứng;
CA; CB là nồng độ (M) chất A, B tại thời điểm đang xét.
- Tốc độ trung bình của phản ứng là tốc độ được tính trong một khoảng thời gian phản ứng.
(mo-dau-trang-94-hoa-hoc-10-1)
Trong đó:
: tốc độ trung bình của phản ứng
∆C = C2 – C1: sự biến thiên nồng độ
∆t = t2 – t1 : biến thiên thời gian
C1, C2 là nồng độ của một chất tại hai thời điểm tương ứng t1 và t2.
1. Tốc độ phản ứng
Lời giải:
Phản ứng cháy xảy ra nhanh hơn, có phát sáng và tỏa nhiệt mạnh, lá cây nhanh chóng bị chuyển thành tro.
Phản ứng oxi hóa kim loại trong thân tàu trong điều kiện tự nhiên xảy ra chậm hơn, một thời gian mới xuất hiện gỉ kim loại, không phát sáng, không tỏa nhiệt mạnh.
Lời giải:
- Ở cùng điều kiện, nhiều chất khác nhau sẽ biến đổi hóa học nhanh, chậm khác nhau.
Ví dụ: Trong cùng một môi trường nhiệt độ phòng:
+ Quá trình oxi hóa sắt (cửa sắt) tạo gỉ sắt xảy ra chậm (vài tháng hoặc vài năm).
+ Quá trình oxi hóa thức ăn xảy ra nhanh (vài tiếng, 1 ngày hoặc vài ngày).
- Với cùng một chất, trong điều kiện khác nhau cũng biến đổi hóa học nhanh, chậm khác nhau.
Ví dụ: Rau được bảo quản trong tủ lạnh sẽ giữ được lâu hơn rau để bên ngoài.
Lời giải:
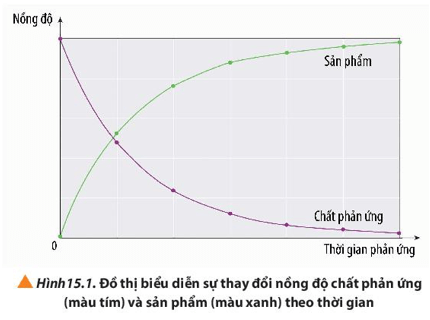
- Nồng độ của chất phản ứng giảm dần theo thời gian.
- Nồng độ của chất sản phẩm tăng dần theo thời gian.
Luyện tập trang 95 Hóa học 10: Xét phản ứng phân hủy N2O5 ở 45oC
Lời giải:
= 1,36.10-3 (M/s)
Vậy tốc độ trung bình của phản ứng theo N2O4 trong 184 giây đầu tiên là 1,36.10-3 (M/s)
2. Biểu thức tốc độ phản ứng
Lời giải:
Theo định luật tác dụng khối lượng tốc độ phản ứng tỉ lệ thuận với nồng độ các chất tham gia phản ứng.
⇒ Tốc độ phản ứng tăng khi tăng nồng độ chất phản ứng. Ngược lại, tốc độ phản ứng giảm khi giảm nồng độ chất phản ứng.
Lời giải:
- Khi ở nơi đông người trong không gian kín, ta cảm thấp khó thở và phải thở nhanh hơn.
Giải thích: Oxygen duy trì sự hô hấp, khi ở nơi đông người trong không gian kín nồng độ oxygen thấp hơn.
⇒ Nồng độ oxygen trong không khí không đủ để cung cấp cho mọi người.
⇒ Ta cảm thấp khó thở và phải thở nhanh hơn.
- Bệnh nhân suy hô hấp cần thở oxygen thay vì không khí (chứa 21% thể tích oxygen).
Giải thích: Bệnh nhân suy hô hấp khó khăn trong việc tự thở, dẫn đến thiếu oxygen cung cấp cho hoạt động của cơ thể. Trong bình khí nén oxygen, nồng độ oxygen cao hơn nồng độ oxygen có trong không khí giúp bệnh nhân thở dễ dàng hơn, cung cấp đủ oxygen cho các tế bào, giúp duy trì sự sống.
Luyện tập trang 96 Hóa học 10: Cho phản ứng đơn giản sau:
a) Viết biểu thức tốc độ tức thời của phản ứng trên
b) Tốc độ phản ứng thay đổi thế nào khi nồng độ H2 giảm 2 lần và giữ nguyên nồng độ Cl2?
Lời giải:
H2(g) + Cl2(g) → 2HCl(g)
a) Biểu thức tốc độ tức thời của phản ứng viết theo định luật là:
b) Nồng độ H2 giảm 2 lần và giữ nguyên nồng độ Cl2
⇒
Vậy tốc độ phản ứng giảm một nửa khi nồng độ H2 giảm 2 lần và giữ nguyên nồng độ Cl2
Lên men sữa chua tạo sữa chua (3)
Lời giải:
Sắp xếp theo thứ tự tốc độ giảm dần: (2) > (1) > (3) > (4)
Bài tập (trang 97)
Bài 1 trang 97 Hóa học 10: Cho phản ứng đơn giản xảy ra trong bình kín: 2NO(g) + O2(g) → 2NO2(g)
a) Viết biểu thức tốc độ tức thời của phản ứng
b) Ở nhiệt độ không đổi, tốc độ phản ứng thay đổi thế nào khi
- nồng độ O2 tăng 3 lần, nồng độ NO không đổi?
- nồng độ NO tăng 3 lần, nồng độ O2 không đổi?
- nồng độ NO và O2 đều tăng 3 lần?
Lời giải:
a) Biểu thức tốc độ tức thời của phản ứng:
b) - nồng độ O2 tăng 3 lần, nồng độ NO không đổi
⇒ Tốc độ phản ứng tăng 3 lần
- nồng độ NO tăng 3 lần, nồng độ O2 không đổi
⇒ Tốc độ phản ứng tăng 9 lần
- nồng độ NO và O2 đều tăng 3 lần
⇒ Tốc độ phản ứng tăng 27 lần.
2CO(g) + 2NO(g) → 2CO2(g) + N2(g)
Lời giải:
Dựa vào tỉ lệ hệ số trong phương trình ta thấy nồng độ tiêu hao của NO nhanh gấp hai lần nồng độ tạo thành của N2.
Bài 3 trang 97 Hóa học 10: Cho phản ứng:
Lời giải:
Tốc độ trung bình của phản ứng là:
Bài 4 trang 97 Hóa học 10: Dữ liệu thí nghiệm của phản ứng:
SO2Cl2(g) → SO2(g) + Cl2(g) được trình bày ở bảng sau
a) Tính tốc độ trung bình của phản ứng theo SO2Cl2 trong thời gian 100 phút.
b) Sau 100 phút, nồng độ của SO2Cl2 còn lại là bao nhiêu?
c) Sau 200 phút, nồng độ của SO2 và Cl2 thu được là bao nhiêu?
Lời giải:
a) Tốc độ trung bình của phản ứng theo SO2Cl2 trong thời gian 100 phút.
(M/phút)
b) Sau 100 phút, nồng độ của SO2Cl2 còn lại là 1,00 – 0,13 = 0,87 M
c) Sau 200 phút, nồng độ của SO2Cl2 còn lại là: 0,78 M
⇒ Nồng độ của SO2Cl2 đã phản ứng là: 1,00 – 0,78 = 0,22 M
⇒ nồng độ của SO2 và Cl2 thu được là 0,22 M
Xem thêm lời giải bài tập SGK Hoá học lớp 10 Chân trời sáng tạo hay, chi tiết khác:
Bài 13: Enthalpy tạo thành và biến thiên enthalpy của phản ứng hóa học
Bài 14: Tính biến thiên enthalpy của phản ứng hóa học
Bài 16: Các yếu tố ảnh hưởng đến tốc độ phản ứng hóa học
Bài 17: Tính chất vật lí và hóa học các đơn chất nhóm VIIA
Bài 18: Hydrogen halide và một số phản ứng của ion halide