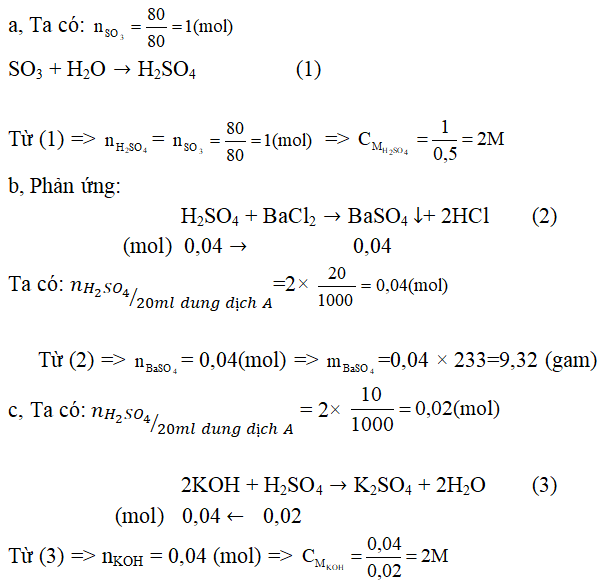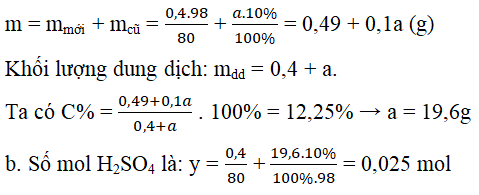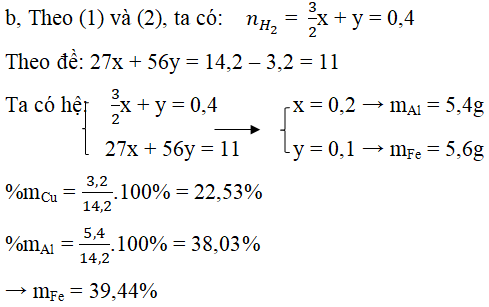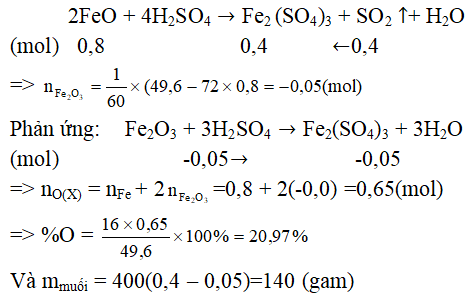Lí thuyết Kim loại tác dụng với axit H2SO4
1. Lí thuyết
1.1 Kim loại tác dụng với axit H2SO4
Tác dụng với kim loại tạo thành muối sunfat và H2
2M + nH2SO4 → M2(SO4)n + nH2 ↑
(M đứng trước H2, n là số oxi hóa thấp nhất của kim loại)
1.2 Kiến thức mở rộng
Ở trạng thái loãng là một axit mạnh, ở trạng thái đặc là một chất ôxihóa mạnh.
- Ở dạng loãng là axít mạnh: làm đỏ quì tím, tác dụng kim loại(trước H2) giải phóng H2, tác dụng bazơ, oxit bazơ và nhiều muối.
H2SO4 làm quỳ tím hóa đỏ
Fe + H2SO4 → FeSO4 + H2
NaOH + H2SO4 → NaHSO4 + H2O
CuO + H2SO4 → CuSO4 + H2O
BaCl2 + H2SO4 → BaSO4 + 2HCl
Na2 CO3 + H2SO4 → Na2SO4 + H2O + CO2
- Ở dạng đặc là một chất ôxi hóa mạnh
Tác dụng với kim loại: oxi hoá hầu hết các kim loại (trừ Au và Pt) tạo muối hoá trị cao và thường giải phóng SO2 (có thể H2 S, S nếu kim loại khử mạnh như Mg ).
2 Fe + 6H2SO4 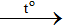
Cu + 2H2SO4 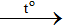
Al, Fe, Cr không tác dụng với H2SO4 đặc nguội, vì kim loại bị thụ động hóa.
- Tác dụng với phi kim ( tác dụng với các phi kim ở dạng rắn, to) tạo hợp chất của phim kim ứng với số oxh cao nhất.
C + 2H2SO4 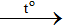
S + 2H2SO4 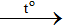
- Tác dụng với một số chất có tính khử
FeO + H2SO4 
HBr + H2SO4 
Hút nước của 1 số chất hữu cơ:
C12H22O11 + H2SO4(đ) → 12C + H2SO4.11H2O
2. Bài tập vận dụng
Câu 1. Trộn 200 ml dung dịch NaOH 1M với 150ml dung dich H2SO4 1M. Hỏi sau khi phản ứng kết thúc khôi lượng muối thu được là bao nhiêu?
Lời giải:
Đáp án:
Ta có: nNaOH = 0,2 × 1 = 0,2(mol); nH2SO4 = 0,15 mol
Phản ứng: NaOH + H2SO4 → NaHSO4 + H2O
(mol) 0,15 ← 0,15 → 0,15
NaOH + NaHSO4 → Na2SO4 + H2O
(mol) 0,05 → 0,05
⇒ nNaHSO4 dư = 0,15 – 0,05 = 0,1 (mol)
⇒ mmuối = mNaHSO4 + mNaSO4 = 120 × 0,1 + 142 × 0,05=19,1(gam)
Câu 2. Cho 80 gam SO3 vào một cốc nước sau đó thêm nước vào đến vạch 0,5 lít thì dừng (gọi là dung dịch A).
a, Tính nồng độ mol/l của dung dịch A.
b, Cho 20 ml dung dịch A vào dung dịch BaCl4 dư. Hãy tính khối lượng kết tủa thu được.
c, Để trung hòa 20ml dung dịch KOH thì cần 10ml dung dịch A. Tính nồng độ mol/l của dung dịch KOH.
Lời giải:
Đáp án:
Câu 3. Hòa tan 0,4 gam SO3 vào a gam dung dịch H2SO4 10% thu được dung dịch H2SO4 12,25%.
a) Tính a
b) Thêm 10 ml dung dịch Ba(OH)2 0,5 M vào dung dịch thu được ở trên lọc kết tủa thêm tiếp 50 ml dung dịch NaOH 0,8 M vào nước lọc rồi cho bay hơi thu được 6,44 gam chất rắn X. Xác định công thức của X.
Lời giải:
Đáp án:
a. Khi hòa tan SO3 vào dung dịch xảy ra phản ứng: SO3 + H2O → H2SO4
Khối lượng của H2SO4:
Số mol Ba(OH)2 là x= 0,01.0,5 = 0,005 mol;
Số mol NaOH là z = 0,05.0,8 = 0,04 mol.
Khi thêm các dung dịch trên ta có phản ứng:
Ba(OH)2 + H2SO4 → BaSO4↓ + 2H2O (1)
2NaOH + H2SO4 → Na2SO4 + 2H2O (2)
Theo phương trình phản ứng (1) và (2) x + z/2 = 0,025 = y
⇒ H2SO4 phản ứng hoàn toàn, lọc bỏ kết tủa BaSO4 thì trong dung dịch chỉ còn Na2SO4 với số mol là: 0,02 mol.
Cho bay hơi dung dịch thu được Na2SO4.nH2O (X).
Vậy MX = 6,44/0,02 = 322g
MX = (2.23 + 96 + 18n) = 322 → n = 10
Vậy X là Na2SO4.10H2O
Câu 4. Cho 14,2 gam hỗn hợp A gồm ba kim loại Al, Fe và M vào dung dịch H2SO4 loãng dư thu được 8,96 lít H2 (54oC; 1,2 atm), dung dịch B và 3,2 gam rắn C. Hòa tan toàn bộ rắn C vào dung dịch H2SO4 đậm đặc nóng thoát ra V lít khí E (có mùi hắc) (đktc).
a) Xác định kim loại M (biết V lít khí E làm mất màu vừa đủ 50ml dung dịch Br2 1M).
b) Tính % khối lượng mỗi kim loại trong hỗn hợp A.
Lời giải:
Đáp án:
a, Vì Al và Fe tác dụng với H2SO4 loãng nên rắn C là kim loại M không phản ứng với H2SO4 loãng.
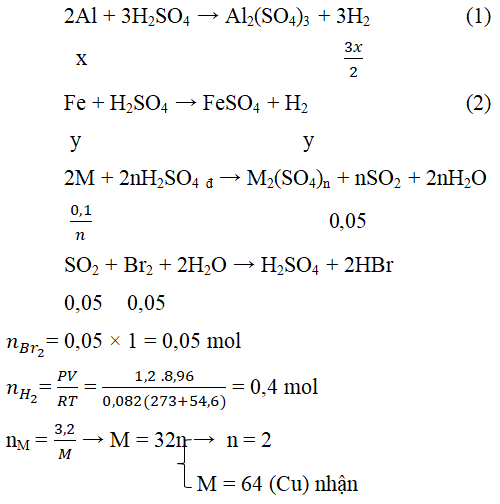
Câu 5. Khi pha loãng H2SO4 cần làm như sau:
A. Cho từ từ H2SO4 đặc vào nước và khuấy đều
B. Cho từ từ nước vào H2SO4 đặc và khuấy đều
C. Cho nước và axit đồng thời
D. Lấy 2 phần nước pha với một phần axit.
Lời giải:
Đáp án: A
H2SO4 đậm đặc rất háo nước. Khi tan vào nước tỏa ra một nhiệt lượng lớn. Nếu cho H2O vào axit khi đó nước sẽ sôi tức thời và bắn tung tóe ra ngoài mang theo axit, sẽ gây bỏng. Do đó, phải cho H2SO4 vào nước và khuấy từ từ để nhiệt tản dần khắp dung dịch
Câu 6. Cho phương trình phản ứng hóa học:
H2SO4 đặc + 8HI → 4I2 + H2S + 4H2O
A. H2SO4 là chất oxi hóa, HI là chất khử
B. HI là chất oxi hóa
C. I2 oxi hóa H2S thành H2SO4 và nó bị khử thành HI
D. I2 khử H2S thành H2SO4 và nó bị khử thành HI.
Lời giải:
Đáp án: A
Câu 7. Cho 3,68 gam hỗn hợp gồm Al và Zn tác dụng với một lượng vừa đủ dung dịch H2SO4 10% thu được 2,24 lít khí H2 (ở đktc). Khối lượng dung dịch thu được sau phản ứng là:
A. 101,48g B. 101,68g C. 97,80g D. 88,20g
Lời giải:
Đáp án: B
Ta có: nH2SO4 = nH2 = 2,24/22,4 = 0,1 mol
→ mH2SO4 = 0,1 × 98 = 9,8g → mdd H2SO4 = (9,8×100)/10 = 98g
Áp dụng định luật bảo toàn khối lượng:
mhỗn hợp KL + mdd H2SO4 = mdd sau phản ứng + mH2
→ mdd sau phản ứng = mhỗn hợp KL + mdd H2SO4 - mH2 = 3,68 + 98 – 0,1 × 2 = 101,48g
Câu 8. Hòa tan hoàn toàn 49,6 gam hỗn hợp X gồm Fe, FeO, Fe2O3 Fe3O4 bằng H2SO4 đặc, nóng thu được dung dịch Y và 8,96 lít SO2 (đktc)
a, Tính phần trăm khối lượng của oxi trong hỗn hợp X.
b, Tính khôi lượng muối thu được trong dung dịch Y
Lời giải:
Đáp án:
Quy hỗn hợp X về hai chất FeO và Fe2O3
Phản ứng:
Và mmuối = 400(0,4 – 0,05) = 140 (gam)
Xem thêm các dạng bài tập Hóa học hay khác:
Lí thuyết về Kim loại kiềm thổ (2024) chi tiết nhất
Lí thuyết về kim loại kiềm (2024) chi tiết nhất
Lí thuyết kim loại tác dụng với HNO3 (2024) chi tiết nhất