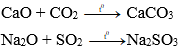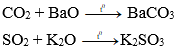Lí thuyết phân loại oxit
1. Lí thuyết
1.1 Phân loại
Căn cứ vào tính chất hóa học của oxit, người ta phân loại oxit thành 4 loại như sau:
- Oxit bazơ là những oxit tác dụng với dung dịch axit tạo thành muối và nước.
- Oxit axit là những oxit tác dụng với dung dịch bazơ tạo thành muối và nước.
- Oxit lưỡng tính là những oxit tác dụng với dung dịch axit và tác dụng với dung dịch bazơ tạo thành muối và nước.
- Oxit trung tính hay còn gọi là oxit không tạo muối là những oxit không tác dụng với axit, bazơ, nước.
1.2 Kiến thức mở rộng
Tính chất hóa học của oxit
- Oxit bazơ: Oxit bazơ có những tính chất hóa học nào ?
+ Tác dụng với nước: Một số oxit bazơ tác dụng với nước tạo thành dung dịch bazơ (kiềm).
Ví dụ:
Na2O + H2O → 2NaOH
BaO + H2O → Ba(OH)2
Những oxit bazơ tác dụng với nước tạo thành dung dịch kiềm là: Li2O, Na2O, K2O, Rb2O, Cs2O, CaO, BaO, SrO.
+ Tác dụng với axit: Oxit bazơ + axit → muối + nước
Ví dụ:
BaO + 2HCl → BaCl2 + H2O
Fe2O3 + 3H2SO4 → Fe2(SO4)3 + 3H2O
+ Tác dụng với oxit axit: Một số oxit bazơ, là những oxit bazơ tan trong nước tác dụng với oxit axit tạo thành muối.
Ví dụ:
- Oxit axit: Oxit axit có những tính chất hóa học nào ?
+ Tác dụng với nước: Nhiều oxit axit tác dụng với nước tạo thành dung dịch axit.
Ví dụ:
SO3 + H2O → H2SO4
P2O5 + 3H2O → 2H3PO4
Những oxit khác như SO2, N2O5 … cũng có phản ứng tương tự.
+ Tác dụng với dung dịch bazơ: Oxit axit + dung dịch bazơ → muối + nước.
Ví dụ:
CO2 + Ca(OH)2 → CaCO3 (↓) + H2O
CO2 + 2NaOH → Na2CO3 + H2O
Những oxit khác như SO2, P2O5 …cũng có phản ứng tương tự.
+ Tác dụng với oxit bazơ: Oxit axit tác dụng với một số oxit bazơ (tan) tạo thành muối.
Ví dụ:
- Oxit lưỡng tính: Một số oxit vừa tác dụng dung dịch axit, vừa tác dụng với dung dịch bazơ, gọi là oxit lưỡng tính như: Al2O3, ZnO, Cr2O3, PbO…
Ví dụ:
Al2O3 + 6HCl → 2AlCl3 + 3H2O
Al2O3 + 2NaOH → H2O + 2NaAlO2 (natri aluminat)
- Oxit trung tính (hay là oxit không tạo muối): Một số oxit không tác dụng với axit, dung dịch bazơ, nước gọi là oxit trung tính như: NO, N2O, CO,…
2. Bài tập vận dụng
Bài 1: Oxit nào sau đây phản ứng với nước ở điều kiện thường?
A. Al2O3
B. CuO
C. Na2O
D. MgO
Lời giải
Các oxit bazơ của kim loại kiềm và kiềm thổ (trừ BeO, MgO) tác dụng được với nước ở điều kiện thường.
Na2O + H2O → 2NaOH
Đáp án: C
Bài 2: Trong những dãy oxit sau, dãy gồm những chất tác dụng được với nước để tạo ra dung dịch kiềm là:
A. CuO, CaO, Na2O, K2O
B. CaO, Na2O, K2O, BaO
C. CuO, Na2O, BaO, Fe2O3
D. PbO, ZnO, MgO, Fe2O3
Lời giải
Ghi nhớ: các oxit của kim loại kiềm và kiềm thổ (trừ BeO, MgO) tác dụng được với nước ở điều kiện thường tạo ra dung dịch bazo
A. loại CuO
B. thỏa mãn
C. loại CuO; Fe2O3
D. loại tất cả
Đáp án cần chọn là: B
Bài 3: Dãy các chất nào tác dụng được với nước?
A. SO2, CO2, Na2O, CaO
B. NO,CO, Na2O, CaO
C. SO2, CO2, FeO, CaO
D. NO, CO, Na2O, FeO
Lời giải
A đúng
B sai do NO,CO là không tác dụng với nước
C sai do FeO không tác dụng với nước
D sai do NO, CO, FeO không tác dụng với nước
Đáp án: A
Bài 4: Khí cacbon monooxit (CO) có lẫn tạp chất là khí cacbon đioxit (CO2) và lưu huỳnh đioxit (SO2). Dùng dung dịch nào sau đây để tách được những tạp chất ra khỏi CO?
A. Dung dịch HCl
B. Dung dịch Ca(OH)2
C. Dung dịch H2SO4
D. Dung dịch NaCl
Lời giải
Dẫn hỗn hợp khí qua dung dịch bazơ dư, các tạp chất là oxit axit bị giữ lại. Khí đi ra khỏi dung dịch là CO (oxit trung tính không tác dụng với bazơ)
PTHH: CO2 + Ca(OH)2 → CaCO3 ↓ + H2O
SO2 + Ca(OH)2 → CaSO3 ↓ + H2O
Đáp án: B
Bài 5: Cho 15,3 gam oxit của kim loại hóa trị II vào nước thu được 200 gam dung dịch bazơ với nồng độ 8,55%. Công thức của oxit trên là
A. Na2O
B. CaO
C. BaO
D. K2O
Lời giải
Đặt công thức hóa học của oxit là MO
PTHH: MO + H2O → M(OH)2
Ta có:
mM(OH)2 = gam
Theo phương trình, ta có:
=> kim loại M là Ba
=> công thức oxit là BaO
Đáp án: C
Bài 6: Hòa tan hoàn toàn 10 gam MgO cần dùng vừa đủ 400 ml dung dịch HCl aM thu được dung dịch X. Giá trị của a là
A. 1,50M
B. 1,25M
C. 1,35M
D. 1,20M
Lời giải
nMgO = 0,25 mol
MgO + 2HCl → MgCl2 + H2O
0,25 → 0,5 mol
=> Nồng độ của dung dịch HCl là
Đáp án: B
Bài 7: Hòa tan hoàn toàn 53,6 gam hỗn hợp A gồm (FeO, CuO) cần dùng vừa đủ 500 ml dung dịch H2SO4 1,4M (D = 1,2g/ml) thu được dung dịch X. Giả thiết thể tích của dung dịch sau phản ứng thay đổi không đáng kể. Nồng độ phần trăm của muối FeSO4 trong dung dịch X là
A. 7,04%
B. 6,06%
C. 9,30%
D. 6,98%
Lời giải
Gọi số mol của FeO và CuO lần lượt là x và y mol
=> mhỗnhợp = mFeO + mCuO => 72x + 80y = 53,6 (1)
nH2SO4 = 0,5.1,4 = 0,7 mol
FeO + H2SO4 → FeSO4 + H2O
x → x → x
CuO + H2SO4 → CuSO4 + H2O
y → y
=> nH2SO4 = x + y = 0,7 (2)
Từ (1) và (2) => x = 0,3 mol; y = 0,4 mol
Ta có: m dung dịch H2SO4 = D.V = 1,2.500 = 600 gam
=> m dd trước phản ứng = m hỗn hợp A + m dd H2SO4 = 53,6 + 600 = 653,6 gam
Vì phản ứng không tạo chất khí hay chất kết tủa
=> m dd sau phản ứng = m dd trước phản ứng = 653,6 gam
Đáp án: D
Bài 8: Cho 20 gam hỗn hợp X gồm CuO và Fe2O3 tác dụng vừa đủ với 0,2 lít dung dịch HCl có nồng độ 3,5M. Thành phần phần trăm theo khối lượng của CuO và Fe2O3 trong hỗn hợp X lần lượt là :
A. 25% và 75%
B. 20% và 80%
C. 22% và 78%
D. 30% và 70%
Lời giải
Gọi a là số mol của CuO và b là số mol của Fe2O3 có trong 20 gam
hh 200 ml dd HCl 3,5 M => nHCl = 0,2 . 3,5 = 0,7 mol
CuO + 2HCl → CuCl2 + H2O
a mol → 2a mol
Fe2O3 + 6HCl → 2FeCl3 + 3H2O
b mol → 6b mol
Ta có hệ PT:
m hh = m CuO + m Fe2O3 = 80a + 160b = 20
nHCl = 2a + 6b = 0,7
Giải hệ trên ta được
a = 0,05 mol b = 0,1 mol => mCuO = 0,05 . 80 = 4g
=> %CuO = 20% => %Fe2O3 = 80%
Đáp án: B
Bài 9: Sục 3,36 lít khí SO3 (đktc) vào 400 ml nước thu được dung dịch A. Biết DH2O = 1 g/ml ). Nồng độ phần trăm của chất tan trong dung dịch A là
A. 2,91%
B. 1,94%
C. 3,49%
D. 3,57%
Lời giải
nSO3 = 0,15 mol
SO3 + H2O → H2SO4
0,15 → 0,15 mol
mH2O = D.V = 400 gam
Đáp án: D
Bài 10: Hòa tan hết 12,4 gam Natrioxit vào nước thu được 500ml dung dịch A . Nồng độ mol của dung dịch A là :
A. 0,8M
B. 0,6M
C. 0,4M
D. 0,2M
Lời giải
nNa2O = 12,4 : 62 = 0,2 mol
PTHH: Na2O + H2O → 2NaOH
1 2
0,2 → 0,4
CM NaOH = nNaOH : V = 0,4 : 0,5 = 0,8M
Đáp án: A
Bài 11: Hòa tan 6,2 g Na2O vào nước được 2 lít dung dịch. Nồng độ mol của dung dịch thu được là:
A. 0,1M
B. 0,2 M
C. 0,3M
D. 0,4M
Lời giải
nNa2O = mNa2O : MNa2O = 6,2 : (23 . 2 + 16) = 0,1 mol
PTHH: Na2O + H2O → 2NaOH
Tỉ lệ 1 2
Phản ứng 0,1 ? mol
Từ PTHH => nNaOH = 2 nNa2O = 0,2 mol
Đáp án: A
Bài 12: Oxit bazơ không có tính chất hóa học nào sau đây?
A. Một số oxit bazơ tác dụng được với nước ở điều kiện thường.
B. Oxit bazơ tác dụng được với dung dịch axit.
C. Oxit bazơ tác dụng được với tất cả kim loại.
D. Một số oxit bazơ tác dụng được với oxit axit.
Lời giải
Oxit bazơ không có tính chất tác dụng được với tất cả kim loại.
Đáp án: C
Bài 13: Dãy các chất tác dụng được với oxit bazơ Na2O là:
A. H2O, SO2, HCl
B. H2O, CO, HCl
C. H2O, NO, H2SO4
D. H2O, CO, H2SO4
Lời giải
A tác dụng với Na2O
B có CO không tác dụng
C có NO không tác dụng
D có CO không tác dụng
Đáp án: A
Bài 14: Tính chất hóa học của oxit axit là
A. tác dụng với nước
B. tác dụng với dung dịch bazơ
C. tác dụng với một số oxit bazơ
D. cả 3 đáp án trên.
Lời giải
Tính chất hóa học của oxit axit là
- Tác dụng với nước.
- Tác dụng với dung dịch bazơ.
- Tác dụng với một số oxit bazơ.
Đáp án: D
Bài 15: Oxit axit có thể tác dụng được với
A. oxit bazơ
B. nước
C. bazơ
D. cả 3 hợp chất trên
Lời giải
Tính chất hóa học của oxit axit là
+ Tác dụng với nước tạo thành dung dịch axit
+ Tác dụng với dung dịch bazơ tạo thành muối và nước
+ Tác dụng với một số oxit bazơ tạo thành muối
Đáp án: D
Bài 16: Cho các oxit bazơ sau: Na2O, FeO, CuO, Fe2O3, BaO. Số oxit bazơ tác dụng với nước ở nhiệt độ thường là
A. 2
B. 3
C. 4
D. 5
Lời giải
Các oxit bazơ tác dụng được với nước ở nhiệt độ thường là: Na2O và BaO
Na2O + H2O → 2NaOH
BaO + H2O → Ba(OH)2
Đáp án: A
Bài 17: 0,05 mol FeO tác dụng vừa đủ với:
A. 0,02mol HCl
B. 0,1mol HCl
C. 0,05mol HCl
D. 0,01mol HCl
Lời giải
FeO + 2HCl → FeCl2 + H2O
nFeO = 0,05 mol
theo phương trình nHCl = 2 nFeO = 0,1 mol
Đáp án: B
Bài 18: Hòa tan 4,88 gam hỗn hợp A gồm MgO và FeO trong 200 ml dung dịch H2SO4 0,45M loãng thì phản ứng vừa đủ, thu được dung dịch B. Phần trăm khối lượng của MgO trong A là
A. 59,02%
B. 61,34%
C. 40,98%
D. 38,66%
Lời giải
Gọi số mol của MgO và FeO trong hỗn hợp A là x và y mol
Vì mA = mMgO + mFeO = 40x + 72y
→ 40x + 72y = 4,88 (1)
Phương trình hóa học
MgO + H2SO4 → MgSO4 + H2O (*)
x → x
FeO + H2SO4 → FeSO4 + H2O (**)
y → y
Theo phương trình (*):
nH2SO4 = 0,2.0,45 = 0,09 mol
→ x + y = 0,09 (2)
Từ (1) và (2) ta có hệ phương trình:
=> mMgO = 40.0,05 = 2gam => % mMgO =
Đáp án: C
Bài 19: Cho 20 gam hỗn hợp Na2O và CuO tác dụng hết với 3,36 lít SO2(đktc). Sau phản ứng thấy thu được một chất rắn không tan. Thành phần phần trăm theo khối lượng của 2 oxit trong hỗn hợp lần lượt là:
A. 46,5% và 53,5%
B. 53,5% và 46,5%
C. 23,25% và 76,75%
D. 76,75% và 23,25%
Lời giải
PTPƯ: Na2O + SO2 → Na2SO3
nNa2O = nSO2 = 3,36:22,4 = 0,15(mol)
Đáp án: A
Bài 20: Biết rằng 1,12 lít khí cacbon đioxit (đktc) tác dụng vừa đủ với 100 ml dung dịch NaOH tạo ra muối trung hòa. Nồng độ mol của dung dịch NaOH đã dùng là
A. 1M
B. 2M
C. 0,1M
D. 0,2M
Lời giải
CO2 + 2NaOH → Na2CO3 + H2O
Từ phương trình, ta có:
=> nồng độ mol của dung dịch NaOH là:
Đáp án: A
Xem thêm các dạng bài tập Hóa học hay khác:
Lí thuyết tổng hợp về tơ (2024) chi tiết nhất
Lí thuyết về thang pH (2024) chi tiết nhất
Lí thuyết đồng phân hình học (2024) chi tiết nhất
Lí thuyết về muối (2024) chi tiết và đầy đủ nhất
Lí thuyết về kim loại (2024) chi tiết nhất