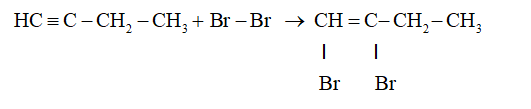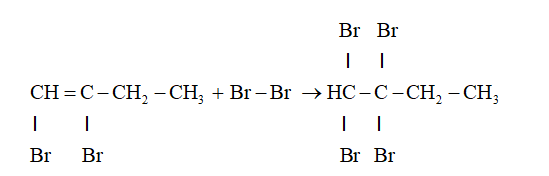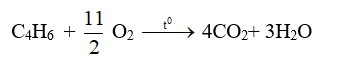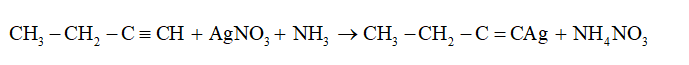Công thức, tính chất, ứng dụng của But - 1 - in
I. Lí thuyết
1. Công thức
Ankin but-1-in có công thức cấu tạo là CH ≡ C – CH2 – CH3.
2. Tính chất vật lí
- Ở điều kiện thường, butin là chất khí, không tan nước.
- Nhận biết: Ankin có nối ba đầu mạch được nhận biết bằng phản ứng thế bằng ion kim loại khi sục vào dung dịch AgNO3 trong amoniac.
3. Tính chất hóa học
Phản ứng cộng
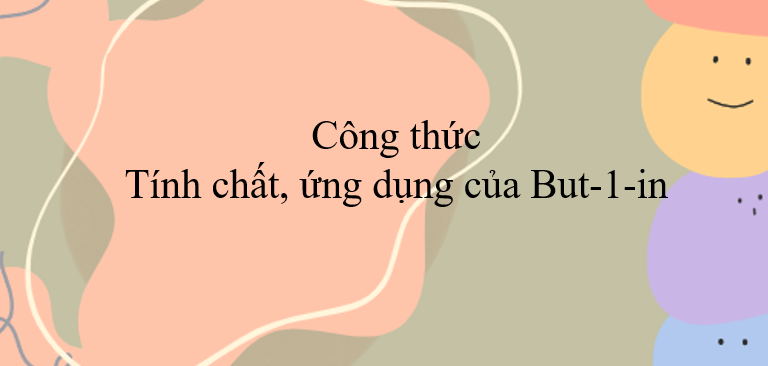
- Cộng brom
- Dẫn butin qua dung dịch brom màu da cam.
+ Hiện tượng: Dung dịch brom bị mất màu. butin có phản ứng cộng với brom trong dung dịch.
+ Sản phẩm mới sinh ra có liên kết đôi trong phân tử nên có thể cộng tiếp với một phân tử brom nữa:
+ Trong điều kiện thích hợp, butin cũng có phản ứng cộng với hiđro và một số chất khác.
- Cộng hiđro
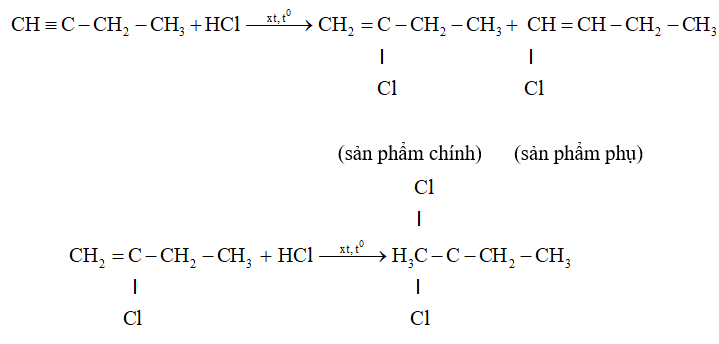
- Cộng hiđro clorua
+ Phản ứng cộng HX, H2O vào các ankin trong dãy đồng đẳng của axetilen cũng tuân theo quy tắc Mac-côp-nhi-côp như anken.
Phản ứng oxi hóa
- Butin là hiđrocacbon, vì vậy khi đốt, propin sẽ cháy tạo ra cacbon đioxit và nước, tương tự metan và etilen.
- Propin cháy trong không khí với ngọn lửa sáng, tỏa nhiều nhiệt.
Phản ứng thế bới kim loại
- Tính chất riêng của các ankin có nối ba đầu mạch
II. Bài tập vận dụng
Câu 1: Hỗn hợp khí X gồm 0,3 mol H2 và 0,1 mol vinylaxetilen. Nung X một thời gian với xúc tác Ni thu được hỗn hợp khí Y có tỉ khối so với không khí là 1. Tính số mol H2 phản ứng?
A. 2,24 lít
B. 4,48 lít
C. 10,08 lít
D. 5,04 lít
Hướng dẫn giải:
Theo bài:
Bảo toàn khối lượng: mY = mX = 0,3.2 + 0,1.52 = 5,8g
nY=mYMY=5,829=0,2mol
nH2
Đáp án B
Câu 2: Cho 2,24 lít (đktc) hỗn hợp X gồm C2H4 và C2H2 lội chậm qua bình đựng dung dịch Br2 dư thấy khối lượng bình tăng thêm 2,7 gam. Thành phần phần trăm thể tích của C2H2 có trong hỗn hợp X là
A. 40%
B. 50%
C. 60%
D. 75%
Hướng dẫn giải
Gọi số mol của C2H4 và C2H2 lần lượt là x và y mol
x + y = 0,1 (1)
Ta có khối lượng bình tăng bằng khối lượng hỗn hợp khí X 28x + 26y = 2,7 (2)
Từ (1) và (2) x = y = 0,05
Phần trăm thể tích bằng phần trăm số mol khí.
Đáp án B
Câu 3: Cho m gam propin tác dụng với H2 dư (Ni, ) thu được (m + 8) gam sản phẩm hữu cơ Y. Giá trị của m là:
A. 80 gam
B. 40 gam
C. 160 gam
D. 120 gam
Hướng dẫn giải
Đáp án A
Câu 4: Đun nóng hỗn hợp khí gồm 0,06 mol C2H2 và 0,04 mol H2 với xúc tác Ni, sau một thời gian thu được hỗn hợp khí Y. Dẫn toàn bộ hỗn hợp Y lội từ từ qua bình đựng dung dịch brom (dư) thì còn lại 0,448 lít hỗn hợp khí Z (ở đktc) có tỉ khối so với O2 là 0,5. Khối lượng bình dung dịch brom tăng là
A. 1,20 gam
B. 1,04 gam
C. 1,64 gam
D. 1,32 gam
Hướng dẫn giải
Gọi m gam là khối lượng bình dung dịch brom tăng.
Bảo toàn khối lượng ta có:
0,06.26 + 0,04.2 = 0,02.0,5.32 + m
m = 1,32 gam
Đáp án D
Câu 5: Khi cho brom phản ứng hoàn toàn 0,3 mol hỗn hợp gồm một ankin và một anken cần vừa đủ 0,4 mol Br2. Thành phần phần trăm về số mol của ankin trong hỗn hợp là:
A. 75%
B. 25%
C. 33,33%
D. 66,67%
Hướng dẫn giải
Gọi
Ta có:
a + 2b = 0,4 (2)
Từ (1) và (2) a = 0,2 mol; b = 0,1 mol
% n ankin = 0,1.100/0.3 = 33,33%
Đáp án C
Câu 6: Hỗn hợp X gồm một hiđrocacbon (khí) và H2, với . Cho hỗn hợp đi qua Ni nung nóng, sau khi phản ứng xảy ra hoàn toàn thu được hỗn hợp Y có . Công thức phân tử của hiđrocacbon trong X là
A. C3H4.
B. C3H6.
C. C4H8.
D. C4H6.
Hướng dẫn giải
Bảo toàn khối lượng: mX = mY
Giả sử nhhX = 5 mol; nhhY = 2 mol.
Ta có
hiđrocacbon là CnH2n – 2 có số mol bằng
ban đầu có CnH2n - 2 1,5 mol và H2 3,5 mol.
n = 3 C3H4
Đáp án A
Câu 7: Một hỗn hợp X gồm một anken và một ankin. Cho 0,1 mol hỗn hợp X vào nước brom dư thấy có 0,16 mol Br2 đã tham gia phản ứng. Mặt khác, đốt cháy hoàn toàn 0,1 mol hỗn hợp X thu được 0,28 mol CO2. Vậy 2 chất trong hỗn hợp X là
A. C2H4 và C3H4
B. C4H8 và C2H2
C. C3H6 và C2H2
D. C3H6 và C3H4
Hướng dẫn giải
0,1 mol X + O2 0,28 mol CO2
Bảo toàn C ta có: 0,04n + 0,06m = 0,28 2n + 3m = 14.
Ta thấy n = 4; m = 2 là giá trị thỏa mãn X là C4H8 và C2H2
Đáp án B
Câu 8: Dẫn 2,24 lít hỗn hợp gồm etilen, propilen, propen, các buten và axetilen (ở đktc) qua dung dịch brom dư thì thấy khối lượng brom trong bình giảm 19,2 gam. Lượng CaC2 cần dùng để điều chế được lượng axetilen có trong hỗn hợp trên là
A. 6,4 gam
B. 3,2 gam
C. 2,56 gam
D. 1,28 gam
Hướng dẫn giải
Anken + Br2 Sp
Ankin + 2Br2 Sp
naxetilen = = 0,12 - 0,1 = 0,02 mol
Đáp án D
Câu 9: Hỗn hợp X gồm C2H2 và H2 (có tỉ lệ mol tương ứng là 1 : 2). Đun nóng 10,08 lít (đktc) hỗn hợp X với xúc tác Ni, sau một thời gian thu được hỗn hợp khí Y. Dẫn hỗn hợp Y qua dung dịch nước brom dư, thấy bình brom tăng 3 gam và còn lại V lít (đktc) hỗn hợp khí Z không bị hấp thụ. Tỉ khối của Z so với heli bằng 5/3. Giá trị của V là
A. 13,44 lít
B. 4,48 lít
C. 10,08 lít
D. 5,04 lít
Hướng dẫn giải
Ta có mX = mY = mbình tăng + mZ
0,15. 26 + 0,3. 2 = 3 + mZ mZ = 1,5 gam
V= 5,04 lít.
Đáp án D
Câu 10: Cho 28,2 gam hỗn hợp X gồm 3 ankin đồng đẳng kế tiếp qua một lượng dư H2 (, Ni) để phản ứng xảy ra hoàn toàn. Sau phản ứng thể tích thể tích khí H2 giảm 26,88 lít (đktc). Công thức phân tử của 3 ankin là
A. C2H2, C3H4, C4H6.
B. C4H6, C5H8, C6H10.
C. C3H4, C4H6, C5H8.
D. Cả A và C đều đúng
Hướng dẫn giải
Ta có: số mol khí giảm = số mol H2 tham gia phản ứng = 1,2 mol
tổng số mol hỗn hợp = = 0,6
Hỗn hợp có thể là C2H2, C3H4, C4H6 hoặc C3H4, C4H6, C5H8
Đáp án D
Xem thêm các dạng bài tập Hóa học hay khác:
Công thức, tính chất, ứng dụng của axit panmitic (2024) hay, chi tiết nhất
Công thức, tính chất, ứng dụng của axit metacrylic (2024) hay, chi tiết nhất
Các chuỗi phản ứng thường gặp (2024) hay nhất
Cách viết phương trình phân tử và ion rút gọn (2024) hay, chi tiết nhất
Lý thuyết cấu tạo chất (2024) hay, chi tiết nhất