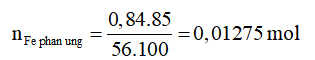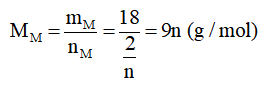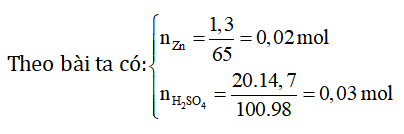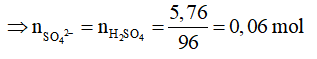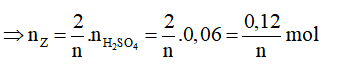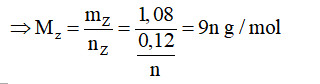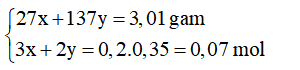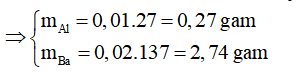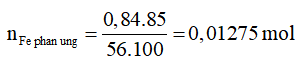Công thức, tính chất, ứng dụng của axit metacrylic
1. Lí thuyết
1.1 Công thức
Axit metacrylic là một hợp chất axit hữu cơ không no và có công thức hóa học là: CH2=C(CH3)−COOH. Nó có mùi đặc trưng rất khó chịu là mùi chát và chua.
1.2 Tính chất vật lí và hóa học
Tính chất vật lí
- Axit metacrylic tồn tại dưới dạng là một dung dịch chất lỏng, không màu và có mùi rất là khó ngửi
- Ngoài ra nó còn có thể bị hòa tan trong nước ấm và trộn với các dung môi hữu cơ khác.
- Nhiệt độ nóng chảy: 16∘C
- Nhiệt độ sôi: 160,5∘C
- Mật độ: 1,02 g/cm³
- Khối lượng phân tử: 86,06 g/mol
Tính chất hóa học
- Phản ứng với Brom:
CH2=C(CH3)COOH + Br2 → CH2Br−CBr(CH3)−COOH
- Tác dụng với NaOH:
NaOH + CH2=C(CH3)COOH → H2O + CH2=C(CH3)COONa
Axit metacrylic phản ứng với H2:
CH2=C(CH3)−COOH + H2 → CH3−CH(CH3)−COOH
- Phản ứng este hóa:
CH3OH + CH2=C(CH3)COOH → CH2=C(CH3)COOCH3 + H2O
- Ngoài ra còn tác dụng với ancol metylic:
CH3OH + CH2=C(CH3)COOH → CH2=C(CH3)COOCH3 + H2O
1.3 Ứng dụng
- Đây là nguyên liệu chủ yếu để sản xuất nhựa
- Không chỉ vậy được sử dụng tạo ra phôi sản phẩm trong các nhà máy sản xuất nhựa.
- Được sử dụng trong việc làm đẹp có trong thành phần của một số loại sơn lót móng tay.
2. Bài tập vận dụng
Bài 1: Người ta lấy 688 gam axit metacrylic tác dụng với 320 gam rượu metylic, thu được este với hiệu suất 60%. Nếu đem lượng este này trùng hợp để tạo thủy tinh hữu cơ (plexiglas), hiệu suất 80%, thì khối lượng polyme thu được sẽ là bao nhiêu?
A. 384 gam
B. 480 gam
C. 348 gam
D. Tất cả đều sai
Đáp án: A. 384 gam
axit metacrylic có công thức:
;
=> rượu metylic dư => thu được là:
Bài 2: Cho các kim loại được ghi bằng các chữ cái: A, B, C, D tác dụng riêng biệt với dung dịch HCl. Hiện tượng quan sát được ghi trong bảng dưới đây:
| Kim loại | Tác dụng của dung dịch HCl |
| A | Giải phóng hidro chậm |
| B | Giải phóng hidro nhanh, dung dịch nóng dần |
| C | Không có hiện tượng gì xảy ra |
| D | Giải phóng hidro rất nhanh, dung dịch nóng lên |
Theo em nếu sắp xếp 4 kim loại trên theo chiều hoạt động hoá học giảm dần, thì cách sắp xếp nào đúng trong các cách sắp xếp sau:
A. D, B, A, C
B. C, B, A, D
C. A, B, C, D
D. B, A, D, C
Đáp án: A. D, B, A, C
Kim loại cho tác dụng với HCl không có hiện tượng gì xảy ra Kim loại không tác dụng với HCl → C là kim loại yếu đứng sau Hidro.
Kim loại càng mạnh (càng hoạt động hóa học) khi tác dụng với HCl phản ứng xảy ra càng mãnh liệt, rõ ràng. (Khí thoát ra nhiều, dung dịch nóng lên).
→ Thứ tự kim loại hoạt động hóa học giảm dần là: D, B, A, C.
Bài 3: Hòa tan hoàn toàn 18 gam một kim loại M cần dùng 800ml dung dịch HCl 2,5M. Kim loại M là kim loại nào sau đây? (biết hóa trị của kim loại trong khoảng từ I đến III).
A. Ca
B. Mg
C. Al
D. Fe
Đáp án: C. Al
2M + 2nHCl → 2MCln + nH2
2/n <…...2 …………………………..mol
Vậy
⇒ nH2 = nFe pư = 0,01275 mol
⇒ VH2 = 0,01275.22,4 = 0,2856 mol
Nếu n = 1 thì MM = 9 → loại
Nếu n = 2 thì MM = 18 → loại
Nếu n = 3 thì MM = 27 → M là kim loại Al
Bài 4: Cho hỗn hợp Al và Fe tác dụng với hỗn hợp dung dịch chứa AgNO3 và Cu(NO3)2 thu được dung dịch B và chất rắn D gồm 3 kim loại. Cho D tác dụng với dung dịch HCl dư, thấy có khí bay lên. Thành phần chất rắn D là:
A. Al, Fe, Cu
B. Fe, Cu, Ag
C. Al, Cu, Ag
D. Kết quả khác
Đáp án: B. Fe, Cu, Ag
Al là kim loại mạnh nhất nên Al sẽ phản ứng đầu tiên → Al sẽ bị hòa tan hết → 3 kim loại thu được là Ag, Cu và Fe dư.
Bài 5: Để hòa tan hoàn toàn 1,3 gam kẽm thì cần 14,7 gam dung dịch H2SO4 20%. Khi phản ứng kết thúc khối lượng hiđro thu được là:
A. 0,03 gam
B. 0,06 gam
C. 0,04 gam
D. 0,02 gam
Đáp án: C. 0,04 gam
Zn + H2SO4 → ZnSO4 + H2
⇒ Zn phản ứng hết, dd axit còn dư
⇒ nH2 = nZn = 0,02 mol
⇒ mH2 = 2.0,02 = 0,04 g
Bài 6: Hòa tan 2,7 gam kim loại A bằng dung dịch H2SO4 loãng dư. Sau phản ứng thu được 3,36 lít H2 (đktc). Kim loại A là:
A. Fe
B. Sn
C. Zn
D. Al
Đáp án: D. Al
Bài 7: Cho 1,08 gam kim loại Z vào dung dịch H2SO4 loãng dư. Lọc dung dịch, đem cô cạn thu được 6,84 gam một muối khan duy nhất. Vậy kim loại Z là:
A. Niken
B. Canxi
C. Nhôm
D. Sắt
Đáp án: C. Nhôm
2Z + nH2SO4 → Z2(SO4)n + nH2
Ta có:
mZ + mSO42- = mmuoi
mSO42- = mmuoi - mZ = 6,84-1,08=5,76g
Thử chọn lần lượt n=1, 2, 3 ta được Z là kim loại Al hóa trị III
Bài 8: Có 4 kim loại X, Y, Z, T đứng sau Mg trong dãy hoạt động hoá học. Biết rằng:
-X và Y tác dụng với dung dịch HCl giải phóng khí hidro.
-Z và T không phản ứng với dung dịch HCl.
-Y tác dụng với dung dịch muối của X và giải phóng X.
-T tác dụng được với dung dịch muối của Z và giải phóng Z.
Hãy xác định thứ tự sắp xếp nào sau đây là đúng (theo chiều hoạt động hóa học giảm dần)
A. Y, T, Z, X
B. T, X, Y, Z
C. Y, X, T, Z
D. X, Y, Z, T
Đáp án: C. Y, X, T, Z
- X và Y tác dụng với dung dịch HCl giải phóng khí hidro → X, Y đứng trước Hidro trong dãy hoạt động hóa học.
- Z và T không phản ứng với dung dịch HCl → Z, T đứng sau Hidro trong dãy hoạt động hóa học.
→ X, Y là kim loại mạnh hơn Z, T.
- Y tác dụng với dung dịch muối của X và giải phóng X → Y là kim loại mạnh hơn X.
- T tác dụng được với dung dịch muối của Z và giải phóng Z → T là kim loại mạnh hơn Z.
→ thứ tự sắp xếp các kim loại (theo chiều hoạt động hóa học giảm dần) là: Y, X, T, Z
Bài 9: Để hòa tan hoàn toàn 3,01 gam bột gồm nhôm và bari thì cần vừa đủ 350ml dung dịch HCl 0,2M. Theo em khối lượng mỗi kim loại trong hỗn hợp ban đầu là bao nhiêu ?
A. 0,19 g và 2,82 g
B. 0,95 g và 2,06 g
C. 0,27 g và 2,74 g
D. 3 g và 0,01 g
Đáp án: C. 0,27 g và 2,74 g
Gọi số mol của Al và Ba lần lượt là x, y (mol)
Theo đề bài và theo phương trình phản ứng, ta lập được hệ sau:
Giải hệ, ta được: x = 0,01 mol, y = 0,02 mol
Bài 10: Cho 0,84 gam sắt vào dung dịch HCl dư. Sau phản ứng ta được muối clorua và khí H2, biết hiệu suất phản ứng là 85%. Thể tích H2 thu được (đktc) là:
A. 0,15 lit
B. 0,1256 lit
C. 0,2856 lit
D. kết quả khác.
Đáp án: C. 0,2856 lit
Fe + 2HCl → FeCl2 + H2
Vì H = 85% nên:
nH2 = nFe pư = 0,01275 mol
VH2 = 0,01275.22,4= 0,2856 lit
Xem thêm các dạng bài tập Hóa học hay khác:
Lí thuyết về kim loại kiềm (2024) chi tiết nhất
Lí thuyết kim loại tác dụng với HNO3 (2024) chi tiết nhất
Lí thuyết về Kim loại kiềm thổ (2024) chi tiết nhất
Lí thuyết Kim loại tác dụng với axit H2SO4 (2024) chi tiết nhất