Cho các liên kết và giá trị năng lượng liên kết (Eb) của một số liên kết cộng hoá trị như sau
264
15/11/2023
Bài 16.22 trang 80 Sách bài tập Hóa học 11: Cho các liên kết và giá trị năng lượng liên kết (Eb) của một số liên kết cộng hoá trị như sau:
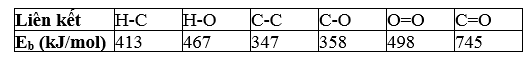
a) Tính biến thiên enthalpy chuẩn của phản ứng đốt cháy hơi ethanol.
b) Khi đốt cháy cùng số mol ethanol và methanol, nhiệt năng của phản ứng nào tạo ra nhiều hơn?
Trả lời
a) Phương trình hoá học của phản ứng đốt cháy hơi ethanol:
C2H5OH(g) + 3O2(g) →2CO2(g) + 3H2O(g)
Công thức tính biến thiên enthalpy của phản ứng dựa vào năng lượng liên kết như sau:
ΔrHo298=∑Eb(cd)−∑Eb(sp)
ΔrHo298 = 5×Eb(C-H) + Eb(C-C) + Eb(C-O) + Eb(O-H) + 3×Eb(O=O) - 2×2×Eb(C=O) - 3×2×Eb(O-H)
= 5×413+ 347+ 358+ 467+ 3×498-4×745-6×467 = -1 051 (kJ).
b) Phương trình hoá học của phản ứng đốt cháy hơi methanol:
CH3OH(g) + 32 O2(g) →CO2(g) + 2H2O(g)
Công thức tính biến thiên enthalpy của phản ứng dựa vào năng lượng liên kết như sau :
ArH°298 = 3×Eb(C-H) + Eb(C-O) + Eb(O-H) + 1,5×Eb(O=O) - 2×Eb(C=O) - 4×Eb(O-H)
= 3×413 + 358 + 467+ 1,5×498 - 2×745 - 4×467 = -547 (kJ).
Vậy khi đốt cháy cùng số mol methanol và ethanol thì ethanol giải phóng nhiệt năng lớn hơn.
Xem thêm các bài giải SBT Hóa học lớp 11 Chân trời sáng tạo hay, chi tiết khác:

