Bài tập về toluen
I. Lí thuyết và phương pháp giải
1. Định nghĩa
Toluen là một hợp chất hyđrocacbon thơm. Đây là một chất lỏng trong suốt, có mùi thơm nhẹ, không tan trong cồn,
ether, acetone và hầu hết các dung môi hữu cơ khác, tan ít trong nước.
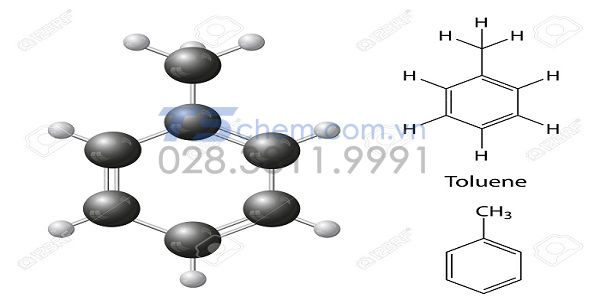
Toluen có công thức là C7H8.
Toluen còn có các tên gọi khác nhau đó là metylbenzen hay phenylmetan, Toluol, …
2. Tính chất vật lý
- Toluen là dang chất lỏng trong suốt mùi thơm nhẹ và không vị. Toluen có khả năng bay hơi lớn và dễ cháy, dễ bắt lửa.
- Toluen không tan trong cồn, ether, acetone và các dung môi hữu cơ khác, tan ít trong nước.
- Khối lượng phân tử của Toluen là 92.14 g/mol.
- Tỷ trọng của Toluen là 0.8669 g/cm3.
- Độ hoà tan trong nước của Toluen là 0,053 g/100 mL (20-25 °C).
- Nhiệt độ nóng chảy của Toluen là −93 độ C.
- Nhiệt độ sôi của Toluen là 110.6 độ C.
- Nhiệt độ tới hạn của Toluen là 320 độ C.
- Độ nhớt của Toluen là 0,590 cP ở 20 độ C.
3. Tính chất hóa học
- Toluen tham gia phản ứng với chất brom khan cho ra brom toluen và axit HBr
Br2 + C6H5CH3 → C6H5CH2Br + HBr
- Toluen tham gia phản ứng với khí clo tạo thành diclometan và axit HCl trong điều kiện có sự xúc tác của ánh sáng.
Cl2 + C6H5CH3 → HCl + C6H5CH2Cl
- Toluen tham gia phản ứng với nitro hóa tạo ra nitrotoluen và nước .
- Toluen tham gia phản ứng cộng với H2 tạo ra metylxiclohexan.
- Toluen tham gia phản ứng oxy hóa với nhóm metyl.
4. Ứng dụng

- Toluen ứng dụng như là một dung môi hàng đầu của các ngành công nghiệp.
- Toluen được dùng chủ yếu trong làm dung môi như dung môi pha sơn, chất pha loãng.
- Toluen được dùng để sản xuất nhựa tổng hợp, sản xuất keo dán và các sản phẩm cùng loại, dùng trong keo dán cao su, xi măng cao su, …
- Toluen được dùng làm chất cải thiện một vài chỉ số của xăng dầu, và làm chất mang phụ gia cho nhiên liệu.
- Toluen cũng được ứng dụng vào sản xuất mỹ phẩm đặc biệt là nước hoa.
- Ngoài ra, Toluen còn được ứng dụng như chất tẩy rửa, dùng để sản xuất thuốc nhuộm và điều chế thuốc nổ
- TNT cũng như sản xuất mực in.
5. Phương pháp giải
+ Bước 1: Tính số mol các chất đề bài đã cho số liệu và viết phương trình phản ứng hóa học xảy ra.
+ Bước 2: Tính toán luôn theo phương trình phản ứng hóa học hoặc đặt ẩn nếu đề bài là hỗn hợp.
+ Bước 3: Lập phương trình toán học và giải phương trình Số mol các chất cần tìm.
+ Bước 4: Tính toán theo yêu cầu đề bài.
Lưu ý: Trong một hỗn hợp mà có nhiều phản ứng xảy ra thì phản ứng trung hoà được ưu tiên xảy ra trước.
II. Ví dụ minh họa
Ví dụ 1: khi đun nóng toluen không tác dụng với chất nào?
Lời giải:
Khi đun nóng toluen không tác dụng được với NaOH
Ví dụ 2: Cho dãy các chất sau: toluen, phenyl fomat, fructozơ, glyxylvalin (Gly-val), etylen glicol, triolein. Số chất bị thủy phân trong môi trường axit là?
Lời giải:
Trong dãy chất trên, có 3 chất bị thủy phân trong môi trương axit, đó là phenyl fomat, glyxylvalin (Gly-val), triolein.
Ví dụ 3: Khi nitro hóa toluen thu được hỗn hợp sản phẩm là?
Lời giải:
o – nitrotoluen và p – nitrotoluen.
III. Bài tập vận dụng
Bài 1: Hãy phân biệt toluen và stiren
Lời giải:
- Toluen và stiren đều là các hợp chất hữu cơ không màu và không tan trong nước. Tuy nhiên, chúng có những đặc điểm khác nhau giúp phân biệt chúng như sau:
- Công thức hóa học: Toluen có công thức hóa học là C7H8, trong khi đó stiren có công thức hóa học là C8H8.
- Mùi: Toluen có mùi hăng và được sử dụng như một dung môi trong các sản phẩm như sơn, dầu mỡ và keo. Stiren không có mùi và được sử dụng chủ yếu để sản xuất polymer.
- Điểm sôi: Điểm sôi của toluen là 110,6 độ C, trong khi đó điểm sôi của stiren là 145,8 độ C.
- Tính chất hoá học: Toluen là một hợp chất bền vững và không dễ cháy. Stiren, tuy nhiên, là một hợp chất cháy nổ và dễ phản ứng với oxy trong không khí.
- Ứng dụng: Toluen được sử dụng chủ yếu như một dung môi và một thành phần trong sản xuất nhựa và cao su. Stiren được sử dụng để sản xuất polystyren và các sản phẩm polymer khác.
Bài 2: Cho dãy các chất: stiren, ancol benzylic, anilin, toluen, phenol. Số chất trong dãy có khả năng làm mất màu nước brom là
Lời giải:
Stiren, anilin và phenol
Bài 3: Dùng một hóa chất nào sau đây để nhận biết các chất sau: stiren, toluen, phenol
Lời giải:
Dung dịch Br2
Bài 4: Cho các monome sau: stiren, toluen, metyl axetat, etylen oxit, vinyl axetat, caprolactam, metyl metacrylat, metyl acrylat, propilen, benzen, axit etanoic, axit ε-aminocaproic, acrilonitrin. Số monome tham gia phản ứng trùng hợp là:
Lời giải:
Gồm stiren, etylen oxit, vinyl axetat, caprolactam, metyl metacrylat, metyl acrylat, propilen, acrilonitrin.
Bài 5: hoạt tính sinh học của benzen toluen là gì ?
Lời giải:
Hoạt tính sinh học của benzen, toluen là : Gây hại cho sức khỏe.
Bài 6: Để nhận biết 3 chất lỏng bị mất nhãn: Benzen, toluen, stiren chỉ cần dùng một thuốc thử là
Lời giải:
Để nhận biết 3 chất lỏng bị mất nhãn:Benzen, toluen, stiren chỉ cần dùng một thuốc thử là dung dịch KMnO4.
– Stiren làm mất màu dung dịch KMnO4 ngay ở nhiệt độ thường
3C6H5-CH=CH2 + 2KMnO4 + 4H2O → 3C6H5-CH(OH)-CH2(OH) + 2MnO2 ↓ đen+2KOH
– Toluen không làm mất màu dung dịch KMnO4 ở điều kiện thường nhưng làm mất màu dung dịch KMnO4 khi đun nóng.
C6H5CH3 + 2KMnO4 Cách nhận biết stiren nhanh nhất C6H5COOK + 2MnO2 ↓ đen + KOH + H2O
– Benzen không làm mất màu dung dịch KMnO4 ở nhiệt độ thường và cả khi đun nóng.
Bài 7: nhận biết các chất sau: benzen, toluen, stiren và hex-1-in
Lời giải:
– Dùng dd AgNO3/NH3 nhận được hex – 1 – in.
– Dùng KMnO4 nhận được stiren ở điều kiện thường, nhân được toluene khi đun nóng.
– Không có hiện tượng là benzen.
Bài 8: nhận biết các chất sau: benzen, toluen, stiren và phenol
Lời giải:
- Dùng dung dịch Br2: Có kết tủa trắng là phenol, chỉ mất màu nâu đỏ là stiren.
- Hai chất còn lại đun nóng với dung dịch KMnO4, màu tím nhạt dần là toluen. Không mất màu tím là benzen.
Bài 9: Hãy cho biết benzen và toluen đều có phản ứng với chất nào?
Lời giải:
Toluen và benzen cùng phản ứng hiđro có xúc tác Ni, đun nóng; Br2 có bột Fe đun nóng.
Bài 10: toluen là tên gọi của chất nào sau đây?
Lời giải:
Toluen, hay còn gọi là methylbenzen hay phenylmethan
Xem thêm các dạng bài tập Hóa học hay khác:
30 Bài tập về cách viết công thức cấu tạo (2024) có đáp án
30 Bài tập về hợp chất vô cơ (2024) có đáp án chi tiết nhất
30 Bài tập về hoá hợp (2024) có đáp án chi tiết nhất
30 Bài tập về phương trình hoá học (2024) có đáp án chi tiết nhất




