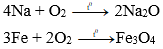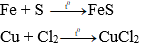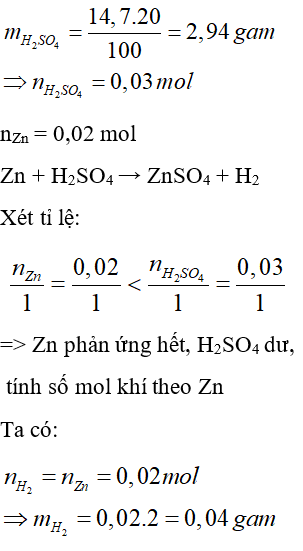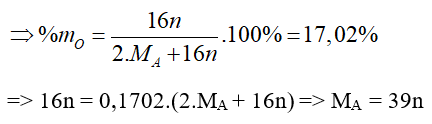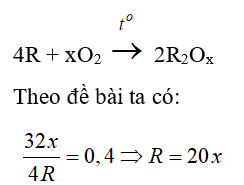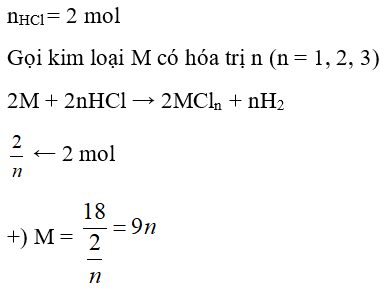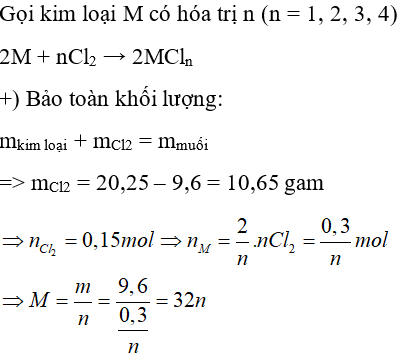Bài tập về Tính chất hóa học của kim loại
I. Lý thuyết và phương pháp giải
1. Tính chất vật lí
• Tính dẻo
- Kim loại có tính dẻo.
- Các kim loại khác nhau có tính dẻo khác nhau.Do có tính dẻo nên kim loại được rèn, kéo sợi, dát mỏng tạo nên các đồ vật khác nhau.
• Tính dẫn điện
- Kim loại có tính dẫn điện.
- Các kim loại khác nhau có khả năng dẫn điện khác nhau. Kim loại có khả năng dẫn điện tốt nhất là Ag, sau đó đến Cu, Al, Fe,...Do có tính dẫn điện, một số kim loại được sử dụng làm dây dẫn điện. Thí dụ như: đồng, nhôm, ...
- Chú ý: Không nên sử dụng dây dẫn điện trần hoặc dây điện đã bị hỏng lớp bọc cách điện để tránh bị điện giật, hay cháy do chập điện,...
• Tính dẫn nhiệt
- Kim loại có tính dẫn nhiệt .
- Kim loại khác nhau có tính dẫn nhiệt khác nhau. Kim loại nào dẫn điện tốt cũng thường dẫn nhiệt tốt.
- Dó có tính dẫn nhiệt và một số tính chất khác, nhôm, thép không gỉ (inox) được dùng để làm dụng cụ nấu ăn.
• Ánh kim
- Kim loại có ánh kim.Nhờ tính chất này, một số kim loại được dùng làm đồ trang sức và các vật dụng trang trí khác.
2. Tính chất hóa học
a) Tác dụng với oxi:
Hầu hết kim loại (trừ Au, Pt, Ag,..) tác dụng với oxi ở nhiệt độ thường hoặc nhiệt độ cao, tạo thành oxit.
Ví dụ:
b) Tác dụng với phi kim khác (Cl2, S, ...):
Nhiều kim loại tác dụng với nhiều phi kim, tạo thành muối.
Ví dụ:
c) Tác dụng với dung dịch axit
Nhiều kim loại tác dụng với dung dịch axit (HCl, H2SO4 loãng...) tạo thành muối và H2.
Ví dụ:
Fe + 2HCl → FeCl2 + H2
2Al + 3H2SO4 (loãng) → Al2(SO4)3 + 3H2
d) Tác dụng với dung dịch muối
Kim loại hoạt động mạnh hơn (trừ các kim loại phản ứng với nước như Na, K, Ba, Ca...) tác dụng với muối của kim loại yếu hơn, tạo thành muối mới và kim loại mới.
Ví dụ:
Fe + CuSO4 → FeSO4 + Cu
Mg + FeCl2 → MgCl2 + Fe
3. Phương pháp giải bài tập
+ Bước 1: Tính số mol các chất đề bài đã cho số liệu và viết phương trình phản ứng hóa học xảy ra.
+ Bước 2: Tính toán luôn theo phương trình phản ứng hóa học hoặc đặt ẩn nếu đề bài là hỗn hợp.
+ Bước 3: Lập phương trình toán học và giải phương trình Số mol các chất cần tìm.
+ Bước 4: Tính toán theo yêu cầu đề bài.
Lưu ý: Trong một hỗn hợp mà có nhiều phản ứng xảy ra thì phản ứng trung hoà được ưu tiên xảy ra trước.
II. Ví dụ minh họa
Ví dụ 1: Cho 1,3 gam kẽm phản ứng với 14,7 gam dung dịch H2SO4 20%. Khi phản ứng kết thúc khối lượng khí thoát ra là:
A. 0,03 gam
B. 0,06 gam
C. 0,04 gam
D. 0,02 gam
Đáp án: C
Ví dụ 2: Hòa tan 5,6 gam Fe bằng 250ml dung dịch HCl 1M, sau phản ứng thu được dung dịch X có chứa chất tan T. Chất T có khả thể tác dụng với Na2CO3 tạo khí. Coi thể tích dung dịch thay đổi không đáng kể. Nồng độ mol của T là:
A. 0,2M.
B. 0,4M.
C. 0,6M.
D. 0,8M.
Đáp án: A
Ví dụ 3: Cho 1,35g Al vào dung dịch chứa 7,3g HCl. Khối lượng muối nhôm tạo thành là
A. 6,675 g
B. 8,945 g
C. 2,43 g
D. 8,65 g
Đáp án: A
III. Bài tập tự luyện
Bài 1: Thả một mảnh nhôm vào ống nghiệm chứa dung dịch CuSO4. Xảy ra hiện tượng:
A. Không có dấu hiệu phản ứng.
B. Có chất rắn màu trắng bám ngoài lá nhôm, màu xanh của dung dịch CuSO4 nhạt dần.
C. Có chất rắn màu đỏ bám ngoài lá nhôm, màu xanh của dung dịch CuSO4 nhạt dần.
D. Có chất khí bay ra, dung dịch không đổi mà
Lời giải
Nhôm đứng trước đồng trong dãy điện hóa do đó sẽ đẩy đồng ra khỏi muối
2CuSO4 + 2Al → 3Cu↓ + Al2(SO4)3
Đáp án: C
Bài 2: Axit H2SO4 loãng phản ứng với tất cả các chất trong dãy nào dưới đây?
A. FeCl3, MgO, Cu, Ca(OH)2
B. NaOH, CuO, Ag, Zn
C. Mg(OH)2, CaO, K2SO3, SO2
D. Al, Al2O3, Fe(OH)3, BaCl2
Lời giải
Axit H2SO4 loãng phản ứng được với: Al, Al2O3, Fe(OH)3, BaCl2
Loại A vì Cu không phản ứng
Loại B vì Ag không phản ứng
Loại C vì SO2 không phản ứng
Đáp án: D
Bài 3: Chất nào sau đây không phản ứng với dung dịch HCl
A. Fe
B. Fe2O3
C. SO2
D. Mg(OH)2.
Lời giải
SO2 là oxit axit nên không phản ứng được với HCl
Đáp án: C
Bài 4: Axit sunfuric loãng tác dụng được với dãy chất nào sau đây?
A. Zn, CO2, NaOH
B. Zn, Cu, CaO
C. Zn, H2O, SO3
D. Zn, NaOH, Na2O
Lời giải
H2SO4 loãng tác dụng được với oxit bazơ, bazơ, kim loại đứng trước H, muối
A. Loại CO2
B. Loại Cu
C. Loại H2O, SO3
D. Thỏa mãn
Đáp án cần chọn là: D
Bài 5: Cho các kim loại Fe, Cu, Ag, Al, Mg. Trong các kết luận sau đây, kết luận nào sai ?
A. Kim loại tác dụng với dung dịch HCl, H2SO4 loãng: Cu, Ag
B. Kim loại tác dụng với dung dịch CuSO4 : Fe, Al, Mg
C. Kim loại không tác dụng với H2SO4 đặc nguội: Al, Fe
D. Kim loại không tan trong nước ở nhiệt độ thường: Tất cả các kim loại trên
Lời giải
Kết luận sai là: Kim loại tác dụng với dung dịch HCl, H2SO4 loãng: Cu, Ag
Đáp án: A
Bài 6: Để tách riêng các chất khỏi hỗn hợp gồm Fe, Cu, Al cần phải dùng hóa chất nào sau đây là thích hợp nhất?
A. HCl và HNO3
B. NaOH và HCl
C. HCl và CuCl2
D. H2O và H2SO4
Lời giải
Để tách riêng các chất khỏi hỗn hợp gồm Fe, Cu, Al cần phải dung : NaOH và HCl vì
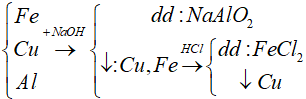
Đáp án: B
Bài 7: Tính chất hóa học chung của kim loại gồm:
A. Tác dụng với phi kim, tác dụng với axit.
B. Tác dụng với phi kim, tác dụng với bazơ, tác dụng với muối.
C. Tác dụng với phi kim, tác dụng với axit, tác dụng với muối.
D. Tác dụng với oxit bazơ, tác dụng với axit.
Lời giải
Tính chất hóa học chung của kim loại gồm: tác dụng với phi kim, tác dụng với axit, tác dụng với muối.
Đáp án: C
Bài 8: Phương pháp nhiệt luyện dùng để điều chế
A. Các kim loại hoạt động mạnh như Ca, Na, Al
B. Các kim loại hoạt động yếu
C. Các kim loại hoạt động trung bình
D. Các kim loại hoạt động trung bình và yếu
Lời giải
Phương pháp nhiệt luyện dùng để điều chế các kim loại hoạt động trung bình
Đáp án: C
Bài 9: Kim loại nhôm bị hòa tan bởi H2SO4 loãng, thu được muối sunfat và khí hiđro. Phản ứng mô tả hiện tượng trên là
A. 2Al + H2SO4 → Al2(SO4)3 + H2
B. 2Al + H2SO4 → Al2SO4 + H2
C. Al + 3H2SO4 → Al(SO4)3 + H2
D. 2Al + 3H2SO4 → Al2(SO4)3 + 3H2
Lời giải
Phản ứng đúng là: 2Al + 3H2SO4 → Al2(SO4)3 + 3H2
Đáp án: D
Bài 10: Ngâm một viên kẽm sạch trong dd CuSO4. Câu trả lời nào sau đây là đúng nhất cho hiện tượng quan sát được?
A. Không có hiện tượng nào xảy ra.
B. Một phần viên kẽm bị hòa tan, có một lớp màu đỏ bám ngoài viên kẽm và màu xanh lam của dung dịch nhạt dần.
C. Không có chất mới nào sinh ra, chỉ có một phần viên kẽm bị hòa tan.
D. Kim loại đồng màu đỏ bám ngoài viên kẽm, viên kẽm không bị hòa tan.
Lời giải
Kẽm đứng trước Cu trong dãy điện hóa do đó đẩy được đồng ra khỏi dung dịch muối
Zn + CuSO4 → Cu + ZnSO4
Đáp án: B
Câu 11: Cho phản ứng: Zn + CuSO4 → muối X + kim loại Y. X là
A. ZnSO4
B. CuSO4
C. Cu
D. Zn
Zn + CuSO4 → ZnSO4 + Cu
⇒ muối X là ZnSO4
Đáp án: A
Câu 12: Nhúng một thanh sắt vào dung dịch đồng (II) sunfat. Phản ứng hóa học xảy ra là:
A. Fe + CuSO4 → FeSO4 + Cu.
B. Fe + Cu2SO4 → FeSO4 + 2Cu.
C. 2Fe + 3CuSO4 → Fe2(SO4)3 + 3Cu.
D. 2Fe + 3CuSO4 → Fe2(SO4)3 + 6Cu.
Phản ứng hóa học xảy ra là:
Fe + CuSO4 → FeSO4 + Cu.↓
Đáp án: A
Câu 13: Cho sơ đồ phản ứng sau: A + NaOH → NaAlO2 + H2O. A là chất nào trong số các chất sau:
A. Al
B. Al2O3
C. Al(OH)3
D. Cả B và C đều đúng
Al2O3+ 2NaOH →2 NaAlO2 + H2O
Hoặc Al(OH)3+ NaOH → NaAlO2 + 2H2O
Đáp án: D
Câu 14: Một bạn học sinh đã đổ nhầm dung dịch sắt (II) sunfat vào lọ chứa sẵn dung dịch kẽm sunfat. Để thu được dung dịch chứa duy nhất muối kẽm sunfat, theo em dùng kim loại nào ?
A. Đồng
B. Sắt
C. Kẽm
D. Nhôm
Để thu được dung dịch chứa duy nhất muối ZnSO4 thì cần loại bỏ được dung dịch FeSO4 và không tạo ra muối nào khác
⇒ kim loại sử dụng được là Zn
PTHH: Zn + FeSO4 → ZnSO4 + Fe
Đáp án: C
Câu 15: Dung dịch muối ZnSO4 có lẫn một ít tạp chất là CuSO4. Dùng kim loại nào sau đây để làm sạch dung dịch ZnSO4 nêu trên là dễ dàng nhất?
A. Fe.
B. Zn.
C. Cu.
D. Mg.
Ta dùng kim loại Zn để làm sạch
Zn + CuSO4 → ZnSO4 + Cu↓
Đáp án: B
Câu 16: Trong hợp chất oxit của kim loại A thì oxi chiếm 17,02% theo khối lượng. Kim loại A là:
A. Cu
B. Zn
C. K
D. Na
Giả sử kim loại A có hóa trị n (n = 1, 2, 3, 4)
⇒ công thức oxit của kim loại A là A2On
Trong hợp chất oxit của kim loại A thì oxi chiếm 17,02% theo khối lượng
Ta có bảng sau:
| n | 1 | 2 | 3 | 4 |
| MA | 39 (Kali) | 78 (loại) | 117 (loại) | 156 (loại) |
Vậy A là Kali
Đáp án: C
Câu 17: Để oxi hóa hoàn toàn một kim loại R thành oxit phải dùng một lượng oxi bằng 40% lượng kim loại đã dùng. R là kim loại nào sau đây ?
A. Fe
B. Al
C. Mg
D. Ca
Gọi nguyên tử khối của kim loại R là R và có hóa trị là x (x = 1, 2, 3, 4)
Ta có bảng sau:
| x | 1 | 2 | 3 |
| R | 20 (loại) | 40 (canxi) | 60 (loại) |
Vậy R là Canxi
Đáp án: D
Câu 18: Hòa tan 5,1g oxit của một kim loại hóa trị III bằng dung dịch HCl, số mol axit cần dùng là 0,3 mol. Công thức phân tử của oxit đó là :
A. Fe2O3
B. Al2O3
C. Cr2O3
D. FeO
Gọi công thức của oxit là A2O3
Ta có A2O3 + 6HCl → 2ACl3 + 3H2O
Từ pthh ta có nA2O3 = 1/6 nHCl = 1/6 . 0,3 = 0,05 mol
⇒ MA2O3 = mA2O3 : nA2O3 = 5,1 : 0,05 = 102
MA2O3 = 2 . MA + 3 . 16 = 2MA + 48 = 102
⇒ MA = 27 ⇒ A là nhôm
Đáp án: B
Câu 19: Hòa tan hoàn toàn 18 gam một kim loại M cần dùng 800 ml dung dịch HCl 2,5M. Kim loại M là kim loại nào sau đây? (biết hóa trị của kim loại trong khoảng từ I đến III).
A. Ca
B. Mg
C. Al
D. Fe
Ta có bảng sau:
| n | 1 | 2 | 3 |
| M | 9 (loại) | 18 (loại) | 27 (Al) |
Đáp án: C
Câu 20: Cho 17g oxit M2O3 tác dụng hết với dung dịch H2SO4 thu được 57g muối sunfat. Nguyên tử khối của M là:
A. 56
B. 52
C. 55
D. 27
Đáp án: D
Câu 21: Đốt cháy hoàn toàn 9,6 gam một kim loại M (chưa rõ hóa trị) trong bình chứa khí clo nguyên chất. Sau khi phản ứng kết thúc, để nguội thì thu được 20,25 gam muối clorua. Kim loại M là
A. Fe
B. Al
C. Cu
D. Zn
Ta có bảng sau:
| n | 1 | 2 | 3 | 4 |
| M | 32 (loại) | 64 (Cu) | 96 (loại) | 128 (loại) |
Vậy M là kim loại Cu
Đáp án: C
Câu 22: Cho 10,8 g một kim loại M (hóa trị III) phản ứng với khí clo tạo thành 53,4g muối. Kim loại M là:
A. Na
B. Fe
C. Al
D. Mg
2M + 3Cl2 → 2MCl3 (1)
Áp dụng định luật bảo toàn khối lượng ta có
mCl2 + mM = mMCl3
⇒ mCl2 = mMCl3 – mCl2 = 53,4 – 10,8 = 42,6g
⇒ nCl2 = mCl2 : MCl2 = 42,6 : 71 = 0,6 mol
Từ pt (1) ta có nM= 2/3 . nCl2 = 2/3 . 0,6 = 0,4 mol
⇒ MM = mM : nM = 10,8 : 0,4 = 27g/mol
⇒ M là nhôm
Đáp án: C
Xem thêm các dạng câu hỏi và bài tập liên quan khác:
30 Bài tập về Tính chất vật lí của kim loại (2024) có đáp án chi tiết nhất
30 Bài tập về Nhôm (2024) có đáp án chi tiết nhất
30 Bài tập về Hợp kim sắt: Gang, thép (2024) có đáp án chi tiết nhất
30 Bài tập về Sự ăn mòn kim loại và bảo vệ kim loại không bị ăn mòn (2024) có đáp án chi tiết nhất
30 Bài tập của Dãy hoạt động hóa học của kim loại (2024) có đáp án chi tiết nhất