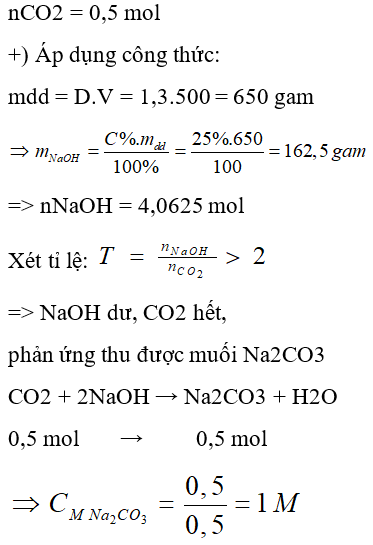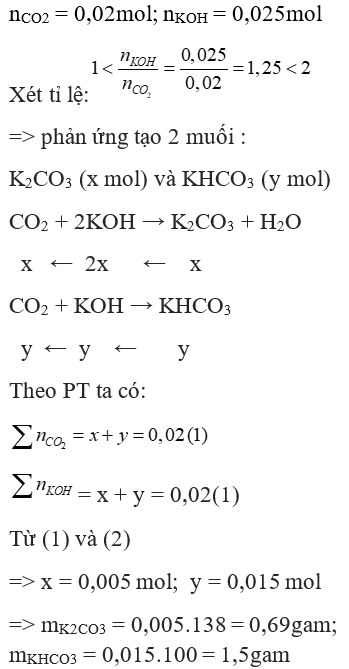Bài tập về Tính chất hóa học của axit
I. Lý thuyết và phương pháp giải
1. Tính chất hóa học của axit
a. Axit làm đổi màu chất chỉ thị
Dd axit làm quỳ tìm chuyển màu đỏ.
b. Axit + kim loại à muối + H2
3H2SO4 +2Al Al2(SO4)3 + 3H2
Zn +2HCl ZnCl2 +H2
Cu + HCl k pư
Cu + H2SO4 k pư
c. Axit + bazo à muối + nước
H2SO4 + 2 NaOH Na2SO4 + H2O
H2SO4 + Cu(OH)2 CuSO4 + H2O
(Dd màu xanh lam)
HCl + NaOH NaCl + H2O
Chú ý: pư giữa axit và bazo là pư trung hòa.
d. Axit + oxit bazo à muối + nước
Fe2O3 + 6HCl 2FeCl3 + 3H2O
( dd màu vàng nâu)
CuO + 2HCl CuCl2 + H2O
e. Axit + muối à axit mới + muối mới
BaCl2 + H2SO4 BaSO4 + 2HCl
2. Phân loại axit
- axit mạnh : HCl, HNO3, H2SO4,
- axit yếu : H2S, H2CO3,..
3. Một số axit quan trọng
|
|
HCl |
H2SO4 loãng |
|
|
Giống nhau |
- làm đổi màu quỳ tím - tác dụng với KL tạo muối và giải phóng H2 Fe + 2HCl FeCl2 + H2 Zn + H2SO4 ZnSO4 +H2 - tác dụng với bazo tạo muối + nước 2HCl + Cu(OH)2 CuCl2 +2H2O H2SO4 + Cu(OH)2 CuSO4 + 2H2O - tác dụng với oxit bazo tạo muối + nước 2HCL + CuO CuCl2 + H2O H2SO4 + CuO CuSO4 + H2O - tác dụng với muối tạo ra axit mới và muối mới. |
||
|
Khác nhau
|
Tính chất của H2SO4 đặc. - tác dụng với kim loại tạo muối sunfat và không giải phóng H2. Cu + 2H2SO4đặc, nóng CuSO4 +2H2O + SO2 - tính háo nước: H2SO4 đ C12H22O11 --------- > 11H2O + 12C C + 2H2SO4 đ CO2 + 2H2O + 2SO2 Htg: đường từ màu trắng chuyển sang màu vàng, sau đó chuyển sang nâu và cuối cùng thành khối đen xốp bị bọt khí đẩy lên khỏi miệng cốc. |
||
|
Ứng dụng |
- điều chế muối clorua. - làm sạch bề mặt kim loại trước khi hàn. - tẩy rủ kim loại trước khi sơn, tráng, mạ kim loại. - chế biến thực phẩm, dược phẩm,.. |
||
 |
|||
4. Phương pháp giải bài tập
+ Bước 1: Tính số mol các chất đề bài đã cho số liệu và viết phương trình phản ứng hóa học xảy ra.
+ Bước 2: Tính toán luôn theo phương trình phản ứng hóa học hoặc đặt ẩn nếu đề bài là hỗn hợp.
+ Bước 3: Lập phương trình toán học và giải phương trình Số mol các chất cần tìm.
+ Bước 4: Tính toán theo yêu cầu đề bài.
Lưu ý: Trong một hỗn hợp mà có nhiều phản ứng xảy ra thì phản ứng trung hoà được ưu tiên xảy ra trước.
II. Ví dụ minh họa
Ví dụ 1: Cho 11,2 lít CO2 vào 500 ml dung dịch NaOH 25% (D = 1,3 g/ml). Nồng độ mol/lit của dung dịch muối tạo thành là
A. 1M
B. 2M
C. 2,5M
D. 1,5M
Đáp án: A
Ví dụ 2: Dẫn 448 ml CO2 (đktc) sục vào bình chứa 100 ml dung dịch KOH 0,25M. Khối lượng hai muối tạo thành là
A. 0,85 gam và 1,5 gam.
B. 0,69 gam và 1,7 gam.
C. 0,85 gam và 1,7 gam.
D. 0,69 gam và 1,5 gam
Đáp án: D
Ví dụ 3: Dẫn 22,4 lít khí CO2 ( đktc) vào 200g dung dịch NaOH 20%. Sau phản ứng tạo ra sản phẩm nào trong số các sản phẩm sau:
A. Muối natricacbonat và nước.
B. Muối natri hidrocacbonat.
C. Muối natricacbonat.
D. Muối natrihiđrocacbonat và natricacbonat.
mchất tan NaOH = (mdd . C%):100% = 200 . 20%:100% = 40g
Đáp án: B
III. Bài tập tự luyện
Bài 1: Axit H2SO4 loãng không tác dụng với kim loại nào sau đây:
A. Al
B. Fe
C. Mg
D. Ag
Lời giải
Kim loại đứng sau H trong dãy điện hóa học của kim loại không tác dụng được với H2SO4 loãng.
Ag đứng sau H => Không phản ứng
Đáp án: D
Bài 2: Kim loại nào sau đây không tác dụng được với dung dịch axit H2SO4 loãng?
A. Fe
B. Al
C. Cu
D. Na
Lời giải
Fe, Al, Na tác dụng với dung dịch axit H2SO4 loãng
Cu không tác dụng với dd axit H2SO4 loãng
Đáp án: C
Bài 3: Dãy gồm các oxit tác dụng được với nước tạo thành dung dịch axit là:
A. CO, CO2, SO2
B. P2O5, NO, SO2
C. P2O5, SO2, CO2
D. NO, SO2, CO
Lời giải
A sai do CO không tác dụng với nước
B sai do NO không tác dụng với nước
C đúng
D sai do NO và CO không tác dụng với nước
Đáp án: C
Bài 4: Chất nào sau đây tác dụng với axit HCl tạo kết tủa trắng?
A. Ba(OH)2
B. Ca(NO3)2
C. AgNO3
D. MgSO4
Lời giải
Chất kết tủa có chứa gốc Cl là AgCl và PbCl2
Chất tạo kết tủa trắng với HCl là AgNO3
PTHH: AgNO3 + HCl → AgCl↓trắng + HNO3
Đáp án: C
Bài 5: Nhóm chất tác dụng với dung dịch H2SO4 loãng sinh ra chất kết tủa màu trắng:
A. ZnO, BaCl2
B. CuO, BaCl2
C. BaCl2, Ba(NO3)2
D. Ba(OH)2, ZnO
Lời giải
A ZnSO4 tan không có kết tủa
B CuSO4 cũng tan
D ZnSO4 tan
C kết tủa BaSO4 màu trắng
Đáp án: C
Bài 6: Tính chất hóa học nào không phải của axit?
A. Tác dụng với kim loại.
B. Tác dụng với muối.
C. Tác dụng với oxit axit.
D. Tác dụng với oxit bazơ.
Lời giải
Tính chất hóa học không phải của axit là: Tác dụng với oxit axit.
Axit không phản ứng với oxit axit
Đáp án: C
Bài 7: Chất nào sau đây tác dụng với Fe ở nhiệt độ thường tạo ra khí hiđro là
A. O2
B. HCl
C. CO2
D. H2O
Lời giải
Axit tác dụng với kim loại tạo muối và giải phóng khí hiđro
Fe + 2HCl → FeCl2 + H2
Đáp án: B
Bài 8: Hãy cho biết muối nào có thể điều chế bằng phản ứng của kim loại với dung dịch Axit H2SO4 loãng ?
A. ZnSO4
B. Na2SO3
C. CuSO4
D. MgSO3
Lời giải
A. Thỏa mãn: Zn + H2SO4 → ZnSO4 + H2↑
B,D loại vì không phải muối sunfat
C. Loại vì Cu không phản ứng với dd H2SO4
Đáp án: A
Bài 9: Hiện tượng quan sát được khi cho mẩu magie vào ống nghiệm chứa axit HCl dư là:
A. Mẩu Mg tan dần, không có bọt khí thoát ra
B. Mẩu Mg tan dần, có bọt khí thoát ra, dung dịch thu được không màu
C. Mẩu Mg tan dần, có bọt khí thoát ra, dung dịch thu được có màu xanh lam
D. Không xảy ra hiện tượng gì
Lời giải
Khi cho mẩu magie vào ống nghiệm chứa axit HCl dư mẩu Mg tan dần, có bọt khí thoát ra, dung dịch thu được không màu : Mg + 2HCl → MgCl2 + H2
Dung dịch MgCl2 thu được không có màu
Đáp án: B
Bài 10: Các kim loại nào sau đây tác dụng được với dung dịch H2SO4 loãng?
A. Mg, Zn, Ag, Cu
B. Mg, Zn, Fe, Cu
C. Zn, Fe, Al, Mg
D. Al, Cu, Fe, Ag
Lời giải
Các kim loại tác dụng được với dung dịch H2SO4 loãng là: Zn, Fe, Al, Mg.
Axit không tác dụng với Cu, Ag và Au.
Đáp án: C
Bài 11: Dãy các chất có thể tác dụng với dung dịch HCl là:
A. Na, FeO, CuO
B. FeO, CuO, CO2
C. Fe, FeO, CO2
D. Na, FeO, CO2
Lời giải
Dãy các chất có thể tác dụng với dung dịch HCl là Na, FeO, CuO
B, C, D sai do có CO2 không tác dụng với HCl
Đáp án: A
Bài 12: Dung dịch A tác dụng với CuO tạo ra dung dịch có màu xanh lam. A là
A. NaOH
B. Na2CO3
C. H2SO4
D. Ca(OH)2
Lời giải
CuO là oxit bazơ => tan trong dung dịch axit H2SO4 tạo muối CuSO4 có màu xanh lam
CuO + H2SO4 → CuSO4 + H2O
Đáp án: C
Bài 13: Cặp chất tác dụng với nhau tạo thành sản phẩm có chất khí:
A. Bari oxit và axit sunfuric loãng
B. Bari hiđroxit và axit sunfuric loãng
C. Bari cacbonat và axit sunfuric loãng
D. Bari clorua và axit sunfuric loãng
Lời giải
PTHH: BaCO3 + H2SO4 → BaSO4↓ + H2O + CO2↑
Đáp án: C
Bài 14: Nhóm oxit vừa tác dụng với nước, vừa tác dụng với dung dịch HCl là
A. Na2O, SO3, CO2
B. K2O, P2O5, CaO
C. BaO, Al2O3, Na2O
D. CaO, BaO, K2O
Lời giải
Loại A vì SO3, CO2 không phản ứng với dung dịch HCl
Loại B vì P2O5 không phản ứng với dung dịch HCl
Loại C vì Al2O3 không tan trong nước
Đáp án: D
Bài 15: Axit HCl tác dụng được với oxit nào trong các oxit sau: Na2O; BaO; CuO; MgO; SO2; P2O5
A. Na2O; BaO; CuO; P2O5
B. BaO; CuO; MgO; SO2
C. Na2O; BaO; CuO; MgO
D. Na2O; BaO; MgO ;P2O5
Lời giải
Na2O; BaO; CuO; MgO là các oxit bazo nên pư với axit=> muối và nước
Đáp án: C
Câu 16: Cho 1,68 lít CO2 (đktc) sục vào bình đựng 250 ml dung dịch KOH dư. Biết thể tích dung dịch trước và sau phản ứng không thay đổi Nồng độ mol/lit của muối thu được sau phản ứng là
A. 0,2M
B. 0,3M
C. 0,4M
D. 0,5M
nCO2 = 0,075 mol
Vì KOH dư nên phản ứng tạo ra muối trung hòa
Đáp án: B
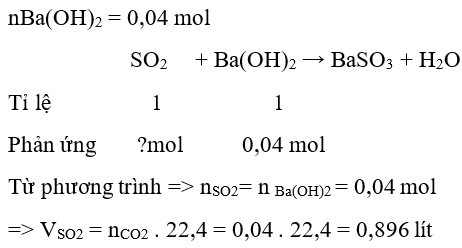
Câu 17: Dùng 400ml dung dịch Ba(OH)2 0,1M hấp thụ hoàn toàn V lít khí SO2 (đktc). Sau phản ứng thu được muối BaSO3 không tan. Giá trị bằng số của V là:
A. 0,896 lít
B. 0,448 lít
C. 8,960 lít
D. 4,480
Đáp án: A
Xem thêm các dạng câu hỏi và bài tập liên quan khác:
30 bài tập về Một số muối quan trọng (2024) có đáp án chi tiết nhất
30 Bài tập về Một số oxit quan trọng (2024) có đáp án chi tiết nhất
30 Bài tập về Mối quan hệ giữa các loại hợp chất vô cơ (2024) có đáp án chi tiết nhất
30 Bài tập về Axit cacbonic và muối cacbonat (2024) có đáp án chi tiết nhất
30 Bài tập về Một số axit quan trọng (2024) có đáp án chi tiết nhất