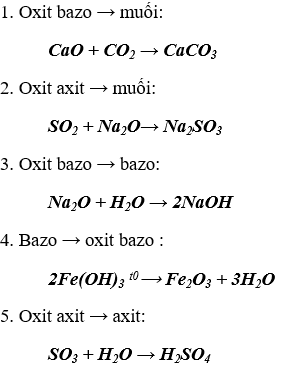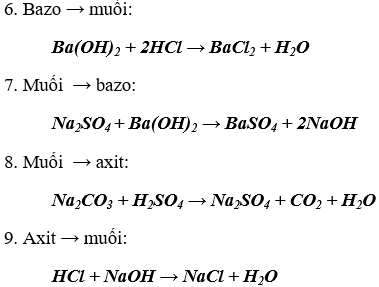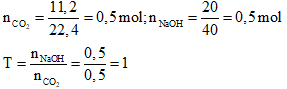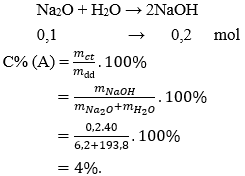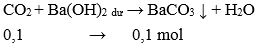Bài tập về Mối quan hệ giữa các loại hợp chất vô cơ
I. Lý thuyết và phương pháp giải
1. Sơ đồ hệ thống mối quan hệ giữa các hợp chất vô cơ
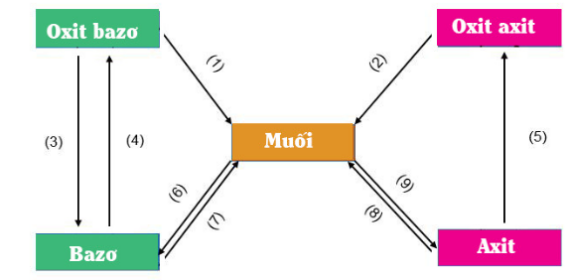
2. Phương trình hóa học minh họa cho mối quan hệ giữa các loại hợp chất vô cơ
3. Phương pháp giải bài tập
+ Bước 1: Tính số mol các chất đề bài đã cho số liệu và viết phương trình phản ứng hóa học xảy ra.
+ Bước 2: Tính toán luôn theo phương trình phản ứng hóa học hoặc đặt ẩn nếu đề bài là hỗn hợp.
+ Bước 3: Lập phương trình toán học và giải phương trình Số mol các chất cần tìm.
+ Bước 4: Tính toán theo yêu cầu đề bài.
Lưu ý: Trong một hỗn hợp mà có nhiều phản ứng xảy ra thì phản ứng trung hoà được ưu tiên xảy ra trước.
II. Ví dụ minh họa
Ví dụ 1: Phát biểu nào sau đây là đúng?
A. Tất cả các muối cabonat đều tan
B. Tất cả các muối của kim loại K, Na đều tan
C. Tất cả các muối của kim loại Cu, Ag đều tan
D. Tất cả các muối sunfat đều không tan
Đáp án: B
Ví dụ 2: Cho 40 gam Cu và ZnO tác dụng với dung dịch HCl loãng, dư, lọc lấy phần không tan cho tác dụng với H2SO4 đặc, nóng thì thu được 5,6 lít khí (đktc). Thành phần phần trăm khối lượng các chất trong hỗn hợp lần lượt là:
A. 30% và 70%
B. 60% và 40%
C. 70% và 30%
D. 40% và 60%
Đáp án: D
Ví dụ 3: Nếu chỉ dùng dung dịch KOh thì có thể phân biệt được hai chất trong mỗi cặp chất nào sau đây?
A. Dung dịch K2SO4 và dung dịch Fe2(SO4)3
B. Dung dịch K2SO4 và dung dịch K2CO3
C. Dung dịch K2SO4 và dung dịch BaCl2
D. Dung dịch K2SO4 và dung dịch KCl
Đáp án: A
Ví dụ 4: Cho 100ml dung dịch H2SO4 2M tác dụng với 100ml dung dịch Ba(NO3)2 1M. Nồng độ mol của các chất trong dung dịch sau phản ứng lần lượt là:
A. 2M và 1M
B. 1,5M và 0,5M
C. 1M và 2M
D. 1M và 0,5M
Đáp án: D
III. Bài tập tự luyện
Câu 1: Chất tác dụng với nước tạo ra dung dịch bazơ là:
A. K2O.
B. CuO.
C. CO.
D. SO2.
Đáp án: A
K2O + H2O → 2KOH.
Câu 2: Chất tác dụng với nước tạo ra dung dịch axit là:
A. CaO
B. BaO
C. Na2O
D. SO3.
Đáp án: D
SO3 + H2O → H2SO4.c
Câu 3: Dãy oxit tác dụng với nước tạo ra dung dịch kiềm:
A. CuO, CaO, K2O, Na2O.
B. CaO, Na2O, K2O, BaO.
C. Na2O, BaO, CuO, MnO.
D. MgO, Fe2O3, ZnO, PbO.
Đáp án: B.
Câu 4: Dãy oxit tác dụng với dung dịch NaOH:
A. CuO, Fe2O3, SO2, CO2.
B. CaO, CuO, CO, N2O5.
C. CO2, SO2, P2O5, SO3.
D. SO2, MgO, CuO, Ag2O.
Đáp án: C.
Oxit axit (CO2, SO2, P2O5, SO3) tác dụng được với dung dịch NaOH.
Câu 5: Dãy oxit vừa tác dụng với nước, vừa tác dụng với dung dịch axit là:
A. CuO, Fe2O3, SO2, CO2.
B. CaO, CuO, CO, N2O5.
C. CaO, Na2O, K2O, BaO.
D. SO2, MgO, CuO, Ag2O.
Đáp án: C.
Câu 6: Hấp thụ hoàn toàn 11,2 lít khí CO2 (đktc) bằng một dung dịch chứa 20 g NaOH. Muối được tạo thành là:
A. Na2CO3.
B. NaHCO3.
C. Hỗn hợp Na2CO3 và NaHCO3.
D. Na(HCO3)2.
Đáp án: B.
→ Sau phản ứng thu được muối NaHCO3.
Câu 7: Hoà tan 6,2 g natri oxit vào 193,8 g nước thì được dung dịch A. Nồng độ phần trăm của dung dịch A là:
A. 4%.
B. 6%.
C. 4,5%
D. 10%
Đáp án: A
Số mol Na2O = 6,2 : 62 = 0,1 mol
Câu 8: Oxit nào sau đây khi tác dụng với nước tạo ra dung dịch có pH > 7 ?
A. CO2
B. SO2
C. CaO
D. P2O5
Đáp án: C
CaO + H2O → Ca(OH)2
Dung dịch Ca(OH)2 có pH > 7.
Câu 9: Cho 2,24 lít CO2 (đktc) tác dụng với dung dịch Ba(OH)2 dư. Khối lượng chất kết tủa thu được là
A. 19,7 g
B. 19,5 g
C. 19,3 g
D. 19 g
Đáp án: A
Số mol CO2 = 2,24 : 22,4 = 0,1 mol
→ m↓ = 0,1.197 = 19,7 gam.
Câu 10: Dùng thuốc thử nào sau đây để phân biệt các chất chứa trong các ống nghiệm mất nhãn: HCl, KOH, NaNO3, Na2SO4.
A. Dùng quì tím và dung dịch CuSO4.
B. Dùng dung dịch phenolphtalein và dung dịch BaCl2.
C. Dùng quì tím và dung dịch BaCl2.
D. Dùng dung dịch phenolphtalein và dung dịch H2SO4.
Đáp án: C
- Sử dụng quỳ tím:
+ Quỳ tím chuyển sang màu đỏ → HCl.
+ Quỳ tím chuyển sang màu xanh → KOH.
+ Quỳ tím không chuyển màu → NaNO3 và Na2SO4.
- Phân biệt NaNO3 và Na2SO4: Dùng BaCl2
+ Xuất hiện kết tủa trắng → Na2SO4.
BaCl2 + Na2SO4 → BaSO4↓ + 2NaCl
+ Không hiện tượng → NaNO3.
Câu 11: Hiện tượng gì sẽ xảy ra khi cho dung dịch HCl vào ống nghiệm chứa KHCO3?
A. Có khí thoát ra và có kết tủa
B. Chỉ có kết tủa trắng
C. Có khí thoát ra và dung dịch trong suốt
D. Dung dịch có màu vàng
Đáp án: C
Câu 12: Điều kiện để muối phản ứng với muối là:
A. Hai muối tham gia phản ứng đều phải tan
B. Hai muối đem phản ứng phải có một muối không tan
C. Hai muối tham gia phản ứng đều phải tan, hai muối tạo thành ít nhất phải có một muối không tan
D. Hai muối tạo thành ít nhất phải có một muối không tan
Đáp án: C
Câu 13: Cho 30,4 gam oxit kim loại M vào 294 gam đung dịch H2SO$_{4}4 20% vừa đủ. Công thức hóa học của oxit trên là:
A. Al2O3
B. Fe2O3
C. Cr2O3
D. FeO
Đáp án: C
Câu 14: Cho a gam một bazo vào dung dịch HCl loãng dư, cô cạn dung dịch sau phản ứng thì thu được 3,25 gam muối clorua khan. Mặt khác, cũng đem nung nóng a gam lượng bazo trên đến khối lượng không đổi thì thu được 1,6 gam một oxit kim loại. Công thức phân tử của bazo là:
A. Fe(OH)3
B. Ba(OH)2
C. Zn(OH)2
D. Ni(OH)2
Đáp án: A
Câu 15: Trộn 13,44 gam dung dịch KOH 25% với 32,5 gam dung dịch FeCl3 20%. Sau phả ứng xảy ra hoàn toàn thu được khối lượng kết tủa là bao nhiêu ?
A. 3 gam
B. 3,14 gam
C. 4,14 gam
D. 2,14 gam
Đáp án: D
Câu 16: Hoà tan 50 g CaCO3 vào dung dịch axit clohiđric dư.Thể tích của khí CO2 (đktc) thu được là:
A. 11,2 lít.
B. 22,4 lít.
C. 8,96 lít.
D. 5,6 lít.
Đáp án: A
Xem thêm các dạng bài tập hay khác:
30 Bài tập Tính chất hóa học của muối (2024) có đáp án chi tiết nhất
30 Bài tập về Một số bazơ quan trọng (2024) có đáp án chi tiết nhất
30 Bài tập về Tính chất hóa học của axit (2024) có đáp án chi tiết nhất
30 Bài tập về Một số oxit quan trọng (2024) có đáp án chi tiết nhất