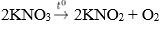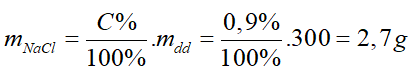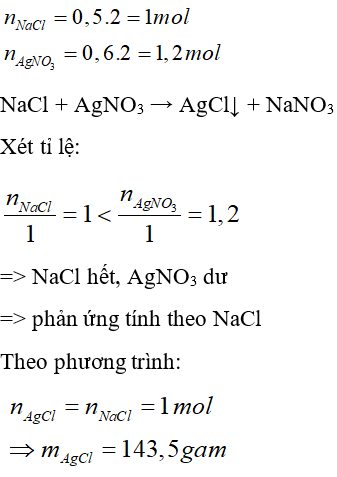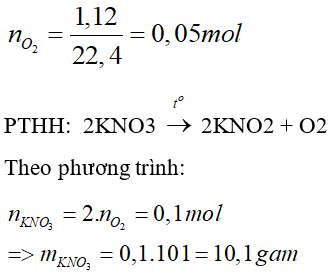Một số muối quan trọng
Lý thuyết
Muối Natri Clorua
1. Trạng thái tự nhiên
Natri clorua có trong nước biển. Cho nước biển bay hơi, ta được chất rắn là hỗn hợp của nhiều muối, thành phần chính là NaCl (trong 1m3 nước biển có hòa tan chừng 27 kg NaCl, 5kg MgCl2, 1kg CaSO4 và một khối lượng nhỏ những muối khác).
Ngoài ra, trong lòng đất cũng chứa một khối lượng muối natri clorua kết tinh gọi là muối mỏ. Những mỏ muối có nguồn gốc từ những hồ nước mặn đã cạn đi từ hàng triệu năm.
2. Cách khai thác
* Ở những nơi có biển hoặc hồ nước mặn, người ta khai thác NaCl từ nước mặn ở trên. Cho nước mặn bay hơi từ từ, thu được muối kết tinh.
* Ở những nơi có mỏ muối, người ta đào hầm hoặc giếng sâu đến mỏ muối để lấy muối lên. Muối mỏ sau khi khai thác, được nghiền nhỏ và tinh chế để có muối sạch.
3. Ứng dụng
Muối NaCl có rất nhiều ứng dụng trong đời sống và sản xuất, nó được dùng để:
- Làm gia vị và bảo quản thực phẩm. Muối iot là muối ăn NaCl có trộn thêm một ít KIO3 + KI.
- Làm nguyên liệu để sản xuất: Na, NaOH, H2, Cl2, Na2CO3, nước gia – ven, …
Kali Nitrat
KNO3 còn có tên gọi khác là diêm tiêu.
1. Tính chất
KNO3 là chất rắn, màu trắng, tan nhiều trong nước, khi tan thu nhiệt.
KNO3 bị nhiệt phân hủy:
2. Ứng dụng:
KNO3 dùng chế tạo thuốc nổ đen, làm phân bón, bảo quản thực phẩm trong công nghiệp.
Bài tập tự luyện
Bài 1: Chất nào trong những thuốc thử sau đây có thể phân biệt dung dịch Na2SO4 và dung dịch Na2CO3:
A. dd HCl
B. dd Pb(NO3)2
C. dd BaCl2
D. dd NaOH
Lời giải
Nhỏ HCl vào ống nghiệm chứa Na2SO4 và Na2CO3
+ Na2SO4 không có hiện tượng
+ Na2CO3 có xuất hiện sủi bọt khí
Na2CO3 + HCl → NaCl + CO2↑ + H2O
Đáp án: A
Bài 2: Trộn những cặp chất nào sau đây ta thu được NaCl ?
A. dung dịch Na2CO3 và dung dịch BaCl2
B. dung dịch NaNO3 và CaCl2
C. dung dịch KCl và dung dịch NaNO3
D. dung dịch Na2SO4 và dung dịch KCl
Lời giải
Thu được NaCl bằng cách trộn dung dich Na2CO3 và dung dịch BaCl2 vì xảy ra phản ứng:
Na2CO3 + BaCl2 → BaCO3 ↓ + 2NaCl
Đáp án: A
Bài 3: Hai dung dịch tác dụng với nhau, sản phẩm thu được có NaCl. Hãy cho biết hai cặp dung dịch các chất đã dùng ban đầu là
A. BaCl2 và NaOH
B. MgCl2 và NaOH
C. Na2SO4 và HCl
D. NaNO3 và KCl
Lời giải
Để thu được sản phẩm là NaCl => 2 chất ban đầu tác dụng với nhau, ngoài sản phẩm là NaCl thì chất còn lại là kết tủa hoặc chất khí hoặc H2O
=> 2 chất là MgCl2 và NaOH
PTHH: MgCl2 + 2NaOH → Mg(OH)2 + 2NaCl
Đáp án: B
Bài 4: Điện phân dung dịch NaCl bão hoà, có màng ngăn giữa hai điện cực, sản phẩm thu được là:
A. NaOH, H2, Cl2
B. NaCl, NaClO, H2, Cl2
C. NaCl, NaClO, Cl2
D. NaClO, H2 và Cl2
Lời giải
PT điện phân: 2NaCl + 2H2O 2NaOH + H2 + Cl2
Đáp án: A
Bài 5: Điện phân dung dịch natri clorua (NaCl) bão hoà trong bình điện phân có màng ngăn ta thu được hỗn hợp khí là:
A. H2 và O2
B. H2 và Cl2
C. O2 và Cl2
D. Cl2 và HCl
Lời giải
2H2O + 2NaCl Cl2 + H2 + NaOH
Đáp án: B
Bài 6: Trong tự nhiên muối natri clorua có nhiều trong:
A. Nước biển
B. Nước mưa
C. Nước sông
D. Nước giếng.
Lời giải
Trong tự nhiên muối natri clorua có nhiều trong: nước biển
Đáp án: A
Bài 7: Có những muối sau: CaCO3, CaSO4, Pb(NO3)2, NaCl. Muối nào nói trên:
A. CaCO3
B. CaSO4
C. Pb(NO3)2
D. NaCl
Lời giải
Muối không được phép có trong nước ăn vì tính độc hại của nó là Pb(NO3)2.
Đáp án: C
Bài 8: Nung kali nitrat (KNO3) ở nhiệt độ cao, ta thu được chất khí là:
A. NO
B. N2O
C. N2O5
D. O2
Lời giải
KNO3 bị nhiệt phân: 2KNO32KNO2 + O2
=> chất khí thu được là O2
Đáp án: D
Bài 9: Muối kali nitrat (KNO3):
A. không tan trong trong nước
B. tan rất ít trong nước
C. tan nhiều trong nước
D. không bị phân huỷ ở nhiệt độ cao
Lời giải
Muối kali nitrat (KNO3) là chất rắn, tan nhiều trong nước, khi tan thu nhiệt.
Đáp án: C
Bài 10: Để làm sạch dung dịch NaCl có lẫn Na2SO4 ta dùng:
A. Dung dịch AgNO3
B. Dung dịch HCl
C. Dung dịch BaCl2
D. Dung dịch Pb(NO3)2
Lời giải
Để làm sạch dung dịch NaCl có lẫn Na2SO4 ta dùng dung dịch BaCl2 vì tạo kết tủa với Na2SO4 và chỉ còn lại dung dịch NaCl
Na2SO4 + BaCl2 → BaSO4 + 2NaCl
Đáp án: C
Bài 11: Trường hợp nào tạo ra chất kết tủa khi trộn hai dung dịch sau ?
A. NaCl và AgNO3
B. NaCl và Ba(NO3)2
C. KNO3 và BaCl2
D. CaCl2 và NaNO3
Lời giải
Trường hợp tạo ra chất kết tủa là : NaCl phản ứng với AgNO3
NaCl + AgNO3 → AgCl↓ + NaNO3
Đáp án: A
Bài 12: Cho phương trình phản ứng: Na2CO3 + 2HCl → 2NaCl + X + H2O. X là:
A. CO
B. CO2
C. H2
D. Cl2
Lời giải
PTHH: Na2CO3 + 2HCl → 2NaCl + CO2 ↑ + H2O
=> khí X là CO2
Đáp án: B
Bài 13: Hoà tan 50 gam muối ăn vào 200 gam nước thu được dung dịch có nồng độ là:
A. 15%
B. 20%
C. 18%
D. 25%
Lời giải
Đáp án: B
Bài 14: Để có được dung dịch NaCl 32%, thì khối lượng NaCl cần lấy hoà tan vào 200 gam nước là:
A. 90 gam
B. 94,12 gam
C. 100 gam
D. 141,18 gam
Lời giải
Gọi khối lượng NaCl cần dùng là m (gam)
=> mdungdịch = mNaCl + mH2O = m + 200
Đáp án: B
Bài 15: Súc miệng bằng dung dịch nước muối 0,9% có tác dụng bảo vệ niêm mạc và sát khuẩn. Số gam NaCl cần lấy để pha 300 gam dung dịch nước muối 0,9% là:
A. 5,4g
B. 0,9g
C. 0,27g
D. 2,7g
Lời giải
Đáp án: D
Câu 16: Hoà tan 10,95 gam KNO3 vào 150 gam nước thì được dung dịch bão hoà ở 200C, độ tan của KNO3 ở nhiệt độ này là
A. 6,3 gam
B. 7,0 gam
C. 7,3 gam
D. 7,5 gam
Lời giải
- Độ tan (S) của một chất trong nước là số gam chất đó hòa tan trong 100 gam nước để tạo thành dung dịch bão hòa ở một nhiệt độ xác định.
150 gam nước hòa tan được 10,95 gam KNO3
100 gam nước hòa tan được S gam KNO3
Đáp án: C
Câu 17: Khi làm nguội 1026,4 gam dung dịch bão hòa R2SO4. nH2O (trong đó R là kim loại kiềm và n nguyên, thỏa mãn điều kiện 7 < n < 12) từ 800C xuống 100C thì có 395,4 gam tinh thể R2SO4. nH2O tách ra khỏi dung dịch. Biết độ tan của R2SO4 ở 800C và 100C lần lượt là 28,3 gam và 9 gam. Công thức phân tử của hiđrat nói trên là:
A. Cu
B. Na
C. Al
D. K
Lời giải
Đáp án: B
Câu 18: Cho 500 ml dung dịch NaCl 2M tác dụng với 600 ml dung dịch AgNO3 2M. Khối lượng kết tủa thu được là
A. 143,5 gam
B. 14,35 gam
C. 157,85 gam
D. 15,785 gam
Lời giải
Đáp án: A
Câu 19: Trong phòng thí nghiệm, người ta thường dùng muối KNO3 để điều chế khí oxi bằng phản ứng phân hủy. Để điều chế 1,12 lít khí O2 (đktc) thì khối lượng muối cần dùng là
A. 20,2 gam.
B. 10,1 gam.
C. 5,05 gam.
D. 7,07 gam
Lời giải
Đáp án: B
Câu 20: Có thể phân biệt BaCl2 và NaCl bằng dung dịch:
A. H2SO4.
B. KOH.
C. NaOH.
D. KNO3.
Lời giải
Dùng H2SO4 để phân biệt BaCl2 và NaCl
+ BaCl2 tạo kết tủa trắng, còn NaCl thì không có hiện tượng gì
H2SO4 + BaCl2 → BaSO4↓ trắng + 2HCl
Đáp án: A
Xem thêm các dạng bài tập hay khác:
30 Bài tập về Axit cacbonic và muối cacbonat (2024) có đáp án chi tiết nhất
30 Bài tập Tính chất hóa học của muối (2024) có đáp án chi tiết nhất
30 Bài tập về Một số bazơ quan trọng (2024) có đáp án chi tiết nhất
30 Bài tập về Một số oxit quan trọng (2024) có đáp án chi tiết nhất
30 Bài tập về Một số axit quan trọng (2024) có đáp án chi tiết nhất