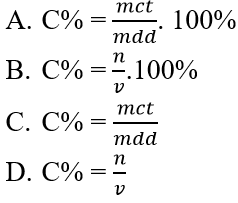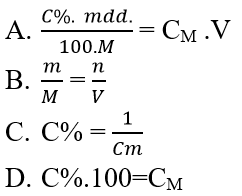Bài tập về dung dịch
I. Lý thuyết
1. Dung dịch, dung môi, chất tan
- Dung môi: là chất có khả năng hòa tan chất khác để tạo thành dung dịch.
- Chất tan: là chất bị hòa tan trong dung môi.
- Dung dịch: là hỗn hợp đồng nhất giữa dung môi và chất tan.
Ví dụ 1: Hòa tan muối ăn vào nước thì:
- Muối ăn là chất tan
- Nước là dung môi.
- Hỗn hợp nước và muối gọi là dung dịch.
Ví dụ 2: Dầu ăn không hòa tan trong nước nhưng lại tan được trong dung môi hữu cơ như xăng, CCl4,…
2. Dung dịch chưa bão hòa, dung dịch bão hòa
- Ở một nhiệt độ nhất định:
+ Dung dịch chưa bão hòa là dung dịch vẫn có thể hòa tan thêm chất tan.
+ Dung dịch bão hòa là dung dịch không thể hòa tan thêm chất tan.
Ví dụ: Hòa tan đường vào nước:
+ Ở giai đoạn đầu: đường tan trong nước ta được dung dịch đường, dung dịch này vẫn có thể hòa tan thêm đường
=> dung dịch chưa bão hòa.
+ Ở giai đoạn sau: cứ hòa tan mãi đường thì đến thời điểm không thể hòa tan thêm được nữa => dung dịch bão hòa.
* Lưu ý: Độ bão hòa của một dung dịch thay đổi theo nhiệt độ (toC), P (áp suất) và tùy thuộc vào chất tan rắn, lỏng hay chất dễ bay hơi.
Ví dụ: Ở 20oC, 100 gam nước hòa tan được tối đa 39,5 gam muối ăn để tạo thành dung dịch bão hòa. Nếu tăng nhiệt độ lên dung dịch trên trở thành dung dịch chưa bão hòa.
3. Biện pháp để chất rắn tan nhanh trong dung môi
a) Khuấy dung dịch:
- Khuấy dung dịch tạo ra tiếp xúc mới giữa phân tử chất rắn và các phân tử nước => sự hòa tan diễn ra nhanh hơn.
b) Đun nóng dung dịch:
- Ở nhiệt độ càng cao, các phân tử chuyển động càng nhanh làm tăng số lần va chạm giữa các phân tử nước và bề mặt chất rắn => sự hòa tan diễn ra nhanh hơn.
c) Nghiền nhỏ chất rắn:
- Nghiền nhỏ chất rắn làm tăng diện tích tiếp xúc giữa chất rắn và phân tử nước => kích thước của vật rắn càng nhỏ thì sự hòa tan diễn ra càng nhanh.
4. Mở rộng: Các công thức tính trong dung dịch
a) Công thức tính số mol khi biết nồng độ mol và thể tích dung dịch
n = CM.Vdd
Trong đó:
CM: nồng độ dung dịch (đơn vị: mol/ lít)
Vdd: thể tích dung dịch (đơn vị: lít)
b) Công thức tính số mol khi biết nồng độ phần trăm và khối lượng dung dịch
n = 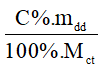
Trong đó:
C%: nồng độ phầm trăm (đơn vị: %)
mdd: khối lượng dung dịch (đơn vị: gam)
Mct: khối lượng mol chất tan (đơn vị: g/mol).
c) Công thức tính số mol khi biết nồng độ phần trăm, thể tích và khối lượng riêng của dung dịch
n = 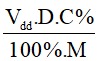
Trong đó:
Vdd: thể tích dung dịch (đơn vị: ml)
D: khối lượng riêng (g/ml)
C%: nồng độ phầm trăm (đơn vị: %)
M: khối lượng mol (đơn vị: g/mol).
d) Công thức tính độ tan
S = 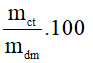
Trong đó:
mct: là khối lượng chất tan (đơn vị: gam)
mdd: là khối lượng dung dịch (đơn vị: gam)
e) Công thức tính nồng độ phần trăm khi biết khối lượng chất tan và khối lượng dung dịch
C% = 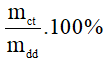
Trong đó:
mct: khối lượng chất tan (đơn vị: gam)
mdd: khối lượng dung dịch (đơn vị: gam)
f) Công thức tính nồng độ phần trăm khi biết nồng độ mol và khối lượng riêng
C% = 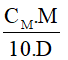
Trong đó:
CM: nồng độ mol (đơn vị: mol/ lít)
M: khối lượng mol (đơn vị: g/mol)
D: khối lượng riêng (đơn vị: g/ml)
g) Công thức về nồng độ mol khi biết số mol và thể tích
CM = 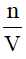
Trong đó:
n: số mol chất tan (đơn vị: mol)
V: thể tích dung dịch (đơn vị: lít)
h) Công thức về nồng độ mol khi biết nồng độ phần trăm và khối lượng riêng
CM = 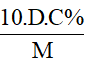
Trong đó:
D: khối lượng riêng (đơn vị: g/ml)
C%: nồng độ phần trăm (đơn vị: C%)
M: khối lượng mol (đơn vị: g/mol)
i) Công thức tính độ rượu
Độ rượu = 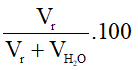
Trong đó:
Vr: thể tích rượu nguyên chất;
VH2O: thể tích nước có trong dung dịch
Vr và VH2O phải cùng đơn vị
II. Ví dụ minh hoạ
Ví dụ 1: Dung dich NaOH 4M (D = 1,43 g/ml). Tính C%
A. 11%
B. 12,2%
C. 11,19%
D. 11,179%
Đáp án: C
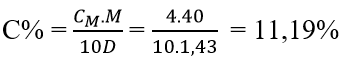
Ví dụ 2: Hòa tan 40 g đường với nước được dung dịch đường 20%. Tính khối lượng dung dịch đường thu được
A. 150 gam
B. 170 gam
C. 200 gam
D. 250 gam
Đáp án: C
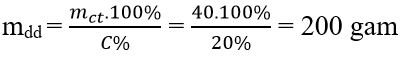
Ví dụ 3: Hòa tan 50 g đường với nước được dung dịch đường 10%. Tính khối lượng nước cần chop ha chế dung dịch
A. 250 gam
B. 450 gam
C. 50 gam
D. 500 gam
Đáp án: B
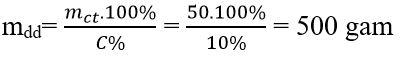
mnước = mdd - m = 500 – 50 = 450 gam
III. Bài tập vận dụng
Câu 1: Số mol trong 400 ml NaOH 6M là
A. 1,2 mol
B. 2,4 mol
C. 1,5 mol
D. 4 mol
Đáp án: B
Hướng dẫn giải: n = CM.V = 0,6.4 = 2,4 (mol)
Câu 2: Hòa tan 300 ml Ba(OH)2 0,4M. Tính khối lượng cuả Ba(OH)2
A. 20,52 gam
B. 2,052 gam
C. 4,75 gam
D. 9,474 gam
Đáp án: A
Hướng dẫn giải:
+ nBa(OH)2 = 0,4.0,3 = 0,12 mol
+ mBa(OH)2 = 0,12.171 = 20,52 g
Câu 3: Hòa tan CuSO4 40% trong 90 g dung dịch. Số mol cần tìm là
A. 0,225 mol
B. 0,22 mol
C. 0,25 mol
D. 0,252 mol
Đáp án: A
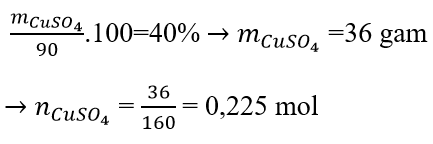
Câu 4: Tính nồng độ mol của 456 ml Na2CO3 10,6 gam
A. 0,32 M
B. 0,129 M
C. 0,2 M
D. 0,219 M
Đáp án: D
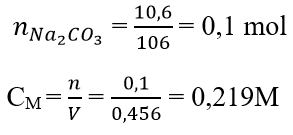
Câu 5: Công thức tính nồng độ phần trăm là
Đáp án: A
Câu 6: Mối quan hệ giữa C% và CM
Đáp án: A
Câu 7: Dung dich HCl 25% (D = 1,198 g/ml). Tính CM
A. 8M
B. 8,2M
C. 7,9M
D. 6,5M
Đáp án: B
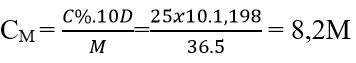
Xem thêm các dạng bài tập Hoá học khác:
30 Bài tập Anilin tác dụng với dung dịch brom (2024) có đáp án chi tiết nhất
30 Bài tập về phân loại muối (2024) có đáp án
30 Bài tập CO2 tác dụng với dung dịch kiềm (2024) có đáp án chi tiết nhất