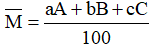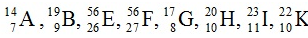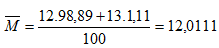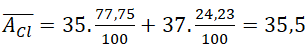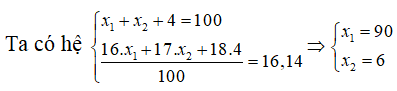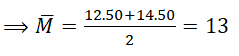Bài tập tính nguyên tử khối trung bình
I. lí thuyết và phương pháp giải
Áp dụng công thức tính nguyên tử khối trung bình:
Với: a, b, c là số nguyên tử (hoặc % số nguyên tử) của mỗi đồng vị.
A, B, C là nguyên tử khối (hay số khối) của mỗi đồng vị.
II. Ví dụ minh họa
Ví dụ 1: Đồng vị là những nguyên tử của cùng một nguyên tố, có số proton bằng nhau nhưng khác nhau về:
A. số electron
B. số notron
C. số proton
D. số obitan
Lời giải:
⇒ Chọn B.
Nhắc lại: Các đồng vị của cùng một nguyên tố hóa học là những nguyên tử có cùng số proton nhưng khác nhau về số notron, do đó số khối A khác nhau.
Ví dụ 2: Trong dãy kí hiệu các nguyên tử sau: .
Các kí hiệu nào cùng chỉ cùng 1 nguyên tố hoá học?
A. A, G và B
B. H và K
C. H, I và K
D. E và F
Lời giải:
H và K cùng 1 nguyên tố hóa học do có cùng số p là 10
⇒ Chọn B.
Ví dụ 3: Nguyên tố Cacbon có 2 đồng vị bền: 612C chiếm 98,89% và 613C chiếm 1,11%. Nguyên tử khối trung bình của C là bao nhiêu?
Lời giải:
Vậy NTK trung bình của C là 12,0111
III. Bài tập vận dụng
Câu 1. Nguyên tố hóa học bao gồm các nguyên tử:
A. Có cùng số khối A.
B. Có cùng số proton.
C. Có cùng số nơtron.
D. Có cùng số proton và số nơtron.
Lời giải:
Đáp án: B
Nguyên tố hóa học bao gồm các nguyên tử có cùng số proton khắc số notron ( hay khác số khối)
Câu 2. Trong dãy kí hiệu các nguyên tử sau, dãy nào chỉ cùng một nguyên tố hóa học:
A. 6A14 ; 7B15
B. 8C16; 8D17; 8E18
C. 26G56; 27F56
D. 10H20 ; 11I22
Lời giải:
Đáp án: B
Câu 3. Cho ba nguyên tử có kí hiệu là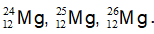
A. Số hạt electron của các nguyên tử lần lượt là: 12, 13, 14.
B. Đây là 3 đồng vị.
C. Ba nguyên tử trên đều thuộc nguyên tố Mg.
D. Hạt nhân của mỗi nguyên tử đều có 12 proton.
Lời giải:
Đáp án: A
Kí hiệu của nguyên tử có dạng với Z là số hiệu nguyên tử, A là số khối
Nhận thấy 3 nguyên tử đều có cùng số Z, khác số khối → 3 nguyên tử là đồng vị của nguyên tố Mg → B, C đúng
Luôn có Z = số p = số e = 12
Câu 4. Nguyên tố clo có hai đồng vị bền 1735Cl chiếm 75,77% và 1737Cl chiếm 24,23%. Tính nguyên tử khối trung của clo?
A. 35
B. 35,5
C. 36
D. 37
Lời giải:
Đáp án: B
Nguyên tử khối trung bình của clo là:
Câu 5. Có 3 nguyên tử: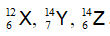
A. X, Y
B. Y, Z
C. X, Z
D. X, Y, Z
Lời giải:
Đáp án: C
Đồng vị là những nguyên tử có cùng số proton ( số hiệu nguyên tử) khác nhau số khối
Thấy X, Z có cùng số proton là 6 , khác nhau số khối → X và Z là đồng vị của nguyên tố Cacbon.
Câu 6. Nguyên tử khối trung bình của đồng là 63,54. Trong tự nhiên, đồng có hai đồng vị 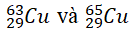
A. 28%
B. 73%
C 42%
D. 37%
Lời giải:
Đáp án: B
Gọi x là % số nguyên tử của 2963Cu ⇒ 100 – x là % của 2965Cu
Ta có 63,54 = (63x + 65(100 - x))/100 ⇒ x = 73
Vậy 2963Cu chiếm 73%
Câu 7. Trong tự nhiên có hai đồng vị bền: 1737Cl chiếm 24,23% tổng số nguyên tử, còn lại là 1735Cl. Thành phần % theo khối lượng của 1737Cl trong HClO4 là:
A. 8,92%
B. 8,43%
C. 8,56%
D. 8,79%
Lời giải:
Đáp án: A
Câu 8. Nguyên tố cacbon có hai đồng vị bền: 12Cchiếm 98,89% và 13C chiếm 1,11%. Nguyên tử khối trung bình của nguyên tố cacbon là
A. 12,5245
B. 12,0111
C. 12,0219
D. 12,0525
Lời giải:
Đáp án: B
Mtb = 98.89% x 12 + 1.11% x 13 = 12,0111
Câu 9. Trong tự nhiên Oxi có 3 đồng vị 16O(x1%) , 17O(x2%) , 18O(4%), nguyên tử khối trung bình của Oxi là 16,14. Phần trăm đồng vị 16O và 17O lần lượt là
A. 35% & 61%
B. 90% & 6%
C. 80% & 16%
D. 25% & 71%
Lời giải:
Đáp án: B
Luôn có x1 + x2 + 4 = 100
Nguyên tử khối trung bình của O là 16.14 = (16x1 + 17x2 + 18.4)/100
Ta có hệ
Câu 10. Một nguyên tố X gồm hai đồng vị là X1 và X2. Đồng vị X1 có tổng số hạt là 18. Đồng vị X2 có tổng số hạt là 20. Biết rằng % các đồng vị trong X bằng nhau và các loại hạt trong X1 cũng bằng nhau. Xác định nguyên tử khối trung bình của X?
A. 13
B. 19
C. 12
D. 16
Lời giải:
Đáp án: A
Các hạt trong đồng vị X1 bằng nhau nên: P = E = N = 18/3 = 6
⇒ Số khối của đồng vị X1 là: P + N= 12
⇒ Số khối của đồng vị X2 là: 20 – 6 = 14
Xem thêm các dạng bài tập Hóa học hay khác:
30 Bài tập về đơn chất và hợp chất, phân tử (2024) có đáp án
30 Câu trắc nghiệm lý thuyết este (2024) hay, có đáp án
30 Bài tập Xác định số oxi hóa của lưu huỳnh (S) trong hợp chất (2024) có đáp án