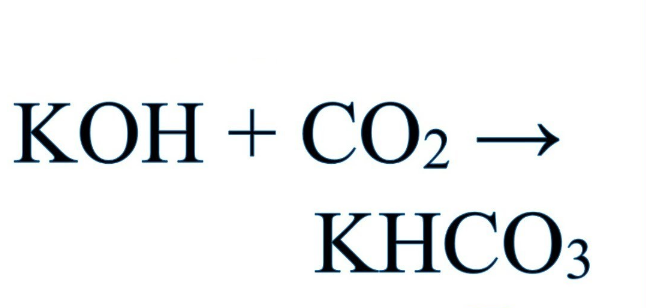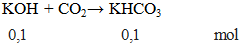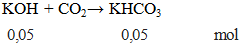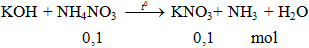Phản ứng KOH + CO2 → KHCO3
1. Phản ứng hóa học
KOH + CO2 → KHCO3
2. Điều kiện phản ứng
Phản ứng xảy ra ngay điều kiện thường.
3. Cách thực hiện phản ứng
Dẫn khí CO2 từ từ đến dư vào ống nghiệm chứa KOH và vài giọt chất chỉ thị.
4. Hiện tượng nhận biết phản ứng
Quan sát sự chuyển màu của chỉ thị phù hợp trước và sau phản ứng.
5. Bài toán CO2 dẫn vào dung dịch KOH
Khi cho CO2 (hoặc SO2) tác dụng với dung dịch KOH đều xảy ra 3 khả năng tạo muối:
CO2 + 2KOH → K2CO3 + H2O (1)
CO2 + KOH → KHCO3 (2)
Đặt T = nKOH/nCO2
Nếu T = 2 : chỉ tạo muối K2CO3
Nếu T = 1 : chỉ tạo muối KHCO3
Nếu 1 < T < 2 : tạo cả muối KHCO3 và K2CO3
Như vậy để xảy ra phương trình phản ứng (1) thì T = 2
Có những bài toán không thể tính T. Khi đó phải dựa vào những dữ kiện phụ để tìm ra khả năng tạo muối.
Hấp thụ CO2 vào NaOH dư (KOH dư) chỉ tạo muối trung hòa Na2CO3 (K2CO3)
Hấp thụ CO2 vào NaOH chỉ tạo muối Na2CO3, Sau đó thêm BaCl2 vào thấy kết tủa. Thêm tiếp Ba(OH)2 dư vào thấy xuất hiện thêm kết tủa nữa → Tạo cả 2 muối Na2CO3 và NaHCO3
Chất hấp thụ vào bình NaOH tăng:
mbình tăng = m dd tăng = m chất hấp thụ(CO2 + H2O có thể có)
Trong trường hợp không có các dữ kiện trên thì chia trường hợp để giải.
6. Bản chất của các chất tham gia phản ứng
6.1. Bản chất của CO2 (Cacbon dioxit)
CO2 là oxit axit tác dụng với dung dịch bazo tạo thành muối và nước.
6.2. Bản chất của KOH (Kali hidroxit)
KOH là một bazo mạnh phản ứng được với oxit axit.
7. Tính chất hoá học của KOH
KOH là một bazo mạnh có khả năng làm thay đổi màu sắc các chất chỉ thị như khiến quỳ tím chuyển sang màu xanh, còn dung dịch phenolphtalein không màu thành màu hồng.
7.1. Tác dụng với oxit axit
Ở điều kiện nhiệt độ phòng, KOH tác dụng với SO2, CO2,...
KOH + SO2 → K2SO3 + H2O
KOH + SO2 → KHSO3
7.2. Tác dụng với axit
Tác dụng với axit tạo thành muối và nước
KOH(dd) + HCl(dd) → KCl(dd) + H2O
Tác dụng với các axit hữu cơ để tạo thành muối và thủy phân este, peptit
RCOOR1 + KOH → RCOOK + R1OH
7.3. Tác dụng với kim loại
KOH tác dụng với kim loại mạnh tạo thành bazo mới và kim loại mới.
KOH + Na → NaOH + K
7.4. Tác dụng với muối
KOH tác dụng với muối để tạo thành muối mới và axit mới
2KOH + CuCl2 → 2KCl + Cu(OH)2↓
7.5. KOH điện li mạnh
KOH là một bazo mạnh, trong nước phân ly hoàn toàn thành ion K+ và OH-
7.6. KOH phản ứng với một số oxit kim loại mà oxit, hidroxit của chúng lưỡng tính
KOH phản ứng được với một số oxit kim loại mà oxit, hidroxit của chúng lưỡng tính như nhôm, kẽm,…
2KOH + 2Al + 2H2O → 2KAlO2 + 3H2↑
2KOH + Zn → K2ZnO2 + H2↑
7.7. Phản ứng với một số hợp chất lưỡng tính
KOH + Al(OH)3 → KAlO2 + 2H2O
2KOH + Al2O3 → 2KAlO2 + H2O
8. Câu hỏi vận dụng
Câu 1. Cho 0,1 mol KOH phản ứng với lượng dư CO2 ở đktc thu được dung dịch X. Khối lượng muối tan có trong X là
A. 13,8 gam. B. 12,8 gam. C. 11,8 gam. D. 10,0 gam.
Lời giải:
Do CO2 dư nên có phản ứng
mmuối = 0,1.100 = 10 gam.
Đáp án D.
Câu 2. Dẫn khí CO2 từ từ đến dư vào dung dịch KOH thu được dung dịch X.Muối tan có trong dung dịch X là
A. K2CO3. B. K2CO3 và KHCO3. C. KHCO3. D. K2CO3 và KOH.
Lời giải:
Do CO2 dư nên có phản ứng KOH + CO2 → KHCO3
Muối tan có trong dung dịch X là KHCO3.
Đáp án C.
Câu 3. Cho 2,24 lít khí CO2 ở đktc phản ứng với dung dịch chứa 0,05 mol KOH. Khối lượng muối tan có trong dung dịch sau phản ứng là
A. 13,8 gam. B. 12,8 gam. C. 10 gam. D. 5 gam.
Lời giải:
Có T = 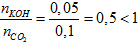
mmuối = 0,05.100 = 5 gam.
Đáp án D.
Câu 4: Hiện tượng xảy ra khi đun nóng muối NH4NO3 với KOH là
A. Có khí màu nâu đỏ bay ra.
B. Có khí mùi trứng thối thoát ra.
C. Có khí màu vàng lục, mùi xốc thoát ra.
D. Có khí mùi khai thoát ra.
Lời giải:
KOH + NH4NO3 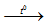
NH3 là khí có mùi khai.
Đáp án D.
Câu 5: Cho dung dịch KOH dư vào 100 ml NH4NO3 1 ml đun nóng nhẹ. Thể tích khí ở đktc thu được là
A. 1,12 lít.
B. 2,24 lít.
C. 3,36 lít.
D. 4,48 lít
Lời giải:
V = 0,1.22,4 = 2,24 lít.
Đáp án B.
Xem thêm các phương trình hóa học khác:
NH4NO3 ra NH3 | NH4NO3 + NaOH → NaNO3 + NH3↑ + H2O
FeCl3 + KOH → Fe(OH)3 + KCl | FeCl3 ra Fe(OH)3
KOH + H3PO4 → K3PO4 + H2O | KOH ra K3PO4
CO2 + KOH → K2CO3 + H2O | CO2 ra K2CO3
SO2 + KOH → K2SO3 + H2O | SO2 ra K2SO3