Phản ứng H2NCH2COOH + HCl → ClH3NCH2COOH
1. Phương trình phản ứng giữa Gly và HCl
H2NCH2COOH + HCl → ClH3NCH2COOH
2. Điều kiện phản ứng xảy ra Gly và HCl
Nhiệt độ thường
3. Bản chất của các chất tham gia phản ứng
3.1. Bản chất của H2NCH2COOH (glyxin)
Do có nhóm NH2 thể hiện tính bazo nên glyxin phản ứng với dung dịch axit.
3.2. Bản chất của HCl (Axit clohidric)
Dung dịch axit HCl có đầy đủ tính chất của một axit mạnh nên tác dụng được với chất có tính bazo.
4. Tính chất hóa học của glyxin
4.1. Tác dụng với dung dịch bazơ (do có nhóm COOH)
H2N-CH2-COOH + NaOH → H2N-CH2-COONa + H2O
4.2. Tác dụng với dung dịch axit (do có nhóm NH2)
H2N-CH2-COOH + HCl → ClH3N-CH2-COOH
4.3. Phản ứng este hóa nhóm COOH
H2N-CH2-COOH + C2H5OH 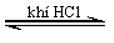
4.4. Phản ứng của NH2 với HNO2
H2N-CH2-COOH + HNO2 → HO-CH2-COOH + N2 + H2O
5. Bài tập vận dụng
Câu 1. Cho 3,0 gam glyxin tác dụng với dung dịch HCl dư, cô cạn cẩn thận dung dịch sau phản ứng thu được m gam muối khan. Giá trị của m là
A. 4,23.
B. 3,73.
C. 4,46.
D. 5,19.
Lời giải:
Đáp án: C
nGly=0,04mol⇒nHCl=nGly=0,04mol⇒mm=mGly+mHCl=0,04.75+0,04.36,5=4,46gam
Câu 2. Cho 0,2 mol H2NC3H5(COOH)2 (axit glutamic) vào 250 ml dung dịch HCl 2M, thu được dung dịch X. Cho một lượng vừa đủ dung dịch NaOH vào X để phản ứng xảy ra hoàn toàn số mol NaOH đã phản ứng là
A. 0,45.
B. 0,60.
C. 1,00.
D. 0,50.
Lời giải:
Đáp án: C
Coi hôn hợp X gồm H2NC3H5(COOH)2 và HCl không phản ứng với nhau và đều phản ứng với NaOH
→ nNaOH phản ứng = ngốc COOH- + nHCl= 0,2.2 + 0,6 = 1 mol
Câu 3. Dung dịch chất nào sau đây làm quỳ tím chuyển thành màu xanh?
A. Alanin.
B. Glyxin.
C. Lysin.
D. Valin.
Lời giải:
Đáp án: C
A, B, D không làm quỳ tím đổi màu
C: lysin làm quỳ chuyển sang màu xanh vì có 2 nhóm NH2 và 1 nhóm COOH
Câu 4. Dung dịch chất nào sau đây không làm mất màu quỳ tím?
A. Glyxin.
B. Lysin.
C. Metylamin.
D. Axit glutamic.
Lời giải:
Đáp án: A
Gly có 1 nhóm COOH và 1 nhóm NH2 nên không làm quỳ tím chuyển màu.
Câu 5. Cho 4,5 gam glyxin tác dụng với dung dịch NaOH vừa đủ, cô cạn dung dịch sau phản ứng thu được m gam muối khan. Giá trị của m là
A. 6,66.
B. 5,55.
C. 4,85.
D. 5,82.
Lời giải:
Đáp án: D
nm=ngly=0,06mol⇒mm=0,06.97=5,82gam
Câu 6. Số nguyên tử oxi trong phân tử axit glutamic là
A. 1.
B. 2.
C. 3.
D. 4.
Lời giải:
Đáp án: D
Số nguyên tử oxi trong phân tử axit glutamic là 4.
Axit glutamic là C5H9NO4, có cấu tạo: HOOC – CH2 – CH2 − CH(NH2) – COOH.
Câu 7. Hợp chất nào dưới đây thuộc loại amino axit
A. CH3COOC2H5
B. HCOONH4
C. C2H5NH2
D. H2NCH2COOH
Lời giải:
Đáp án: D
Amino axit là hợp chất hữu cơ tạp chất hữu cơ tạp chức mà trong phân tử chứa đồng thời nhóm amino (NH2) và nhóm cacboxyl (COOH).
→ Hợp chất thuộc loại amino axit là H2NCH2COOH
A là este, B là muối, C là amin
Câu 8. Phát biểu nào sau đây là đúng ?
A. Ở nhiệt độ thường, các amino axit đều là chất lỏng.
B. Axit glutamic là thành phần chính của bột ngọt,
C. Amino axit thuộc loại hợp chất hữu cơ tạp chức.
D. Các amino axit thiên nhiên hầu hết là các β-amino axit.
Lời giải:
Đáp án: C
A sai vì ở nhiệt độ thường, các amino axit ở thể rắn.
B sai vì thành phần chính của bột ngọt là muối mononatri của axit glutamic.
C đúng.
D sai các amino axit thiên nhiên hầu hết là các α-amino axit.
Câu 9. Cho 11,25 gam glyxin tác dụng với lượng dư dung dịch HCl thu được m gam muối khan. Giá trị của m là
A. 18,745.
B. 14,9.
C. 16,725.
D. 16,575.
Lời giải:
Đáp án: C
nglyxin = 11,25/75 = 0,15 mol
→ nHCl= nglyxin = 0,15mol
Bảo toàn khối lượng: mmuối = mglyxin + mHCl = 11,25 + 0,15.36,5 = 16,725 gam
Câu 10. Trong phân tử amino axit X có một nhóm amino và một nhóm cacboxyl. Cho 8,9 gam X tác dụng vừa đủ với dung dịch NaOH, cô cạn dung dịch sau phản ứng thu được 11,1 gam muối khan. Công thức của X là
A. H2NC2H4COOH.
B. H2NCH2COOH.
C. H2NC3H6COOH.
D. H2NC4H8COOH.
Lời giải:
Đáp án: A
Gọi công thức của amino axit X có dạng H2N-R-COOH
H2N-R-COOH + NaOH → H2N-R-COONa + H2O
Tăng giảm khối lượng ta có:
nX=nNaOH=11,1−8,923−1=0,1mol⇒MX=8,90,1=89⇒89=16+R+45⇒R=28
→ Công thức của X là H2N-C2H4-COOH.
Câu 11. Công thức của glyxin là
A. CH3NH2.
B. H2NCH(CH3)COOH,
C. H2NCH2COOH.
D. C2H5NH2.
Lời giải:
Đáp án: C
Công thức của glyxin là H2NCH2COOH.
Câu 12. Số nhóm amino và số nhóm cacboxyl có trong một phân tử axit glutamic tương ứng là
A. 2 và 2.
B. l và 2.
C. 2 và l.
D. 1 và 1.
Lời giải:
Đáp án: B
Axit glutamic là C5H9NO4, có cấu tạo: HOOC–CH2 – CH2 − CH(NH2) – COOH.
Câu 13. Amino axit X chứa một nhóm -NH2. Cho 15 gam X tác dụng với axit HCl (dư), thu được 22,3 gam muối khan. Công thức cấu tạo thu gọn của X là
A. H2NCH2COOH.
B. CH3CH2CH(NH2)COOH.
C. H2NCH2CH2COOH.
D. CH3CH(NH2)COOH.
Lời giải:
Đáp án: A
Gọi công thức của amino axit X có dạng H2N-R-(COOH)a
Bảo toàn khối lượng ta có:
nHCl=22,3−1536,5=0,2mol⇒nX=nHCl=0,2mol⇒16+R+45a=150,2⇒R+45a=59⇒a=1;R=14
Công thức của X là H2N-CH2-COOH.
Câu 14. Cho 0,04 mol amino axit X tác dụng vừa đủ với 400 ml dung dịch HCl 0,1M thu được 7,34 gam muối khan. Mặt khác 0,04 mol X tác dụng vừa đủ với 80 gam dung dịch NaOH 4%. Công thức của X là
A. H2NC3H6COOH.
B. H2NC2H3(COOH)2.
C. (H2N)2C3H5COOH.
D. H2NC3H5(COOH)2.
Lời giải:
Đáp án: D
Gọi công thức của amino axit X là (H2N)aR(COOH)b
nHCl=0,04mol;nNaOH=80.4%40=0,08⇒(a=nHClnX=1b=nNaOHnX=2)⇒X:H2NR
Áp dụng bảo toàn khối lượng ta có:
mX + mHCl = mmuối
→ mX = 7,34 – 0,04.36,5 = 5,88 gam
→16+R+90=5,880,04→R=41→R:C3H5
→ Công thức của X là H2NC3H5(COOH)2
Câu 15. Hỗn hợp X gồm glyxin, alanin và axit glutamic. Trong X, nguyên tố oxi chiếm 40% về khối lượng. Cho m gam X tác dụng hoàn toàn với dung dịch NaOH, tạo ra 8,16 gam muối. Giá trị của m là
A. 7,2.
B. 4.8.
C. 5.6.
D. 6,4
Lời giải:
Đáp án: D
nO(X)=0,4m16=0,025m(mol)⇒n−COOH(X)=0,0125m(mol)
Áp dụng tăng giảm khối lượng ta có:
mmuối = mX + 22n-COOH (X)
⇒8,16=m+22.0,0125m⇒m=6,4gam
Xem thêm các phương trình hóa học hay khác:
CH3COOH + C2H5OH → CH3COOC2H5 + H2O l Axit axetic ra Etyl axetat l CH3COOH ra CH3COOC2H5
C2H5OH + O2 → CH3COOH + H2O | C2H5OH ra CH3COOH | Rượu etylic ra axit axetic
NaOH + CH3COOH → CH3COONa + H2O | NaOH ra CH3COONa | CH3COOH ra CH3COONa
CH3COOH ra (CH3COO)2Mg | CH3COOH + Mg → (CH3COO)2Mg + H2
NH2CH2COOH + NaOH → NH2CH2COONa + H2O | NH2CH2COOH ra NH2CH2COONa




