Cách xác định số bậc ancol
1. Lí thuyết
1.1 Cách nhận biết ancol
- Để nhận biết ancol ta dùng kim loại Na. Phản ứng sẽ tạo bọt khí thoát ra.
- Tổng quát: 2R(OH)n + 2nNa → 2R(ONa)n + nH2↑
- Hiện tượng: Na tan trong ancol và sủi bọt khí không màu
- Ví dụ:
2C2H5OH + 2Na → 2C2H5ONa + H2↑
1.2 Cách phân biệt ancol bậc I, bậc II, bậc III
Ta có thể phân biệt bậc của ancol bằng cách oxi hóa ancol trong ống đựng CuO đun nóng sau đó nghiên cứu sản phẩm.
+ Nếu sản phẩm tạo ra là anđehit: ancol ban đầu là bậc I
+ Nếu sản phẩm tạo ra là xeton: ancol bậc II.
+ Nếu ancol không bị oxi hóa: ancol bậc III.
- Phân biệt ancol bậc I:
+ Để phân biệt ancol bậc I ta cho ancol tác dụng với CuO (đun nóng). Sau phản ứng màu đen của CuO sẽ chuyển sang màu đỏ của Cu. Sản phẩm tạo thành tác dụng với dung dịch AgNO3/NH3 tạo kết tủa trắng bạc
+ Tổng quát:
(1) RCH2OH + CuO 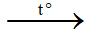 RCHO (anđehit) + H2O + Cu
RCHO (anđehit) + H2O + Cu
(2) RCHO + 2AgNO3 + 3NH3 + H2O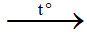 RCOONH4 + 2Ag↓ + 2NH4NO3
RCOONH4 + 2Ag↓ + 2NH4NO3
+ Hiện tượng:
Phản ứng (1): CuO màu đen chuyển dần thành màu đỏ của Cu.
Phản ứng (2): Xuất hiện lớp bạc sáng như gương bám vào thành ống nghiệm.
+ Ví dụ minh họa:
(1) CH3CH2OH + CuO 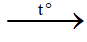 CH3CH=O + H2O + Cu
CH3CH=O + H2O + Cu
CH3-CHO + 2AgNO3 + 3NH3 + H2O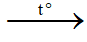 CH3-COONH4 + 2Ag↓ + 2NH4NO3
CH3-COONH4 + 2Ag↓ + 2NH4NO3
- Phân biệt ancol bậc II:
+ Để phân biệt ancol bậc II ta cho ancol tác dụng với CuO (đun nóng). Sau phản ứng màu đen của CuO sẽ chuyển sang màu đỏ.
Sản phẩm tạo thành không có phản ứng tráng gương.
+ Tổng quát:
R1CH(OH)R2 + CuO 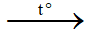 R1COR2 (xeton) + Cu + H2O
R1COR2 (xeton) + Cu + H2O
+ Hiện tượng:
CuO màu đen chuyển dần thành màu đỏ của Cu.
+ Phương trình hóa học minh họa:
CH3CH(OH)C2H5 + CuO 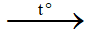 CH3-CO-CH3 + Cu + H2O
CH3-CO-CH3 + Cu + H2O
- Phân biệt ancol bậc III:
Ancol bậc III không có phản ứng với CuO như trên.
2. Bài tập vận dụng
Bài 1: Chỉ dùng các chất nào dưới đây để có thể phân biệt 2 ancol đồng phân có cùng công thức phân tử C3H7OH?
A. Na và H2SO4 đặc
B. Na và CuO
C. CuO và dung dịch AgNO3/NH3
D. Na và dung dịch AgNO3/NH3
Đáp án: B. Na và CuO
Ứng với công thức phân tử C3H7OH có 2 đồng phân là:
CH3-CH2-CH2-OH: propan-1-ol
CH3-CH(OH)-CH3:propan-2-ol
- Để phân biệt hai ancol đồng phân trên ta cho phản ứng với CuO nung nóng.
Cả hai anol đều làm màu đen của CuO chuyển thành màu đỏ của Cu.
CH3-CH2-CH2-OH + CuO 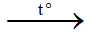 CH3-CH2-CHO (anđehit) + H2O + Cu
CH3-CH2-CHO (anđehit) + H2O + Cu
CH3-CH(OH)-CH3 + CuO 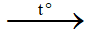 CH3COCH3 (xeton) + Cu + H2O
CH3COCH3 (xeton) + Cu + H2O
- Sản phẩm tạo thành đem đi tráng bạc.
+ Sau phản ứng tạo một lớp bạc kết tủa sáng như gương bám vào thành ống nghiệm thì ancol ban đầu là propan-1-ol
CH3-CH2-CHO + 2AgNO3 + 3NH3 + H2O CH3-CH2-COONH4 + 2Ag↓ + 2NH4NO3
CH3-CH2-COONH4 + 2Ag↓ + 2NH4NO3
+ Sản phẩm tạo thành không có phản ứng tráng gương thì ancol ban đầu là propan-2-ol
Bài 2: Cho 3,70 gam một ancol X no, đơn chức và mạch hở tác dụng cùng Na dư có thấy 0,56 lít khí thoát ra ngoài (tại đktc). Vậy công thức phân tử X là:
A. C2H6O
B. C3H10O
C. C4H10O
D. C4H8O
Đáp án: C. C4H10O
Ta có phương trình phản ứng:
2R-OH + 2Na → 2R-ONa + H2
0,05mol 0,025mol
Theo bài ra ta có: nH2 = 0,56/22,4 = 0,025 mol
Từ PTPƯ: nR-OH = 2.nH2 = 2.0,025 = 0,05 mol
Ta được: MROH = 3,7 : 0,05 = 74 g/mol
=> Ancol no, đơn chức có công thức là CnH2n + 1OH
=> 14n + 8 = 74 => n=4
C4H10O
Bài 3: Lên men dung dịch chứa 300 gam glucozơ thu được 92 gam ancol etylic. Hiệu suất của quá trình lên men tạo thành ancol etylic là:
A. 40%
B. 60%
C. 54%
D. 80%
Đáp án: B. 60%
C6H12O6 → 2C2H5OH
180g 92g
300g → 153,3g
H% = (92/153,3). 100% = 60%
Bài 4: Đung nóng một ancol đơn chức X với dung dịch H2SO4 đăc trong điều kiện nhiệt độ thích hợp sinh ra chất hữu cơ Y, tỉ khối hơi của X so với Y là 0,6956. Công thức phân tử của Y là
A. C3H8O
B. C2H6O
C. CH4O
D. C4H8O
Đáp án: C. CH4O
dX/Y < 1 ⇒ Y là ete
Ta có MY = 2MX - 18
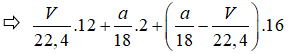
⇒ MX = 32 ⇒ X là CH4O
Bài 5: Cả phenol và ancol etylic đều phản ứng được với
A. Na
B. NaOH
C. Br2
D. NaHCO3
Đáp án: A. Na
Bài 6: Phát biểu nào sau đây không đúng ?
A. Dung dịch natri phenolat phản ứng với khí CO2 lấy chất hữu cơ vừa tạo ra cho tác dụng với dung dịch NaOH lại thu được natri phenolat
B. Phenol phản ứng với dung dịch NaOH, lấy muối vừa tạo ra cho tác dụng với dung dịch HCl lại thu được phenol
C. Cho ancol etylic tác dụng với Na lấy chất rắn thu được hòa tan vào nước lại thu được ancol etylic
D. Cho ancol metylic đi qua H2SO4 đặc ở 170oC tạo thành ankan
Đáp án: D. Cho ancol metylic đi qua H2SO4 đặc ở 170oC tạo thành ankan
Bài 7: Ancol nào sau đây phản ứng với CuO không tạo thành anđehit ?
A. metanol
B. etanol
C. 2-metylpropanol-1
D. propanol-2
Đáp án: D. propanol-2
Bài 8: Cho Na tác dụng vừa đủ với 1,24 gam hỗn hợp 3 ancol đơn chức X, Y, Z thấy thoát ra 0,336 lít khí H2 (đkc). Khối lượng muối natri ancolat thu được là
A. 2,4 gam
B. 1,9 gam
C. 2,85 gam
D. 3,8 gam
Đáp án: B. 1,9 gam
ROH + Na → RONa + 1/2 H2
nNa = 2nH2 = 0,03 mol
Áp dụng định luật bảo toàn khối lượng:
mMuối = ancol + mNa - H2 = 1,24 + 0,03.23 – 0,015.2 = 1,9 g
Bài 9: Khi đốt cháy hoàn toàn m gam hỗn hợp hai ancol no đơn chức, mạch hở thu được V lít khí CO2 (đktc) và a gam H2O. Biểu thức liên hệ giữa m, a vầ V là
A. m = 2a – V/22,4
B. m = 2a – V/11,2
C. m = a + V/5,6
D. m = a – V/5,6
Đáp án: D. m = a – V/5,6
ancol no đơn chức mạch hở ⇒ nO (ancol) = nancol = nH2O – nCO2 = a/18 - V/22,4
m = mC + mH + mO = 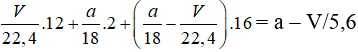
Bài 10: Cho 18,8 gam phenol tác dụng với 45g dung dịch HNO3 63% (có H2SO4 làm xúc tác ). Hiệu suất phản ứng là 100%. Khối lượng axit picric thu được là
A. 50 g
B. 34,35 g
C. 34,55 g
D. 35 g
Đáp án: B. 34,35 g
nphenol = 0,2 mol; nHNO3 = 0,45 mol
C6H5OH + 3HNO3 → C6H2(NO2)3OH + 3H2O
⇒ HNO3 hết; npicric = 1/3 nHNO3 = 0,15 mol
⇒ mpicric = 0,15. 229 = 34,35g
Xem thêm các dạng bài tập Hoá học hay khác:
Tính chất hóa học đặc trưng của kim loại (2024) chi tiết nhất
Tính chất hóa học của NaOH (2024) chi tiết nhất
Lí thuyết tổng hợp về tơ (2024) chi tiết nhất
Lí thuyết đồng phân hình học (2024) chi tiết nhất
Cách xác định số thứ tự chu kì trong bảng tuần hoàn (2024) hay nhất, chi tiết nhất




