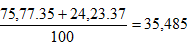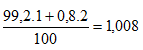Cách tính phần trăm số nguyên tử mỗi đồng vị
1. Lý thuyết
Công thức tính phần trăm số nguyên tử mỗi đồng vị
Giả sử nguyên tố R có 2 hai đồng vị A và B với số khối tương ứng là A và B
a, b là phần trăm tương ứng của 2 đồng vị trong tự nhiên.
Ta có: a + b = 100 hay b = 100 – a.
Thay vào công thức tính nguyên tử khối trung bình:
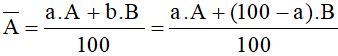
Từ đó giải ra được a và b.
Bạn nên biết
Nhiều dồng vị, đặc biệt các dồng vị phóng xạ,được sử dụng nhiều trong đời sống, y học, nghiên cứu sự phát triển của cây trồng,..
+ Tia 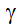 của đồng vị 60CO là tác nhân tiệt trùng, chống nấm mốc hữu hiệu trong bảo quản lương thực, thực phẩm và các hạt giống.
của đồng vị 60CO là tác nhân tiệt trùng, chống nấm mốc hữu hiệu trong bảo quản lương thực, thực phẩm và các hạt giống.
+ Sử dụng đồng vị 131I trong chuẩn đoán và điều trị tuyến giáp.
+ Tia 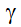 được sử dụng như một lưỡi dao sắc trong các ca mổ không chảy máu đối với các khối u nằm trong não.….
được sử dụng như một lưỡi dao sắc trong các ca mổ không chảy máu đối với các khối u nằm trong não.….
Mở rộng
Cách tính phần trăm khối lượng của một đồng vị trong phân tử:
Bước 1: Xác định được % số nguyên tử của đồng vị cần xét.
Bước 2: Xác định nguyên tử khối trung bình của đồng vị.
Bước 3: Tính % khối lượng của đồng vị cần xét trong một đơn vị về mol hoặc khối lượng.
2. Ví dụng minh họa
Ví dụ 1: Đồng có 2 đồng vị là 2963Cu và 2965Cu. Nguyên tử khối trung bình của đồng là 63,54. Tính thành phần phần trăm số nguyên tử của mỗi đồng vị.
Lời giải:
Đặt thành phần phần trăm của 2963Cu và 2965Cu lần lượt là x và 1-x (%)
M− = 63.x +65.(1-x) = 63.54
Giải PT ⇒ x= 0,73 (73%)
% 2963Cu = 73%; và % 2965Cu = 27%
Ví dụ 2: Trong tự nhiên, X có hai đồng vị 1735X và 1737X, chiếm lần lượt 75,77% và 24,23% số nguyên tử X. Y có hai đông vị à 11Y và 12Y, chiếm lần lượt 99,2% và 0,8% số nguyên tử Y.
a) Trong tự nhiên có bao nhiêu loại phân tử XY?
A. 2 B. 4 C. 5 D. 6
b) Phân tử khối trung bình của XY là
A. 36,0. B. 36,5. C. 37,5. D. 37,0.
Lời giải:
a) Các loại phân tử XY là : 35X – 1Y, 35X – 2Y, 37X – 1Y, 37X – 2Y
b) Nguyên tử khối trung bình của X :
Nguyên tử khối trung bình Y là:
Phân tử khối trung bình của XY: 35,485 + 1,008 =36,493 ≈ 36,5.
3. Bài tập vận dụng
Câu 1: Đồng có 2 đồng vị là 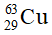 và
và 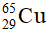 . Nguyên tử khối trung bình của đồng là 63,54. Tính thành phần phần trăm số nguyên tử của mỗi đồng vị.
. Nguyên tử khối trung bình của đồng là 63,54. Tính thành phần phần trăm số nguyên tử của mỗi đồng vị.
A. 27% và 73%
B. 37% và 63%
C. 73% và 27%
D. 63% và 37%
Hướng dẫn giải:
Đặt thành phần phần trăm của 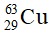 và
và 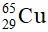 lần lượt là x (%) và 100 - x (%)
lần lượt là x (%) và 100 - x (%)
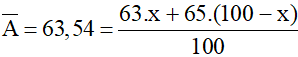
⇒ x= 73%
⇒ % 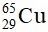 = 100% -73%=27%
= 100% -73%=27%
Đáp án C
Câu 2: Nguyên tố Bo có 2 đồng vị là 11B(x1%) và 10B(x2%) , nguyên tử khối trung bình của Bo là 10,8. Giá trị của x1 % là bao nhiêu?
A. 80%
B. 20%
C. 89,2%
D. 10,8%
Hướng dẫn giải
Ta có x2 = 100 - x1
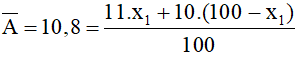
⇒x=80%
Đáp án A
Câu 3: Clo có 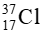 chiếm 24,23 % còn lại là
chiếm 24,23 % còn lại là 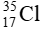 . Thành phần %
. Thành phần %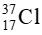 trong HClO3 là ( cho biết với hidro là đồng vị 1H, oxi là đồng vị 16O).
trong HClO3 là ( cho biết với hidro là đồng vị 1H, oxi là đồng vị 16O).
A. 9,43%
B. 10,56%
C. 9,79%
D. 10,61%
Hướng dẫn giải
Phần trăm của đồng vị 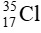 là : 100%-24,23%=75,77%
là : 100%-24,23%=75,77%
Nguyên tử khối trung bình của Clo là:
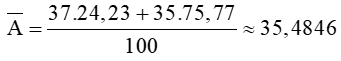
Tính trong 1 mol HClO3 -> n3717Cl= 0,2423 mol
% 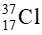 trong HClO3 là :
trong HClO3 là :
% 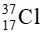 =
= 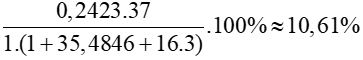
Đáp án D
Câu 4. Cho ba nguyên tử có kí hiệu là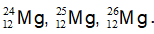
A. Số hạt electron của các nguyên tử lần lượt là: 12, 13, 14.
B. Đây là 3 đồng vị.
C. Ba nguyên tử trên đều thuộc nguyên tố Mg.
D. Hạt nhân của mỗi nguyên tử đều có 12 proton.
Hướng dẫn giải:
Đáp án: A
Kí hiệu của nguyên tử có dạng với Z là số hiệu nguyên tử, A là số khối
Nhận thấy 3 nguyên tử đều có cùng số Z, khác số khối → 3 nguyên tử là đồng vị của nguyên tố Mg → B, C đúng
Luôn có Z = số p = số e = 12
Xem thêm cách làm các dạng bài tập hóa học hay khác:
Cách tính nguyên tử khối trung bình (2024) chi tiết, có đáp án
Cách tính nồng độ đương lượng (2024) chính xác, có đáp án.
Cách tính số mol (2024) chi tiết, có đáp án
Cách tính độ pH (2024) hay, chi tiết nhất
Cách tính khối lượng nguyên tử (2024) hay nhất, chi tiết nhất