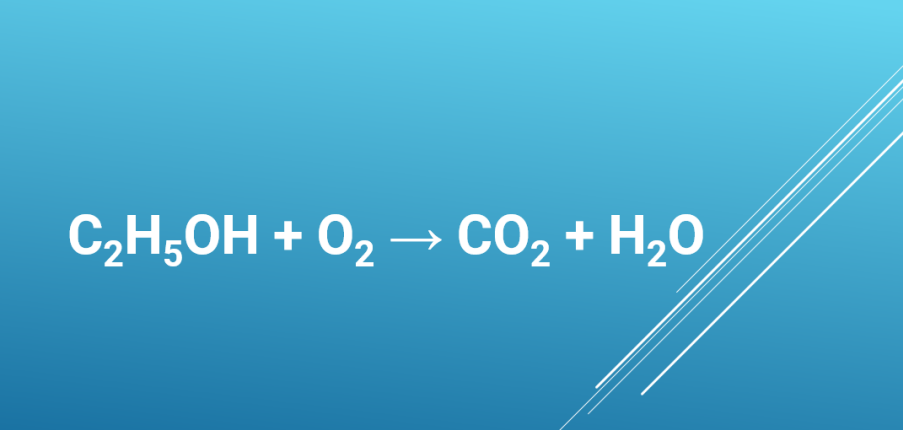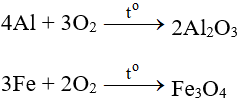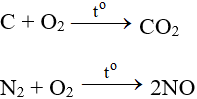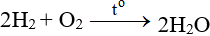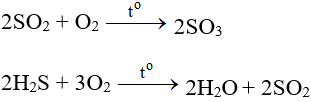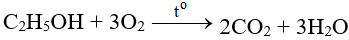Phương trình C2H5OH + 3O2 t0→ 2CO2 + 3H2O
1. Phương trình phản ứng hóa học
C2H5OH + 3O2 t0→ 2CO2 + 3H2O
2. Hiện tượng nhận biết phản ứng.
- Rượu etylic cháy với ngọn lửa màu xanh, toả nhiều nhiệt. Khí CO2 bay lên.
3. Điều kiện phản ứng
- Nhiệt độ
4. Bản chất của các chất tham gia phản ứng
4.1. Bản chất của C2H5OH (Ancol etylic)
- Trong phản ứng trên C2H5OH là chất khử.
- C2H5OH tham gia phản ứng oxi hoá hoàn toàn. Khi bị đốt, các ancol cháy, toả nhiều nhiệt. Tính chất này được dùng trong việc sát trùng dụng cụ y tế, làm nhiên liệu, ...
4.2. Bản chất của O2 (Oxi)
Trong phản ứng trên O2 là chất oxi hoá.
5. Tính chất hóa học
5.1. Tính chất hóa học của C2H5OH
Etylic C2H5OH phản ứng với oxi
Rượu etylic dễ cháy, khi cháy không có khói và ngọn lửa có màu xanh da trời,toả nhiều nhiệt
C2H5OH + 3O2 2CO2 + 3H2O
Etanol C2H5OH tác dụng với Na, NaNH3
Etanol chỉ tác dụng với Na hay NaNH2
2C2H5OH + Na → 2C2H5ONa + H2↑
C2H5OH + NaNH2 → C2H5ONa + NH3
Etanol C2H5OH phản ứng với axit axetic
Tổng quát phản ứng este hóa
ROH + R’COOH ↔ R’COOR + H2O
Phản ứng được thực hiện trong môi trường axit và đun nóng.
Phản ứng có tính thuận nghịch nên chú ý đến chuyển dịch cân bằng.
C2H5OH + CH3COOH ↔ CH3COOC2H5 + H2O
5.2. Tính chất hóa học của O2
Khi tham gia phản ứng, nguyên tử O dễ dàng nhận thêm 2e. Nguyên tử oxi có độ âm điện lớn (3,44), chỉ kém flo (3,98).
Do vậy, oxi là nguyên tố phi kim hoạt động hoá học, có tính oxi hoá mạnh. Trong các hợp chất (trừ hợp chất với flo), nguyên tố oxi có số oxi hoá là -2.
Oxi tác dụng với hầu hết các kim loại (trừ Au, Pt, ...) và các phi kim (trừ halogen). Oxi tác dụng với nhiều hợp chất vô cơ và hữu cơ.
Tác dụng với kim loại
Tác dụng với hầu hết kim loại (trừ au và Pt), cần có to tạo oxit:
Tác dụng với phi kim
Tác dụng với hầu hết phi kim (trừ halogen), cần có to tạo oxit:
ĐB: Tác dụng với H2 nổ mạnh theo tỉ lệ 2:1 về số mol:
Tác dụng với hợp chất
- Tác dụng với các chất có tính khử:
- Tác dụng với các chất hữu cơ:
6. Cách thực hiện phản ứng
- Nhỏ vài giọt rượu etylic vào chén sứ rồi đốt.
7. Bạn có biết
- Rượu etylic tác dụng mạnh với oxi khi đốt nóng.
8. Bài tập liên quan
Câu 1. Dãy sau đây gồm các chất tác dụng được với etilen trong điều kiện thích hợp?
A. Hiđro, nước, oxi, brom, hiđro bromua
B. Hiđro, nước, oxi, brom, natri hiđroxit
C. Hiđro, nước, oxi, brom, axit cacbonic
D. Hiđro, nước, oxi, brom, axit axetic
Lời giải:
Đáp án: A
Giải thích:
Dãy sau đây gồm các chất tác dụng được với etilen trong điều kiện thích hợp là:
A. Hiđro, nước, oxi, brom, hiđro bromua
C2H4+ H2 → C2H6
C2H4+ H2O → C2H5OH
C2H4 + 3O2→ 2CO2 + 2H2O
2C2H4 + 2HBr → 2C2H4Br + H2
Câu 2. Trong phòng thí nghiệm, etilen thường được điều chế bằng cách.
A. nung nóng etan để tách hidro
B. tách từ khí mỏ dầu
C. tách nước của ancol etylic
D. Cracking dầu mỏ
Lời giải:
Đáp án: C
Giải thích:
Trong phòng thí nghiệm etilen được điều chế bằng cách Đun nóng ancol etylen với H2SO4 đậm đặc
C2H5OH CH2=CH2 + H2O
Câu 3. Trong phòng thí nghiệm, một lượng nhỏ etilen được điều chế
A. từ khí cracking dầu mỏ
B. từ ancol etylic
C. từ khí etan C2H6
D. từ phản ứng của cacbon với hidro
Lời giải:
Đáp án: B
Câu 4. Dẫn m gam hỗn hợp gồm metan và etilen đi qua dung dịch nước brom thì thấy lượng brom tham gia phản ứng là 16 gam. Khí bay ra được đốt cháy hoàn toàn và dẫn sản phẩm cháy đi qua dung dịch Ba(OH)2 dư thì thu được 59,1 gam kết tủa. Giá trị của m là:
A. 4 gam
B. 5 gam
C. 8 gam
D. 2,8 gam
Lời giải:
Đáp án: C
Câu 5. Hóa chất dùng để tách etilen khỏi hỗn hợp etan và etilen là
A. dung dịch NaOH.
B. dung dịch HCl
C. dung dịch brom.
D. dung dịch AgNO3.
Lời giải:
Đáp án: C
Giải thích:
Cho hỗn hợp khí qua dung dịch brom dư, etilen bị giữ lại, thu được etan không phản ứng thoát ra ngoài
CH2=CH2 + Br2 → CH2Br-CH2Br
Câu 6. Khi dẫn khí etilen vào dung dịch Brom dư đựng trong ống nghiệm có quan sát thấy
A. màu của dung dịch brom nhạt dần, có chất kết tủa
B. màu của dung dịch brom không thay đổi
C. màu của dung dịch brom nhạt dần, có khí thoát ra
D. màu của dung dịch brom nhạt dần, có chất lỏng không tan chìm xuống đáy ống nghiệm
Lời giải:
Đáp án: D
Giải thích:
Khi dẫn khí etilen vào dung dịch Brom dư đựng trong ống nghiệm có quan sát thấy. Hiện tượng quan sát được là: Màu vàng của dung dịch nhạt hơn lúc đầu
Phương trình phản ứng hóa học
C2H4 + Br2 → C2H4Br2
Vì Br2 dư nên dd không trong suốt mà chỉ nhạt màu
Xem thêm các phương trình hóa học liên quan khác:
C2H5OH + O2 → CH3COOH + H2O | C2H5OH ra CH3COOH | Rượu etylic ra axit axetic
C2H5Cl + NaOH → C2H5OH + NaCl | C2H5Cl ra C2H5OH
C2H5OH ra C2H4 | C2H5OH → C2H4 + H2O | Ancol etylic ra Etilen