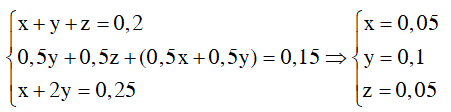C2H5OH + CuO → CH3CHO + Cu + H2O
1. Phương trình phản ứng hóa học
C2H5OH + CuO → CH3CHO + Cu + H2O
2. Hiện tượng nhận biết phản ứng.
Phương trình không có hiện tượng nhận biết đặc biệt.
Trong trường hợp này, bạn chỉ thường phải quan sát chất sản phẩm CH3CHO (Anđehit axetic) (trạng thái: dd) (màu sắc: không màu), Cu (đồng) (trạng thái: rắn) (màu sắc: đỏ), H2O (nước) (trạng thái: lỏng) (màu sắc: không màu), được sinh ra
Hoặc bạn phải quan sát chất tham gia C2H5OH (rượu etylic) (trạng thái: dd) (màu sắc: không màu), CuO (Đồng (II) oxit) (trạng thái: rắn), biến mất.
3. Điều kiện phản ứng
- Nhiệt độ
4. Bản chất của các chất tham gia phản ứng
a. Bản chất của CuO (Đồng oxit)
- Trong phản ứng trên CuO là chất oxi hoá.
- CuO có đầy đủ tính chất hoá học của một oxit bazo và dễ bị khử về Cu.
b. Bản chất của C2H5OH (Ancol etylic)
- Trong phản ứng trên C2H5OH là chất khử.
- C2H5OH là ancol bậc 1 nên sẽ tạo thành andehit khi bị oxi hoá không hoàn toàn.
5. Tính chất hóa học
5.1. Tính chất hóa học của C2H5OH
a. Etylic C2H5OH tác dụng với oxi, phản ứng cháy
- Phản ứng oxi hóa hoàn toàn
Rượu etylic tác dụng mạnh với oxi khi đốt nóng tạo ra ngọn lửa có màu xanh và tỏa nhiều nhiệt.
C2H5OH + 3O2 → 2CO2+ 3H2O
- Phản ứng oxi hóa không hoàn toàn
CH3–CH2–OH + CuO (to) → CH3–CHO + Cu + H2O
CH3–CH2–OH + O2 (xt, to) → CH3COOH + H2O
b. Etylic C2H5OH tác dụng với kim loại mạnh K, Na
Rượu etylic tác dụng được với natri kim loại giải phóng khí hidro.
2C2H5OH + Na → 2C2H5ONa + H2↑
c. Etylic C2H5OH phản ứng với axit axetic
Rượu etylic tác dụng với axit axetic tạo thành etyl axetat trong môi trường H2SO4 đặc, đun nóng. Đây là một este có mùi thơm, ít tan trong nước và thường được ứng dụng làm dung môi trong công nghiệp.
C2H5OH + CH3COOH ⇋ CH3COOC2H5 + H2O
Etylic axit axetat Etylaxetat
5.2. Tính chất hóa học của CuO
- Có đầy đủ tính chất hóa học của một oxit bazơ.
- Dễ bị khử về kim loại đồng.
a. Tác dụng với axít
CuO + 2HCl → CuCl2 + H2O
CuO + 2HNO3 → Cu(NO3)2 + H2O
b. Tác dụng với oxit axit
3CuO + P2O5 → Cu3(PO4)2
c. Tác dụng với các chất khử mạnh: H2, C, CO...
H2 + CuO 
CO + CuO 
6. Cách thực hiện phản ứng
- Cho C2H5OH tác dụng với CuO.
7. Bạn có biết
- Hiện tại chúng tôi không có thêm bất kỳ thông tin nào thêm về phương trình này.
8. Bài tập liên quan (có đáp án)
Câu 1: Tên thay thế của C2H5OH là
A. ancol etylic B. ancol metylic C. etanol D. metanol.
Lời giải:
Đáp án: C
Câu 2: Phản ứng nào sau đây không tạo anđehit axetic ?
A. Cho axetilen phản ứng với nước.
B. Oxi hóa không hoàn toàn etilen.
C. Oxi hóa không hoàn toàn ancol etylic.
D. Oxi hóa không hoàn toàn ancol metylic.
Lời giải:
Đáp án: D
Câu 3: Cho 4,6 gam một ancol no, đơn chức phản ứng với CuO dư nung nóng, thu được 6,2 gam hỗn hợp X gồm anđehit, nước. Cho toàn bộ lượng hỗn hợp X phản ứng hoàn toàn với lượng dư dung dịch AgNO3 trong NH3, đun nóng, thu được m gam Ag. Giá trị của m là
A. 10,8. B. 21,6. C. 43,2. D. 16,2.
Lời giải:
Đáp án: B
mtăng = m[O] = 6,2 – 4,6 = 1,6g
n[O] = nancol = nandehit = 0,1 mol
Mancol = 4,6 : 0,1 = 46 ⇒ C2H5OH
⇒ nAg = 2 nancol = 0,2 ⇒ m = 21,6g
Câu 4: Oxi hoá 9,2 gam ancol etylic bằng CuO đun nóng thu được 13,2 gam hỗn hợp gồm anđehit, axit, ancol dư và nước. Hỗn hợp này tác dụng với Na sinh ra 3,36 lít H2 (ở đktc). Phần trăm ancol bị oxi hoá là :
A. 25%. B. 50%. C. 75%. D. 90%.
Lời giải:
Đáp án: C
Theo giả thiết ta có :
nO pư= nCuO = (13,2-9,2)/16 = 0,25 mol; nH2 = 3,36/22,4 = 0,15 mol
Phương trình phản ứng :
CH3CH2OH + CuO → CH3CHO + H2O + Cu (1)
mol: x
CH3CH2OH + 2CuO → CH3COOH + H2O + Cu (2)
mol: y
2CH3CH2OH + 2Na → 2CH3CH2ONa + H2 (3)
mol: z 0,5z
2CH3COOH + 2Na → 2CH3COOH + H2 (4)
mol: y 0,5y
2H2O + 2Na → 2NaOH + H2 (5)
mol: (x + y) 0,5(x+y)
Theo các phương trình phản ứng và giả thiết ta có :
Vậy phần trăm khối lượng ancol bị oxi hóa là : (0,1+0,05)/0,2.100 = 75%
Câu 5: Cho các nhận định sau:
(a) Axit axetic có khả năng phản ứng được với ancol metylic, metylamin và Mg kim loại.
(b) Độ pH của glyxin nhỏ hơn đimetylamin.
(c) Dung dịch metylamin và axit glutamic đều làm hồng dung dịch phenoltalein.
(d) CH5N có số đồng phân cấu tạo nhiều hơn CH4O.
Số nhận định đúng là
A. 1.
B. 3.
C. 4.
D. 2.
Lời giải:
Đáp án: D
Giải thích:
(a) Đúng:
CH3COOH + CH3OH ⇄ CH3COOCH3 + H2O (xt: H2SO4 đặc, to)
CH3COOH + CH3NH2 → CH3COOH3NCH3
2CH3COOH + Mg → (CH3COO)2Mg + H2
(b) Đúng vì Glyxin có pH = 7 và metylamin có pH > 7.
(c) Sai vì Glu có pH < 7 nên không làm đổi màu phenolphtalein.
(d) Sai vì đều có 1 đồng phân cấu tạo (CH3NH2và CH3OH).
⇒ (a) và (b ) đúng
Câu 6. Hợp chất A chứa C, H, O có M < 90 đvC. A tham gia phản ứng tráng bạc và có thể tác dụng với H2 (xt, Ni) sinh ra ancol chứa C bậc IV trong phân tử. Công thức của A là
A. (CH3)2CHCHO.
B. (CH3)2CH-CH2CHO.
C. (CH3)3C-CH2CHO.
D. (CH3)3CCHO.
Lời giải:
Đáp án: D
Giải thích:
A có khả năng tráng bạc => A chứa gốc –CHO
Ancol chứa C bậc IV => có dạng (CH3)3C-R-CHO
Vì M < 90 => 57 + R + 29 < 90 => R = 0
Vậy kết luận A có công thức hóa học là (CH3)3CCHO.
Câu 7. Các các nhận định dưới đây
(a) Chất béo là trieste của glixerol và các axit béo.
(b) Chất béo nhẹ hơn nước, không tan trong nước nhưng tan nhiều trong dung môi hữu cơ.
(c) Phản ứng thủy phân chất béo trong môi trường kiềm gọi là phản ứng xà phòng hóa.
(d) Các este đều được điều chế từ axit cacboxylic và ancol.
(e) Tristearin, triolein có công thức lần lượt là: (C17H33COO)3C3H5, (C17H35COO)3C3H5.
(f) Tất cả các peptit có phản ứng màu với Cu(OH)2/OH-.
(g) Dung dịch saccarozơ không tham gia phản ứng tráng bạc.
Số nhận định đúng là
A. 2.
B. 4.
C. 5.
D. 3.
Lời giải:
Đáp án: B
Câu 8. Trong các chất sau đây, chất nào có nhiệt độ sôi cao nhất?
A. CH3CH2OH.
B. CH3COOH.
C. CH3CHO.
D. CH3CH3.
Lời giải:
Đáp án: B
Câu 9. Nhỏ từ từ dung dịch axit axetic vào cốc đựng một mẩu đá vôi thấy:
A. Mẩu đá vôi tan dần do axit axetic mạnh hơn axit cacbonic, không thấy có khí thoát ra.
B. mẩu đó vôi tan dần do axit axetic mạnh hơn axit cacbonic, thấy có khí không màu thoát ra.
C. Mẩu đá vôi tan dần, thấy có khí màu lục nhạt thoát ra.
D. mẩu đá vôi không thay đổi do axit axetic yếu hơn axit cacbonic
Lời giải:
Đáp án: B
Câu 10. Để trung hòa 6,72 gam một axit cacboxylic Y (no, đơn chức), cần dùng 200 gam dung dịch NaOH 2,24%. Công thức của Y là
A. CH3COOH.
B. HCOOH.
C. C2H5COOH.
D. C3H7COOH.
Lời giải:
Đáp án: A
Giải thích:
mNaOH = 200.(2,24/100) = 4,48 (g) => nNaOH = 0,112 mol
nY = nNaOH = 0,112 mol => MY = 6,72:0,112 = 60 (CH3COOH)
Câu 11. C2H5OH tác dụng với CuO ở điều kiện thích hợp thu được chất nào sau đây?
A. HCOOH
B. C2H4
C. HCHO
D. CH3CHO
Lời giải:
Đáp án: D
Giải thích:
Phản ứng oxi hóa ancol bậc 1 tạo andehit: CH3CH2OH + CuO → CH3CHO + Cu + H2O
Câu 12. Cho 3,3 gam một anđehit X đơn chức, mạch hở phản ứng với lượng dư AgNO3trong dung dịch NH3, đun nóng. Lượng Ag sinh ra cho phản ứng hết với axit HNO3loãng, thoát ra 1,12 lít khí NO (sản phẩm khử duy nhất, (đktc)). Công thức cấu tạo thu gọn của X là
A. CH3CHO.
B. HCHO.
C. CH3CH2CHO.
D. CH2=CHCHO.
Lời giải:
Đáp án: A
Giải thích:
Ta có: nAg = 3nNO= 0,15 mol
Trường hợp 1: 1 anđehit tạo ra 4Ag
→ nX = 0,075mo → MX = 88
không có công thức nào thỏa mãn.
Trường hợp 2: 1 anđehit tạo ra 2 Ag
→ nX = 0,15mol → MX = 44g (CH3CHO)
Câu 13. Cho 20,5 gam hỗn hợp X gồm rượu etylic và axit axetic tác dụng hết với natri dư thu được 4,48 lít khí (đktc). Tính thành phần % khối lượng rượu etylic và axit axetic trong hỗn hợp X
A. 56,1% và 43,9%
B. 43,9% và 56,1%
C. 46,1% và 53.9%
D. 53.9% và 46,1%
Lời giải:
Đáp án: A
Giải thích:
Gọi số mol rượu etylic và axit axetic trong X lần lượt là x và y (mol).
+ mX = 46x + 60y = 20,5 (1)
Phương trình hóa học:
2C2H5OH + 2Na → 2C2H5ONa + H2
x → 0,5x (mol)
2CH3COOH + 2Na → 2CH3COONa + H2
y → 0,5y (mol)
Theo phương trình hóa học ⟹ nH2 = 0,5x + 0,5y = 0,2 (2)
Từ (1) và (2) ⟹ x = 0,25 và y = 0,15.
mC2H5OH= 0,25.46 = 11,5(g) => %C2H5OH = (11,5/20,5).100 = 56,1%
%CH3COOH = 100% - 56,1% = 43,9%
Xem thêm các phương trình hóa học hay khác:
C2H5OH + O2 → CH3COOH + H2O | C2H5OH ra CH3COOH | Rượu etylic ra axit axetic
C2H5OH + Na → C2H5ONa + H2 | C2H5OH ra C2H5ONa
C2H5OH ra C2H4 | C2H5OH → C2H4 + H2O | Ancol etylic ra Etilen