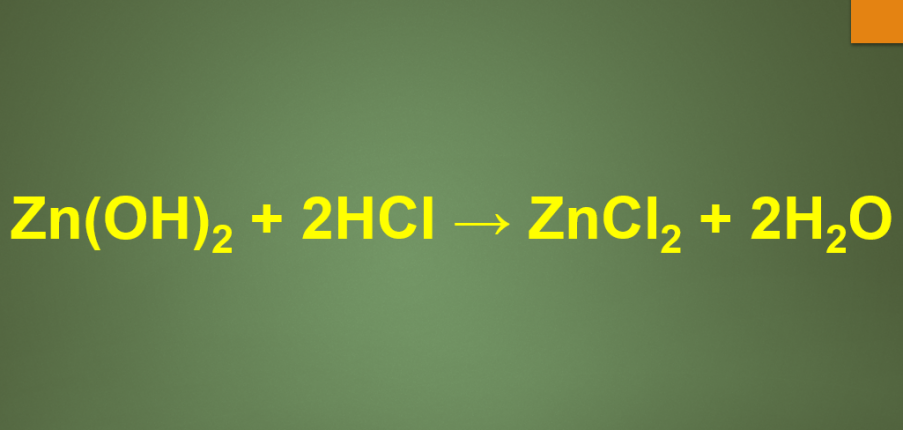Phương trình Zn(OH)2 + 2HCl → ZnCl2 + 2H2O
1. Phương trình phản ứng hóa học
Zn(OH)2 + 2HCl → ZnCl2 + 2H2O
2. Hiện tượng nhận biết phản ứng
Thấy chất rắn tan dần
3. Điều kiện phản ứng
Điều kiện thường
4. Tính chất hoá học
4.1. Tính chất hoá học của Zn(OH)2
- Mang tính chất của hiđroxit lưỡng tính.
Phản ứng với axit
Zn(OH)2 + 2HCl → ZnCl2 + 2H2O
Zn(OH)2 + H2SO4 → ZnSO4 + 2H2O
Hòa tan trong kiềm đặc và trong amoniac
Zn(OH)2 + 2NaOH → Na2ZnO2 + 2H2O
Zn(OH)2 + 4NH3 → [Zn(NH3)4](OH)2
Nhiệt phân
Zn(OH)2 
Zn(OH)2 còn tác dụng với các axit hữu cơ như
2CH3COOH + Zn(OH)2 → (CH3CCO)2Zn + 2H2O
4.2. Tính chất hoá học HCl
- Dung dịch axit HCl có đầy đủ tính chất hoá học của một axit mạnh.
Tác dụng chất chỉ thị
Dung dịch HCl làm quì tím hoá đỏ (nhận biết axit)
HCl → H+ + Cl-
Tác dụng với kim loại
Tác dụng với KL (đứng trước H trong dãy Bêkêtôp) tạo muối (với hóa trị thấp của kim loại) và giải phóng khí hidrô (thể hiện tính oxi hóa)
Cu + HCl → không có phản ứng
Tác dụng với oxit bazo và bazo: Sản phẩm tạo muối và nước
NaOH + HCl → NaCl + H2O
CuO + 2HCl 
Fe2O3 + 6HCl
Tác dụng với muối (theo điều kiện phản ứng trao đổi)
CaCO3 + 2HCl → CaCl2 + H2O + CO2↑
AgNO3 + HCl → AgCl↓ + HNO3
(dùng để nhận biết gốc clorua )
Ngoài tính chất đặc trưng là axit , dung dịch axit HCl đặc còn thể hiện vai trò chất khử khi tác dụng chất oxi hoá mạnh như KMnO4, MnO2, K2 Cr2O7, MnO2, KClO3 ……
4HCl + MnO2 
K2 Cr2 O7 + 14HCl → 3Cl2 + 2KCl + 2CrCl3 + 7H2 O
Hỗn hợp 3 thể tích HCl và 1 thể tích HNO3 đặc được gọi là hỗn hợp nước cường toan ( cường thuỷ) có khả năng hoà tan được Au ( vàng)
3HCl + HNO3 → 2Cl + NOCl + 2H2O
NOCl → NO + Cl
Au + 3Cl → AuCl3
5. Cách thực hiện phản ứng
Đem hòa tan Zn(OH)2 vào dung dịch HCl dư
6. Bạn có biết
Zn(OH)2 là một hiđroxit lưỡng tính, vừa có thể tác dụng với axit, vừa có thể tác dụng với bazơ.
Zn(OH)2 ↓ + 2NaOH → Na2ZnO2 + 2H2O
7. Bài tập liên quan
Bài 1: Chất nào sau đây không phản ứng với NaOH ở điều kiện thường?
A. Zn(OH)2
B. Al(OH)3
C. Fe(OH)3
D. NaHCO3
Hướng dẫn giải
Đáp án C
Vì Fe(OH)3 không tác dụng với dung dịch NaOH.
Bài 2: Dãy gồm các hiđroxit lưỡng tính là
A. Ca(OH)2, Pb(OH)2, Zn(OH)2
B. Ba(OH)2, Al(OH)3, Pb(OH)2
C. Zn(OH)2, Al(OH)3, Pb(OH)2
D. Zn(OH)2, Al(OH)3, Ba(OH)2
Hướng dẫn giải:
Đáp án C
Hiđroxit lưỡng tính là hiđroxit khi tan trong nước vừa có thể phân li như axit, vừa có thể phân li như bazơ.
Một số hiđroxit thường gặp: Zn(OH)2, Al(OH)3, Pb(OH)2, Sn(OH)2, …
Bài 3: Nhỏ từ từ dung dịch HCl đến dư vào ống nghiệm chứa Zn(OH)2. Hiện tượng thu được sau phản ứng là:
A. Không có hiện tượng gì
B. Chất rắn tan dần cho đến hết
C. Có khí thoát ra
D. Chất rắn tan dần và có khí thoát ra
Hướng dẫn giải
Đáp án B
Phương trình hóa học:
Zn(OH)2 + 2HCl → ZnCl2 + 2H2O
⇒ Hiện tượng: chất rắn tan dần đến hết.
Bài 4: Dãy chất nào sau đây phản ứng được với dung dịch HCl
A. CaCO3, ZnO, Zn(OH)2, Zn
B. Cu, CaO, SO2, Al
C. Ag, MgO, NaOH, SO2
D. SO2, Na2O, KOH, NaBr
Hướng dẫn giải
Đáp án A
Loai B vì Cu, SO2 không phản ứng với dung dịch HCl
Loại C vì Ag, SO2 không phản ứng với dung dịch HCl
Loại D vì SO2không phản ứng với dung dịch HCl
Dãy chất nào sau đây phản ứng được với dung dịch HCl
A. CaCO3, ZnO, Zn(OH)2, Zn
Bài 5. Dãy chất nào sau đây, trong nước đều là chất điện li mạnh?
A. H2SO4, Zn(NO3)2, CaCl2, H2S
B. AgCl, CH3COOH, Fe(NO3)3, Zn(OH)2
C. HNO3, Mg(OH)2, BaCl2, NaOH
D. HNO3, CaCl2, AlCl3, Ba(OH)2
Hướng dẫn giải