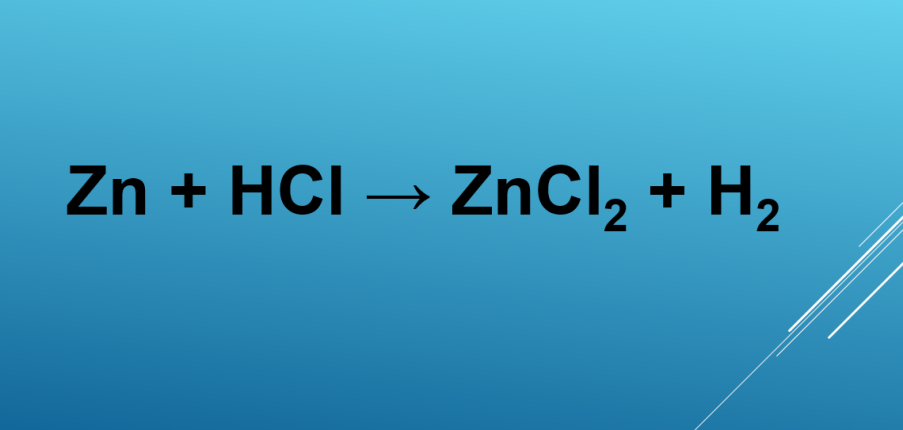
Zn + 2HCl → ZnCl2 + H2
1. Phương trình phản ứng Zn tác dụng HCl
Zn + 2HCl → ZnCl2 + H2
Đây cũng là một trong các phương trình điều chế khí hiđro phản ứng thế
2. Điều kiện để phản ứng Zn tác dụng HCl
Nhiệt độ
3. Điều chế H2 trong phòng thí nghiệm
- Trong phòng thí nghiệm để điều chế H2 thường sử dụng axit HCl (hoặc H2SO4 loãng) và kim loại Zn (hoặc Fe, hoặc Al).
Zn + 2HCl → ZnCl2 + H2↑
- Khí H2 ít tan trong nước và nhẹ hơn không khí nên ta có thể thu H2 theo 2 cách: Đẩy nước và đẩy không khí.
4. Bản chất của các chất tham gia phản ứng
4.1. Bản chất của Zn (Kẽm)
- Trong phản ứng trên Zn là chất khử.
- Zn là kim loại hoạt động có tính khử mạnh tác dụng được với các axit.
4.2. Bản chất của HCl (Axit clohidric)
- Trong phản ứng trên HCl là chất oxi hoá.
- HCl tác dụng với kim loại đứng trước H trong dãy hoạt động hóa học ( trừ Pb) tạo thành muối và khí hidro.
5. Tính chất hoá học của Zn
Kẽm là kim loại hoạt động có tính khử mạnh Zn → Zn2+ + 2e
5.1. Tác dụng với phi kim
Zn tác dụng trực tiếp với nhiều phi kim.
2Zn + O2 → 2ZnO
Zn + Cl2 → ZnCl2
5.2. Tác dụng với axit
- Với các dung dịch axit HCl, H2SO4 loãng:
Zn + 2HCl → ZnCl2 + H2
- Với dung dịch HNO3, H2SO4 đặc:
Zn + 4HNO3 đ → Zn(NO3)2 + 2NO2 + 2H2O
5.3. Tác dụng với H2O
Phản ứng này hầu như không xảy ra vì trên bề mặt của kẽm có màng oxit bảo vệ.
5.4. Tác dụng với bazơ
Kẽm tác dụng với dung dịch bazơ mạnh: NaOH, KOH, Ca(OH)2....
Zn + 2NaOH + 2H2O → Na2[Zn(OH)4] + H2
6. Tính chất hóa học của HCl
Dung dịch axit HCl có đầy đủ tính chất hoá học của một axit mạnh.
6.1. Tác dụng chất chỉ thị
Dung dịch HCl làm quì tím hoá đỏ (nhận biết axit)
HCl → H+ + Cl-
6.2. Tác dụng với kim loại
Tác dụng với KL (đứng trước H trong dãy Bêkêtôp) tạo muối (với hóa trị thấp của kim loại) và giải phóng khí hidrô (thể hiện tính oxi hóa)
Cu + HCl → không có phản ứng
6.3. Tác dụng với oxit bazo và bazo
Sản phẩm tạo muối và nước
NaOH + HCl → NaCl + H2 O
6.4. Tác dụng với muối (theo điều kiện phản ứng trao đổi)
CaCO3 + 2HCl → CaCl2 + H2O + CO2↑
AgNO3 + HCl → AgCl↓ + HNO3
(dùng để nhận biết gốc clorua )
Ngoài tính chất đặc trưng là axit , dung dịch axit HCl đặc còn thể hiện vai trò chất khử khi tác dụng chất oxi hoá mạnh như KMnO4, MnO2, K2Cr2O7, MnO2, KClO3 ……
K2Cr2O7 + 14HCl → 3Cl2 + 2KCl + 2CrCl3 + 7H2O
Hỗn hợp 3 thể tích HCl và 1 thể tích HNO3 đặc được gọi là hỗn hợp nước cường toan ( cường thuỷ) có khả năng hoà tan được Au ( vàng)
3HCl + HNO3 → 2Cl + NOCl + 2H2O
NOCl → NO + Cl
Au + 3Cl → AuCl3
7. Bài tập vận dụng liên quan
Bài 1: Hòa tan hoàn toàn 15,4 gam hỗn hợp Mg và Zn trong dung dịch HCl dư thấy có 0,6 gam khí H2 bay ra. Khối lượng muối tạo thành trong dung dịch là
A. 35,7 gam
B. 36,7 gam
C. 53,7gam
D. 63,7 gam
Hướng dẫn giải:
Đáp án B
nCl- = nHCl = 2nH2 = 0,6 mol.
Ta có: mmuối = mKL + 35,5. nCl-
⇒ mmuối = 36,7 gam.
Bài 2: Dãy nào sau đây chỉ gồm các chất vừa tác dụng được với dung dịch HCl, vừa tác dụng được với dung dịch AgNO3?
A. Fe, Ni, Ag.
B. Zn, Cu, Mg.
C. Cu, Na, Ba.
D. Cr, Zn, Al.
Hướng dẫn giải:
Đáp án D
Cr + 2HCl → CrCl2 + H2
Fe + 2HCl → FeCl2 + H2
2Al + 6HCl → 2AlCl3 + 3H2
Cr + 2AgNO3 → Cr(NO3)2 + 2Ag
Zn + 2AgNO3 → Zn(NO3)2 + 2Ag
Al + 3AgNO3 → Al(NO3)3 + 3Ag
Bài 3: Kim loại tác dụng với dung dịch HCl và tác dụng với khí Cl2 đều thu được cùng một muối là?
A. Cu
B. Zn
C. Ag
D. Fe
Hướng dẫn giải
Đáp án: B
Cu, Ag không phản ứng với HCl => Loại
Fe tác dụng Cl2 tạo FeCl3; Fe tác dụng HCl tạo FeCl2
Zn tác dụng với Cl2 và HCl đều tạo ZnCl2
Zn + Cl2 → ZnCl2
Zn + 2HCl → ZnCl2 + H2
Bài 4: Cho m gam hỗn hợp kim loại Zn, Cu vào dung dịch HCl (dư). Sau khi các phản ứng xảy ra hoàn toàn, thu được 4,48 lít H2 (đktc) và 2,0 gam kim loại không tan. Gía trị của m là:
A. 8,50.
B. 18,0.
C. 15,0.
D. 16,0
Hướng dẫn giải:
Đáp án C
Cu không phản ứng với dung dịch HCl. 2 gam chất rắn không tan chính là khối lượng của Cu.
nZn = nH2 = 4,48/22,4 = 0,2 mol;
⇒ mZn = 65.0,2 = 13g;
⇒ m = 13 + 2 = 15g.
Câu 5. Trong những oxit sau: CuO, MgO, Fe2O3, CaO, Na2O. Oxit nào không bị Hidro khử:
A. CuO, MgO
B. Fe2O3, Na2O
C. Fe2O3, CaO
D. CaO, Na2O, MgO
Hướng dẫn giải:
Bài 6: Cho m gam hỗn hợp kim loại Zn, Cu vào dung dịch HCl (dư). Sau khi các phản ứng xảy ra hoàn toàn, thu được 4,48 lít H2 (đktc) và 2,0 gam kim loại không tan. Gía trị của m là:
A. 15g.
B. 14,35g
C. 8,5g
D. 13g
Hướng dẫn giải
Đáp án A
Cu không phản ứng với dung dịch HCl. 2 gam chất rắn không tan chính là khối lượng của Cu.
nZn = nH2 = 4,48/22,4 = 0,2 mol;
⇒ mZn = 65.0,2 = 13g;
⇒ m = 13 + 2 = 15g.
Câu 7. Sau phản ứng của CuO và H2 thì có hiện tượng gì:
A. Sau phản ứng, chất rắn màu đen chuyển thành xanh lam
B. Sau phản ứng, chất rắn màu đen chuyển thành đỏ
C. Có chất khí bay lên
D. Không có hiện tượng
Hướng dẫn giải:
Câu 8. Sau phản ứng Zn và HCl trong phòng thí nghiệm, đưa que đóm đang cháy vào ống dẫn khí , khí thoát ra cháy được trong không khí với ngọn lửa màu gì?
A. Đỏ
B. Xanh nhạt
C. Cam
D. Tím
Hướng dẫn giải:
Xem thêm các phương trình hóa học hay khác:
Zn + HNO3 (đặc) → Zn(NO3)2 + NO2 + H2O | Zn ra Zn(NO3)2
Zn + HNO3 loãng → Zn(NO3)2 + NH4NO3 + H2O | Zn + HNO3 ra NH4NO3
Zn + HNO3 → Zn(NO3)2 + N2 + H2O | Zn + HNO3 ra N2