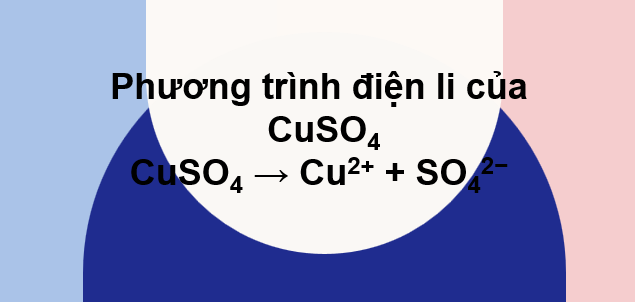
Phương trình điện li của CuSO4
1. Viết phương trình điện li của CuSO4
CuSO4 → Cu2+ + SO42−
2. Chất điện li mạnh
Chất điện li mạnh là một dung dịch/chất tan hoàn toàn hoặc gần như hoàn toàn trong nước, các phân tử hòa tan đều phân li ra ion. Chất điện li mạnh là các axit mạnh như: HCl, HNO3, HClO4, H2SO4… hay các base mạnh như: NaOH, KOH, Ca(OH)2… và hầu hết các muối.
CuSO4 là chất điện li mạnh hay yếu
CuSO4 là chất điện li mạnh
CuSO4 → Cu2+ + SO42
3. Bài tập vận dụng liên quan
Câu 1. Trong số những chất sau: H2S; FeCl3; Cl2; CO2; Ba(OH)2 có bao nhiêu chất khi tan trong nước là chất điện li?
A. 1
B. 2
C. 3
D. 4
Lời giải :
Cl2; CO2 tan trong nước tạo thành HCl, HClO và H2CO3 là chất điện li nhưng không phải là Cl2 và CO2 ban đầu do đó không phải là chất điện li.
Câu 2. Nồng độ mol của phân tử có trong dung dịch AlCl3 có [Cl-]= 0,15M là:
A .0,3 M
B. 0,05 M
C. 0,1 M
D. 0,6 M
Lời giải :
AlCl3→ Al3+ + 3Cl-
0,05M ← 0,15M
Câu 3. Nội dung nhận định nào sau đây đúng
A. Chỉ có hợp chất ion mới bị điện li khi hoà tan trong nước.
B. Độ điện li chỉ phụ thuộc vào bản chất chất điện li.
C. Độ điện li của chất điện li yếu có thể bằng 1.
D. Với chất điện li yếu, độ điện li bị giảm khi nồng độ tăng.
Lời giải :
A sai vì hợp chất cộng hóa trị cũng có thể bị phân ly khi hòa tan trong nước, ví dụ như HCl,...
B sai vì độ điện ly phụ thuộc vào nhiệt độ, nồng độ dung dịch, bản chất của chất tan và dung môi.
C sai vì chất điện ly yếu phân ly không hoàn toàn thành ion nên độ điện ly luôn nhỏ hơn 1 và lớn hơn 0.
D đúng.
Câu 4. Trong dung dịch HClO (dung môi nước) có thể chứa?
A. HClO, H+, ClO-
B. H+, ClO-
C. HClO
D. H+, HClO
Lời giải :
Câu 5. Cho các chất dưới đây: H2SO4, KOH, Ag2SO4, KCl, H2SO3,CuSO4. Các chất điện li mạnh là:
A. Ag2SO4, KCl, CuSO4, H2SO3
B. NaOH, Ag2SO4, KCl, H2SO3, H2S
C. KCl, H2SO3, CuSO4
D. H2SO4, KOH, KCl, CuSO4, Ag2SO4
Lời giải :
Đáp án D
Các chất điện li mạnh là: H2SO4, KOH, KCl, CuSO4, Ag2SO4
Phương trình điện li minh họa:
H2SO4 → 2H+ + SO42-
KOH → K+ + OH−
KCl → K+ + Cl−
CuSO4 → Cu2+ + SO42-
Ag2SO4 → 2Ag+ + SO42-
Câu 6. Dãy nào sau đây gồm các chất điện li?
A. H2S, CO2
B. Cl2, H2SO3
C. CH4, CH3OH
D. NaCl, HCl
Lời giải :
Dãy gồm các chất điện li: NaCl, HCl
Câu 7. Hòa tan 12,5 gam tinh thể CuSO4.5H2O trong nước thành 200 ml dung dịch . Tính nồng độ mol các ion trong dung dịch thu được .
Lời giải :
nCuSO4. 5H2O = 12,5/250 = 0,05 (mol)
CuSO4.5H2O → Cu2+ + SO42- + 5H2O
0,05 0,05 0,05 (mol)
[ Cu2+] = [SO42-] = 0.05/0.2 = 0.25M
Xem thêm các phương trình hóa học hay khác:
Cu+ H2SO4 → CuSO4 + SO2 + H2O | Cu ra CuSO4
CuSO4 + Na2S → CuS + Na2SO4 | CuSO4 ra CuS
H2S + CuSO4 → CuS + H2SO4 | H2S ra CuS