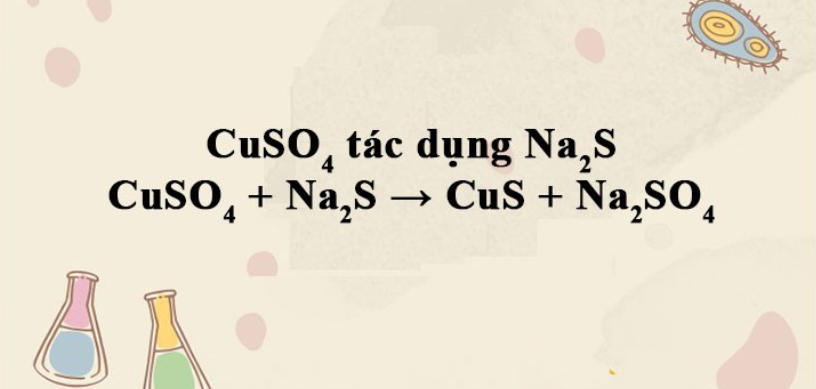Phản ứng CuSO4 + Na2S → CuS + Na2SO4
1. Phương trình phản ứng CuSO4 tác dụng Na2S
CuSO4 + Na2S → CuS↓ + Na2SO4
2. Phương trình ion rút gọn CuSO4 + Na2S
Cu2+ + S2− → CuS↓
3. Hiện tượng CuSO4 tác dụng Na2S
Xuất hiện kết tủa đen Đồng II sunfua (CuS) trong dung dịch.
4. Tính chất hóa học của CuSO4
Có tính chất hóa học của muối.
4.1. Tác dụng với dung dịch bazo
CuSO4 + 2NaOH → Cu(OH)2 + Na2SO4
CuSO4 + Ba(OH)2 → Cu(OH)2 + BaSO4
4.2. Tác dụng với muối
BaCl2 + CuSO4 → CuCl2 + BaSO4
5. Bài tập vận dụng liên quan
Câu 1. Trường hợp xảy ra phản ứng là
A. Cu + Pb(NO3)2.
B. Cu + HCl loãng
C. Cu + HCl + O2.
D. Cu + H2SO4 loãng.
Lời giải:
Câu 2. Cho m gam Cu phản ứng hết với dung dịch HNO3 thu được 4,48 lít (đktc) hỗn hợp khí NO và NO2 có khối lượng là 7,6 gam. Giá trị của m là
A. 25,6
B. 16.
C. 2,56.
D. 12,8.
Lời giải:
Câu 3. Cho các kim loại: Cu, Al, Fe, Au, Ag. Dãy gồm các kim loại được sắp xếp theo chiều tăng dần tính dẫn điện (từ trái sang phải) là
A. Fe < Au < Al < Cu < Ag
B. Fe < Al < Au < Cu < Ag
C. Fe < Al < Cu < Ag < Au
D. Al < Fe < Au < Cu
Lời giải:
Câu 4. Cho các kim loại: Cu, Al, Fe, Au, Zn. Số kim loại phản ứng được với dung dịch HCl là:
A. 2
B. 3
C. 5
D. 4
Lời giải:
Câu 5. Tính chất nào dưới đây là tính chất đặc trưng của khí hiđro sunfua?
A. Là chất khí không màu.
B. Là chất khí độc.
C. Là chất khí có mùi trứng thối.
D. Cả 3 phương án trên đều đúng.
Lời giải:
Đáp án: D
Câu 6. Có các lọ đựng hóa chất riêng rẽ: Na2S, NaCl, AgNO3, Na2CO3. Hóa chất nào sau đây có thể sử dụng để phân biệt các dung dịch đó ?
A. dung dịch NaOH.
B. dung dịch H2SO4.
C. dung dịch HCl.
D. phenolphtalein.
Lời giải:
Đáp án: C
Xem thêm các phương trình hóa học chi tiết khác:
C6H5OH + Br2 → C5H2Br3OH + HBr | C6H5OH ra C5H2Br3OH
C6H5ONa + CO2 + H2O → C6H5OH + NaHCO3 | C6H5ONa ra C6H5OH | C6H5ONa ra phenol
C6H5OH + NaOH → C6H5ONa + H2O | C6H5OH ra C6H5ONa | Phenol + NaOH
C6H6 + C2H4 → C6H5C2H5 | Benzen ra Etylbenzen | C6H6 ra C6H5C2H5