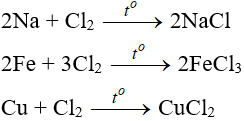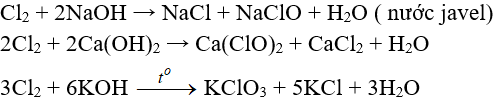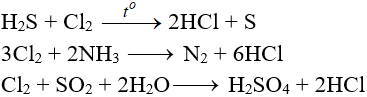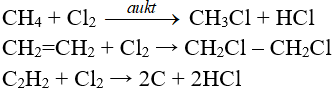Phương trình 3Cl2 + 6KOH to→5KCl + KClO3 + 3H2O
1. Phương trình phản ứng hóa học
3Cl2 + 6KOH to→5KCl + KClO3 + 3H2O
2. Cách thực hiện phản ứng
- Dẫn khí Cl2 vào ống nghiệm chứa dung dịch KOH đun nóng có một vài giọt phenolphtalein.
3. Hiện tượng nhận biết phản ứng
- Ban đầu dung dịch KOH có màu hồng, khi sục khí Cl2 vào thì màu hồng nhạt dần đến khi mất màu.
4. Điều kiện phản ứng
Dung dịch KOH nóng.
5. Mở rộng về tính chất hoá học của Cl2
5.1. Tác dụng với kim loại
Đa số kim loại và có to để khơi màu phản ứng tạo muối clorua (có hoá trị cao nhất )
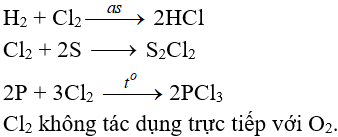
5.2. Tác dụng với phi kim
(Cần có nhiệt độ hoặc có ánh sáng)
5.3. Tác dụng với nước và dung dịch kiềm
- Cl2 tham gia phản ứng với vai trò vừa là chất ôxi hóa, vừa là chất khử.
a. Tác dụng với nuớc
Khi hoà tan vào nước, một phần Clo tác dụng (Thuận nghịch)
Cl20 + H2O → HCl + HClO (Axit hipoclorơ)
Axit hipoclorơ có tính oxy hoá mạnh, nó phá hửy các màu vì thế nước clo hay clo ẩm có tính tẩy màu do.
b. Tác dụng với dung dịch bazơ
5.4. Tác dụng với muối của các halogen khác
Cl2 + 2NaBr → 2NaCl + Br2
Cl2 + 2FeCl2 → 2FeCl3
3Cl2 + 6FeSO4 → 2Fe2(SO4)3 + 2FeCl3
Cl2 + 2KI → 2KCl + I2
5.5. Tác dụng với chất khử khác
5.6. Phản ứng thế, phản ứng cộng, phản ứng phân huỷ với một số hợp chất hữu cơ
6. Bạn có biết
- Nếu cho khí clo tác dụng với dung dịch kiềm nóng thì phản ứng không tạo ra muối hipoclorit mà tạo ra muối clorat.
- Kali clorat còn được điều chế bằng cách điện phân dung dịch KCl 25% ở nhiệt độ 70oC – 75oC.
7. Bài tập vận dụng
Bài 1: Cho khí Cl2 tác dụng với dung dịch KOH, đun nóng, thu được dung dịch chứa muối KCl và muối nào sau đây?
A. KClO
B. KClO3
C. KClO4
D. KClO2
Lời giải
Đáp án đúng là: B
Cho khí Cl2 tác dụng với dung dịch KOH, đun nóng, thu được dung dịch chứa muối KCl và muối KClO3
3Cl2 + 6KOH →t° 5KCl + KClO3 + 3H2O
Bài 2: Hòa tan khí Cl2 vào dung dịch KOH đặc nóng, dư thu được dung dịch chứa các chất tan thuộc dãy nào sau đây?
A. KCl, KClO3, Cl2.
B. KCl, KClO, KOH.
C. KCl, KClO3, KOH.
D. KCl, KClO3.
Lời giải
Đáp án đúng là: C
3Cl2 + 6KOH → 5KCl + KClO3 + 3H2O
Bài 3: Cho phản ứng: Cl2 + KOH → KCl + KClO3 + H2O
Tổng hệ số (nguyên, tối giản) của các chất trong phương trình là
A. 9
B. 18
C. 14
D. 15
Lời giải
Đáp án đúng là: B
3Cl2 + 6KOH → 5KCl + KClO3 + 3H2O
Bài 4: Tiến hành các thí nghiệm sau:
(a) Sục khí Cl2 vào dung dịch NaOH ở nhiệt độ thường.
(b) Hấp thụ hết 2 mol CO2 vào dung dịch chứa 3 mol NaOH.
(c) Cho KMnO4 vào dung dịch HCl dư.
(d) Cho hỗn hợp Fe3O4 vào dung dịch HCl dư.
(e) Cho CuO vào dung dịch HNO3
(f) Cho KHS vào dung dịch NaOH vừa đủ.
Số thí nghiệm thu được hai muối là
A. 4
B. 5
C. 3
D. 6
C
Lời giải
Đáp án đúng là: B
Các phản ứng hóa học xảy ra:
• (a) Cl2 + 2NaOH → NaCl + NaClO + H2O. (→ thỏa mãn).
• (b) 2CO2 + 3NaOH → 1Na2CO3 + 1NaHCO3 + 1H2O. (→ thỏa mãn).
• (c) 2KMnO4 + 16HCl → 2MnCl2 + 2KCl + 5Cl2 + 8H2O. (→ thỏa mãn).
• (d) Fe3O4 + 8HCl → 2FeCl3 + FeCl2 + 4H2O. (→ thỏa mãn)
• (e) CuO + 2HNO3 → Cu(NO3)2 + H2O (→ không thỏa mãn.!).
• (g) 2KHS + 2NaOH → Na2S + K2S + 2H2O.
⇒ có 5 thí nghiệm thỏa mãn thu được 2 muối → chọn đáp án C
Bài 5: Cho phản ứng: Cl2 + KOH → KCl + KClO3 + H2O.
Tỉ lệ giữa số nguyên clo đóng vai trò chất oxi hóa và số nguyên tử clo đóng vai trò chất khử trong phương trình hóa học trên là:
A. 1 : 3.
B. 3 : 1.
C. 5 : 1.
D. 1 : 5.
Lời giải
Đáp án đúng là: C
3Cl2 + 6KOH → 5KCl + KClO3 + 3H2O
⇒ Tỉ lệ giữa số nguyên clo đóng vai trò chất oxi hóa và số nguyên tử clo đóng vai trò chất khử trong phương trình hóa học trên là 5 : 1.
Xem thêm các phương trình hóa học khác:
Fe + Cl2 → FeCl3 | Fe ra FeCl3
SO2 + Cl2 + H2O → HCl + H2SO4 | SO2 ra H2SO4
H2S + Cl2 + H2O → H2SO4 + HCl | H2S ra H2SO4