Phản ứng FeS + H2SO4 → FeSO4 + H2S↑
1. Phương trình phản ứng FeS ra H2S
FeS + H2SO4 → FeSO4+ H2S↑
2. Điều kiện phản ứng FeS tác dụng H2SO4 loãng
Nhiệt độ thường
3. Hiện tượng phản ứng xảy ra
Cho FeS tác dụng H2SO4. Sau phản ứng có khí mùi trứng thối, mùi hắc thoát ra.
4. Bản chất của các chất tham gia phản ứng
4.1. Bản chất của FeS (Sắt (II) sunfua)
FeS có tính chất hoá học của muối tác dụng được với axit.
4.2. Bản chất của H2SO4 (Axit sunfuric)
H2SO4 là một axit mạnh có đầy đủ tính chất của một axit thường gặp tác dụng với muối tạo thành axit mới và muối mới.
5. Câu hỏi vận dụng liên quan
Câu 1. Cho FeS tác dụng với dung dịch H2SO4 loãng, thu được khí A; nếu dùng dung dịch H2SO4 đặc, nóng thì thu được khí B. Dẫn khí B vào dung dịch A thu được rắn C. Các chất A, B, C lần lượt là:
A. H2, H2S, S.
B. H2S, SO2, S.
C. H2, SO2, S.
D. O2, SO2, SO3.
Lời giải:
FeS + H2SO4 → FeSO4 + H2S (A)
2FeS + 10H2SO4 đặc → Fe2(SO4)3+ 9SO2↑ (B)+ 10H2O
2H2S + SO2 → 3S (C) + 2H2O
=> những khí tác dụng được với NaOH là: H2S (A), SO2 (B), S (C)
Câu 2. Cho các sơ đồ phản ứng sau:
(1) MnO2 + HCl → khí X;
(2) FeS + HCl → khí Y;
(3) Na2SO3 + HCl → khí Z;
(4) NH4HCO3 + NaOH (dư) → khí G.
Những khí sinh ra tác dụng được với NaOH là
A. Y, Z, G.
B. X, Y, G.
C. X, Z, G.
D. X, Y, Z.
Lời giải:
(1) MnO2 + 4HCl → MnCl2 + Cl2 (X) + 2H2O
(2) FeS + 2HCl → FeCl2 + H2S (Y)
(3) Na2SO3 + 2HCl → 2NaCl + SO2 (Z) + H2O
(4) NH4HCO3+ 2NaOH (dư) → Na2CO3 + NH3 (G) + 2H2O
=> những khí tác dụng được với NaOH là: Cl2 (X), H2S (Y), SO2 (Z)
Câu 3. Khi làm thí nghiệm với H2SO4 đặc, nóng thường sinh ra khí SO2. Để hạn chế tốt nhất khí SO2 thoát ra gây ô nhiễm môi trường, người ta nút ống nghiệm bằng bông tẩm dung dịch nào sau đây:
A. cồn.
B. muối ăn.
C. xút.
D. giấm ăn.
Lời giải:
Để hạn chế khí SO2 bay ra, người ta sử dụng bông tẩm xút vì xút có khả năng phản ứng:
SO2 + 2NaOH → Na2SO3 + H2O
Câu 4. Có các thí nghiệm sau:
(1) Sục khí SO2 vào nước brom.
(2) Nhúng thanh sắt vào dung dịch H2SO4 loãng, nguội.
(3) Sục khí SO2 vào dung dịch NaOH.
(4) Nhúng lá nhôm vào dung dịch H2SO4 đặc, nguội.
Số thí nghiệm xảy ra phản ứng hoá học là bao nhiêu?
A. 2.
B. 1.
C. 3.
D. 4.
Lời giải:
(1) Sục khí SO2 vào nước brom.
(2) Nhúng thanh sắt vào dung dịch H2SO4 loãng, nguội.
(3) Sục khí SO2 vào dung dịch NaOH.
Câu 5. Cho các trường hợp sau:
(1). SO3 tác dụng với dung dịch Ba(NO3)2.
(2). BaCl2 tác dụng với dung dịch H2SO4 loãng.
(3). Cho FeSO4 tác dụng với dung dịch NaOH
(4). Sục khí H2S vào dung dịch FeCl2
(5). Khí SO2 tác dụng với nước Cl2.
Số trường hợp tạo ra kết tủa là bao nhiêu?
A. 2
B. 3
C. 4
D. 5
Lời giải:
Câu 6. Cho khí H2S lội qua dung dịch CuSO4 thấy có kết tủa màu xám đen xuất hiện, chứng tỏ
A. Có phản ứng oxi hoá - khử xảy ra.
B. Có kết tủa CuS tạo thành, không tan trong axit mạnh.
C. Axit sunfuhiđric mạnh hơn axit sunfuric.
D. Axit sunfuric mạnh hơn axit sunfuhiđric.
Lời giải:
H2S + CuSO4 → CuS↓ (kết tủa đen) + H2SO4
=> Có kết tủa CuS tạo thành, không tan trong axit mạnh.
Câu 7. Để m gam bột sắt trong không khí, sau một thời gian thu được 3 gam hỗn hợp oxit X. Hoà tan hết 3 gam X cần vừa đủ 500 ml dung dịch HNO3 X (mol/l), thu được 0,56 lít khí NO (đktc) duy nhất và dung dịch không chứa NH4 . Giá trị của X là
A. 0,27.
B. 0,32.
C. 0,24.
D. 0,29.
Lời giải:
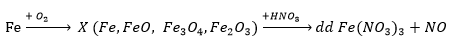
Gọi số mol Fe là a, số mol O2 phản ứng là b
Ta có: 56a + 32b = 3 (1)


Bảo toàn e: 3a = 4b + 0,075
Từ (1) và (2) ta có: a= 0,045; b = 0,015
nHNO3 = nNO3- trong muối nitrat + nN(trong sản phẩm khử)
0,5x = 3. 0,045 + 0,025
x = 0,32 mol
Xem thêm các phương trình hóa học khác:
FeS + HCl → FeCl2 + H2S | FeS ra FeCl2
FeS + H2SO4 → FeSO4 + H2S | FeS ra FeSO4
FeO + H2SO4 → Fe2(SO4)3 + SO2 + H2O | FeO ra Fe2(SO4)3
FeS2 + H2SO4 → Fe2(SO4)3 + SO2 + H2O | FeS2 ra Fe2(SO4)3
Fe(OH)2 + H2SO4 → Fe2(SO4)3 + H2S + H2O | Fe(OH)2 ra Fe2(SO4)3




