Phản ứng FeS + H2SO4 → Fe2(SO4)3 + SO2↑ + H2O
1. Phương trình phản ứng FeS tác dụng với dung dịch H2SO4 đặc nóng
2FeS + 10H2SO4 → Fe2(SO4)3+ 9SO2↑ + 10H2O
2. Điều kiện xảy ra giữa FeS và H2SO4 đặc nóng
Nhiệt độ thường, dung dịch H2SO4 đặc nóng.
3. Bản chất của các chất tham gia phản ứng
3.1. Bản chất của FeS (Sắt (II) sunfua)
- Trong phản ứng trên FeS là chất khử.
- FeS có tính chất hoá học của muối tác dụng được với axit.
3.2. Bản chất của H2SO4 (Axit sunfuric)
- Trong phản ứng trên H2SO4 là chất oxi hoá.
- H2SO4 là một axit mạnh có đầy đủ tính chất của một axit thường gặp tác dụng với muối tạo thành axit mới và muối mới.
4. Tính chất hóa học của H2SO4
Ở trạng thái loãng là một axit mạnh, ở trạng thái đặc là một chất ôxi hóa mạnh.
4.1. Ở dạng loãng là axít mạnh:
Làm đỏ quì tím, tác dụng kim loại(trước H2) giải phóng H2, tác dụng bazơ, oxit bazơ và nhiều muối.
H2SO4 làm quỳ tím hóa đỏ
Fe + H2SO4 → FeSO4 + H2
NaOH + H2SO4 → NaHSO4 + H2O
CuO + H2SO4 → CuSO4 + H2O
BaCl2 + H2SO4 → BaSO4 + 2HCl
Na2 CO3 + H2SO4 → Na2SO4 + H2O + CO2
4.2. Ở dạng đặc là một chất ôxi hóa mạnh
Tác dụng với kim loại: oxi hoá hầu hết các kim loại (trừ Au và Pt) tạo muối hoá trị cao và thường giải phóng SO2 (có thể H2 S, S nếu kim loại khử mạnh như Mg ).
2 Fe + 6H2SO4 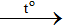
Cu + 2H2SO4 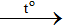
Al, Fe, Cr không tác dụng với H2SO4 đặc nguội, vì kim loại bị thụ động hóa.
a) Tác dụng với phi kim ( tác dụng với các phi kim ở dạng rắn, to) tạo hợp chất của phim kim ứng với số oxh cao nhất.
C + 2H2SO4 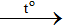
S + 2H2SO4 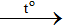
b) Tác dụng với một số chất có tính khử
FeO + H2SO4 
HBr + H2SO4 
Hút nươc của 1 số chất hữu cơ:
C12H22O11 + H2SO4(đ) → 12C + H2SO4.11H2O
c) Ứng dụng
- Axit sunfuric là hoá chất hàng đầu được dùng trong nhiều ngành sản xuất. Hàng năm, các nước trên thế giới sản xuất khoảng 160 triệu tấn H2SO4.
- Axit sunfuric được dùng để sản xuất phân bón, thuốc trừ sâu, chất giặt rửa tổng hợp, tơ sợi hoá học, chất dẻo, sơn màu, phẩm nhuộm, dược phẩm, chế biến dầu mỏ...
5. Câu hỏi vận dụng liên quan
Câu 1. Cho 2,24 gam Fe tác dụng với oxi, thu được 3,04 gam hỗn hợp X gồm 2 oxit. Để hoà tan hết X cần thể tích dung dịch HCl 2M là
A. 25 ml.
B. 50 ml.
C. 100 ml.
D. 150 ml.
Lời giải:
Áp dụng bảo toàn nguyên tố (mol nguyên tử)
Oxit + HCl → muối clorua + H2O
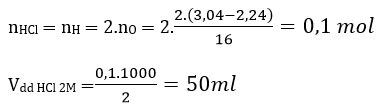
Câu 2. Cho một lượng dư bột sắt Fe phản ứng với dung dịch axit clohiđric HCl, sau khi phản ứng xảy ra thu được các sản phẩm là:
A. Fe dư, FeCl2, H2.
B. FeCl2, H2.
C. Fe dư, FeCl2.
D. FeCl2.
Lời giải:
Fe dư + 2HCl → FeCl2 + H2↑
=> Sản phẩm gồm: FeCl2, H2 và Fe dư
Câu 3. Cho m gam bột Fe vào 800 ml dung dịch hỗn hợp gồm Cu(NO3)2 0,2M và H2SO4 0,25M. Sau khi các phản ứng xảy ra hoàn toàn, thu được 0,6m gam hỗn hợp bột kim loại và V lít khí NO (sản phẩm khử duy nhất của N+5, ở đktc). Giá trị của m và V lần lượt là:
A. 10,8 và 4,48.
B. 10,8 và 2,24.
C. 17,8 và 4,48.
D. 17,8 và 2,24.
Lời giải:
nCu(NO3)2 = 0,8.0,2 = 0,16 mol
nH2SO4 = 0,8.0,25 = 0,2 mol
Do sau phản ứng còn dư hỗn hợp bột kim loại ⇒ Fe còn dư, Cu2+ hết, muối Fe2+

V = 0,1.22,4 – 2,24 lít
m – (0,15 + 0,16).56 + 0,16.64 = 0,6m
m = 17,8
Câu 4. Cho khí H2S lội qua dung dịch CuSO4 thấy có kết tủa màu xám đen xuất hiện, chứng tỏ
A. Có phản ứng oxi hoá - khử xảy ra.
B. Có kết tủa CuS tạo thành, không tan trong axit mạnh.
C. Axit sunfuhiđric mạnh hơn axit sunfuric.
D. Axit sunfuric mạnh hơn axit sunfuhiđric.
Lời giải:
H2S + CuSO4 → CuS↓ (kết tủa đen) + H2SO4
=> Có kết tủa CuS tạo thành, không tan trong axit mạnh.
Câu 5. Để m gam bột sắt trong không khí, sau một thời gian thu được 3 gam hỗn hợp oxit X. Hoà tan hết 3 gam X cần vừa đủ 500 ml dung dịch HNO3 X (mol/l), thu được 0,56 lít khí NO (đktc) duy nhất và dung dịch không chứa NH4 . Giá trị của X là
A. 0,27.
B. 0,32.
C. 0,24.
D. 0,29.
Lời giải:
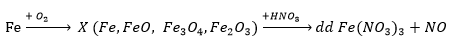
Gọi số mol Fe là a, số mol O2 phản ứng là b
Ta có: 56a + 32b = 3 (1)


Bảo toàn e: 3a = 4b + 0,075
Từ (1) và (2) ta có: a= 0,045; b = 0,015
nHNO3 = nNO3- trong muối nitrat + nN(trong sản phẩm khử)
0,5x = 3. 0,045 + 0,025
x = 0,32 mol
Câu 6. Cho 11,36 gam hồn hợp gồm Fe, FeO, Fe2O3, Fe3O4 phản ứng hết với dung dịch HNO3 loãng (dư), thu được 1,344 lít khí NO (sản phẩm khử duy nhất, ở đktc) và dung dịch X. Dung dịch X có thể hoà tan tối đa 12,88 gam Fe. Số mol HNO3 có trong dung dịch ban đầu là
A. 0,88.
B.0,64.
C. 0,94.
D. 1,04.
Lời giải:
Gọi số mol Fe là a, số mol O là b, ta được 56a+16b = 11,36 (1)
(Fe + O) → (Fe, FeO, Fe2O3, Fe3O4) −+HNO3→ dd X (Fe3+,H+, NO2- + NO

Ta có: 3a = 2b + 0,18 (2)
Giải hệ (1) và (2) ta được a = 0,16, b = 0,15
Dung dịch X hoà tan Fe theo 2 phản ứng:
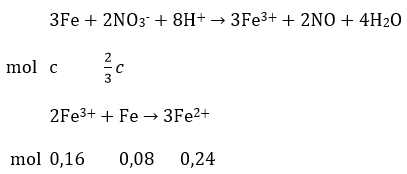
Ta có: c + 0,08 = 0,23mol ⇒ c= 0,15 mol
2c/3=0,10 mol
Bảo toàn nguyên tố N: nHNO3 bđ= nNO3- + nNO = 2nFe2+ + nNO(1) + nNO(2)
nHNO3 = 2.(0,15 + 0,24) + 0,06 + 0,10 = 0,94 mol
Câu 7. Để a gam bột Fe trong không khí một thời gian, thu được 9,6 gam chất rắn X. Hoà tan hoàn toàn X trong dung dịch HNO3 loãng (dư), thu được dung dịch Y và khí NO (sản phẩm khử duy nhất của ). Cho dung dịch NaOH dư vào Y, thu được kết tủa, Lọc kết tủa rồi nung ở nhiệt độ cao đến khối lượng không đổi, thu được 12,0 gam chất rắn. Số mol HNO3 đã phản ứng là:
A. 0,75.
B. 0,65.
C. 0,55.
D. 0,45.
Lời giải:
(a gam Fe + O) → 9,6 gam X (Fe, FeO, Fe2O3, Fe3O4)
−+HNO3→ dd Y (Fe3+,H+,NO33- )+NO)
Y + NaOH(dư) → Fe(OH)3 → Fe2O3 (12 gam)
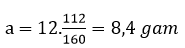
mO = 9,6 – 8,4 = 1,2 gam
⇒ nFe = 0,15 mol; nO = 0,075 mol
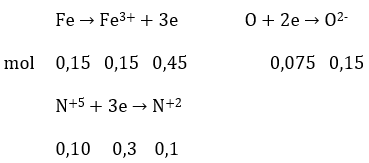
nHNO3 pứ = 0,45 + 0,1 = 0,55 mol
Xem thêm các phương trình hóa học khác:
FeS + HCl → FeCl2 + H2S | FeS ra FeCl2
FeS + H2SO4 → FeSO4 + H2S | FeS ra FeSO4
FeO + H2SO4 → Fe2(SO4)3 + SO2 + H2O | FeO ra Fe2(SO4)3
FeS2 + H2SO4 → Fe2(SO4)3 + SO2 + H2O | FeS2 ra Fe2(SO4)3
Fe(OH)2 + H2SO4 → Fe2(SO4)3 + H2S + H2O | Fe(OH)2 ra Fe2(SO4)3




