Từ các nguyên tử có thể tạo ra các ion bằng cách thêm hoặc bớt electron từ nguyên tử đó
71
29/01/2024
Bài 5.14 trang 15 SBT Hóa học 10: Từ các nguyên tử có thể tạo ra các ion bằng cách thêm hoặc bớt electron từ nguyên tử đó.
a) Oxygen là nguyên tố chiếm tỉ lệ phần trăm khối lượng cao nhất trong cơ thể con người (khoảng 65%). Hãy viết cấu hình electron của O và O2- (Z = 8). Cho biết để hình thành ion O2-, nguyên tử O sẽ nhận thêm electron vào orbital nào. Xác định số electron độc thân trong nguyên tử và ion này.
b) Nhôm (aluminium) được sử dụng phổ biến trong đời sống (chế tạo dụng cụ nhà bếp, cửa, …) cũng như công nghiệp (chế tạo một số bộ phận của máy bay). Hãy biểu diễn cấu hình electron của Al và ion Al3+ (Z = 13) dưới dạng ô orbital. Cho biết để tạo thành ion Al3+, nguyên tử Al sẽ mất đi electron từ orbital nào. Xác định số electron độc thân trong các nguyên tử và ion này.
Trả lời
a) Nguyên tử O (Z = 8) có cấu hình electron: 1s22s22p4
Biểu diễn dưới dạng ô AO:
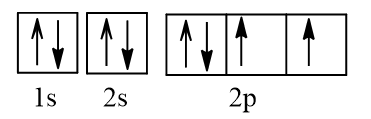
Vậy nguyên tử O có 2 electron độc thân.
O nhận 2 electron vào AO 2p hình thành nên ion O2- có cấu hình electron:
1s22s22p6.
Biểu diễn dưới dạng ô AO:
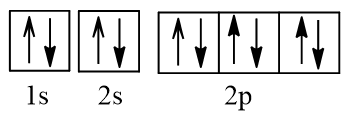
Ion O2- không có electron độc thân nào.
b) Nguyên tử Al (Z = 13) có cấu hình electron: 1s22s22p63s23p1.
Biểu diễn dưới dạng ô orbital:
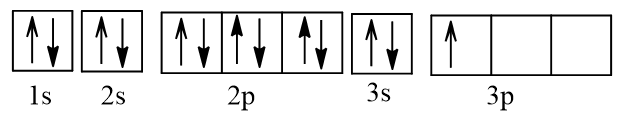
Vậy Al có 1 electron độc thân.
Nguyên tử Al nhường đi 3 electron từ các orbital 3p, 3s để tạo thành ion Al3+ có cấu hình electron: 1s22s22p6.
Biểu diễn dưới dạng ô orbital:
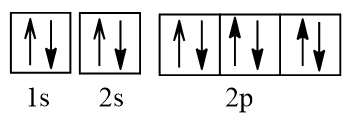
Vậy ion Al3+ không có electron độc thân nào.
Xem thêm các bài giải sách bài tập Vật Lí lớp 10 sách Kết nối tri thức với cuộc sống hay, chi tiết khác
Bài 3: Nguyên tố hóa học
Bài 4: Cấu trúc lớp vỏ electron của nguyên tử
Bài 5: Lớp, phân lớp và cấu hình electron
Bài 6: Cấu tạo của bảng tuần hoàn các nguyên tố hóa học
Bài 7: Xu hướng biến đổi một số tính chất của đơn chất, biến đổi thành phần và tính chất của hợp chất trong một chu kì và trong một nhóm
Bài 8: Định luật tuần hoàn và ý nghĩa của bảng tuần hoàn các nguyên tố hóa học




