Trong một bình kín xảy ra cân bằng hoá học sau: H2(g)+I2(g) phản ứng ở trạng thái cân bằng tạo thành 2HI
737
03/10/2023
Bài 1.13 trang 8 SBT Hóa 11: Trong một bình kín xảy ra cân bằng hoá học sau:
H2( g)+I2( g)⇌2HI(g)
Cho 1 mol H2 và 1 mol I2 vào bình kín, dung tích 2 lít. Lượng HI tạo thành theo thời gian được biểu diễn bằng đồ thị sau:
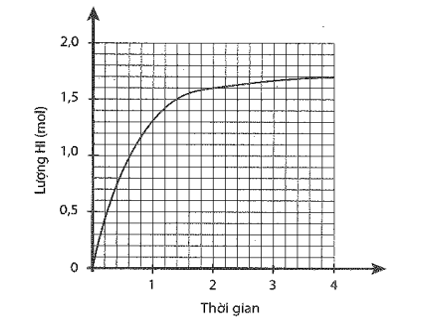
a) Xác định nồng độ các chất ở thời điểm cân bằng.
b) Tính hằng số cân bằng KC.
c) Tính hiệu suất của phản ứng.
Trả lời
a) Số mol HI tại thời điểm cân bằng là 1,7 mol ⇒ Số mol H2 và I2 phản ứng là 0,85 mol. Nồng độ các chất tại thời điểm cân bằng:
[H2] = [I2] = 1−0,852= 0,075 (mol/L)
[HI] = 1,72=0,85 (mol/L)
b) H2(g) + I2(g) ⇌ 2HI(g)
Lượng chất ban đầu : 1 1 0 (mol)
Lượng chất phản ứng: 0,85 0,85 1,7 (mol)
Nồng độ tại cân bằng: 0,152 0,152 1,72 (mol/L)
Hằng số cân bằng (Kc): Kc=(1,72)20,152.0,152≈128,444
c) Hiệu suất phản ứng: H%= 85%
Xem thêm lời giải bài tập SBT Hoá học lớp 11 Kết nối tri thức hay, chi tiết khác:
Bài 1: Khái niệm về cân bằng hoá học
Bài 2: Cân bằng trong dung dịch nước
Bài 3: Ôn tập chương 1
Bài 4: Nitrogen
Bài 5: Ammonia. Muối ammonium
Bài 6: Một số hợp chất của nitrogen với oxygen

