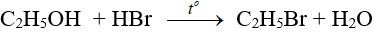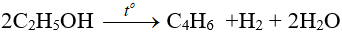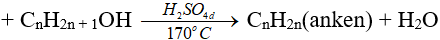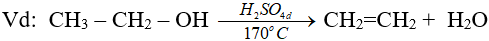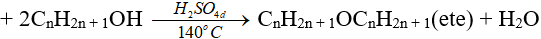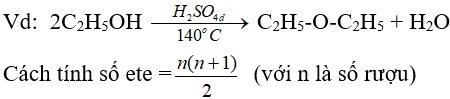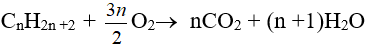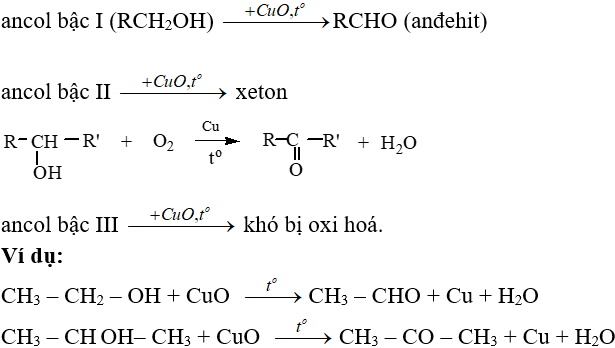C3H5(OH)3 + Cu(OH)2 → [C3H5(OH)2O]2Cu + H2O
1. Phương trình phản ứng C3H5(OH)3 tác dụng với Cu(OH)2
2C3H5(OH)3 + Cu(OH)2 → [C3H5(OH)2O]2Cu + 2H2O
2. Điều kiện phản ứng xảy ra giữa glixerol và Cu(OH)2
Nhiệt độ thường.
3. Bản chất của các chất tham gia phản ứng
3.1. Bản chất của C3H5(OH)3 (Glixerol)
C3H5(OH)3 là ancol đa chức có các nhóm -OH cạnh nhau tham gia được phản ứng thế H của nhóm OH. Khi glixerol tác dụng với đồng hidroxit tạo thành dung dịch màu xanh lam trong suốt. (Chú ý: Đây là phản ứng đặc trưng dùng để nhận biết dung dịch glixerol và các ancol đa chức)
3.2. Bản chất của Cu(OH)2 (Đồng hidroxit)
Cu(OH)2 có đầy đủ tính chất hoá học của hidroxit không tan tạo phức chất, hòa tan trong ancol đa chức có nhiều nhóm –OH liền kề.
4. Cách tiến hành thí nghiệm khi cho Glixerol tác dụng với Cu(OH)2
- Cho vào ống nghiệm 3 – 4 giọt dung dịch CuSO4 2% và 2 – 3 giọt dung dịch NaOH 10%, lắc nhẹ.
- Tiếp tục nhỏ 2 -3 giọt glixerol vào ống nghiệm.
- Lắc nhẹ ống nghiệm.
5. Hiện tượng phản ứng khi cho Glixerol tác dụng với Cu(OH)2
Cho dung dịch NaOH vào dung dịch CuSO4 thấy xuất hiện kết tủa màu xanh, sau đó cho dung dịch glixerol vào thấy tạo phức màu xanh thẫm.
6. Mở rộng tính chất hóa học của Ancol
6.1. Phản ứng thế nguyên tử hiđro của nhóm OH ancol (phản ứng đặc trưng của Ancol)
- Tính chất chung của ancol:
2ROH + Na → 2RONa + H2↑
- Tính chất đặc trưng của glixerol:
2C3H5(OH)3 + Cu(OH)2 → [C3H5(OH)2O]2Cu + H2O
(ĐK: muốn tác dụng với Cu(OH)2 phải có 2 nhóm -OH trở lên liền kề nhau)
→ Phản ứng này dùng để phân biệt ancol đơn chức với ancol đa chức có 2 nhóm OH cạnh nhau trong phân tử.
6.2. Phản ứng thế nhóm OH
- Phản ứng với axit vô cơ:
- Phản ứng tạo dien: dùng sản xuất cao su buna.
(ĐK: phải có xúc tác là Al2O3 + MgO hoặc ZnO/500ºC)
6.3. Phản ứng tách nước (phản ứng đề hidrat hoá)
Chú ý:
(ĐK n ≥ 2, theo quy tắc Zai-xép)
(ancol bậc càng cao thì càng dễ khử nước tạo anken)
(phải là rượu no, đơn chức)
(ancol bậc càng thấp thì càng dễ khử nước tạo ete)
6.4. Phản ứng oxi hoá
- Phản ứng oxi hoá hoàn toàn:
- Phản ứng oxi hoá không hoàn toàn:
7. Bài tập vận dụng
Câu 1. Chọn nhận xét sai
A. Glixerol hòa tan Cu(OH)2 thu được phức đồng (II) glixerat màu xanh lam.
B. Cho hỗn hợp but-1-en và but-2-en cộng H2O/H+ thu được tối đa 3 ancol
C. Cho CH3OH qua H2SO4 đặc , 1400 C thu được sản phẩm hữu cơ Y thì luôn có dY/X >1
D. Từ tinh bột bằng phương pháp sinh hóa ta điều chế được ancol etylic
Lời giải:
Đáp án: B
Sản phẩm chỉ thu được tối đa 2 ancol
Do but – 2- en có cấu tạo đối xứng. Sản phẩm trùng với but – 1 – en
Câu 2. Trong số các chất sau: axit axetic, glixerol, glucozơ, ancol etylic. Số chất hòa tan được Cu(OH)2 ở nhiệt độ thường là:
A. 3
B. 5
C. 1
D. 4
Lời giải:
Đáp án: A
Trong số các chất sau: axit axetic, glixerol, glucozơ, ancol etylic. Số chất hòa tan được Cu(OH)2 ở nhiệt độ thường là 3 chất.
Câu 3. Chọn các nhận định đúng
A.Lipit là chất béo
B.Lipit là tên gọi chung của dầu, mỡ động vật thực vật
C.Lipit là este của glixerol và các axit béo
D.Lipit là những hợp chất hữu cơ có trong tế bào sống, không tan trong nước nhưng tan trong dung môi hữu cơ. Lipit bao gồm chất béo, sáp, steroid, photpholipit
Lời giải:
Đáp án: D
Giải thích:
Lipit là những hợp chất hữu cơ có trong tế bào sống, không tan trong nước nhưng tan trong dung môi hữu cơ. Lipit bao gồm chất béo, sáp, steroid, photpholipit
Câu 4. Cho các nhận định sau:
(1) 1 mol chất béo phản ứng tối đa với 3 mol NaOH.
(2) Chất béo là trieste của glixerol và axit béo gọi chung là steroit.
(3) Chất béo no ở điều kiện thường là chất rắn.
(4) Chất béo triolein phản ứng tối đa 3 mol H2.
(5) Muối natri hoặc kali của các axit béo được dùng làm xà phòng.
Số nhận định đúng là
A. 2
B. 3
C. 4
D. 5
Lời giải:
Đáp án: C
Giải thích:
(1) đúng
(2) sai vì chất béo gọi chung là triglixerit hoặc triaxylglixerol
(3) đúng
(4) đúng, vì triolein có 3 liên kết C=C
(5) đúng
⟹ 4 phát biểu đúng
Câu 5. Cho các nhận định sau:
(1) Chất béo là trieste của glixerol và axit béo.
(2) Các chất béo nhẹ hơn nước, không tan trong nước nhưng tan tốt trong anilin.
(3) Xà phòng là muối natri hoặc kali của các axit cacboxylic.
(4) Thủy phân chất béo trong môi trường axit thu được glixerol và xà phòng.
(5) Chất béo lỏng thành phần chủ yếu chứa các gốc axit béo no.
(6) Phản ứng của chất béo với dung dịch kiềm gọi là phản ứng xà phòng hóa.
(7) Các este thường là các chất lỏng, dễ bay hơi.
Số nhận định đúng là
A. 3
B. 6
C. 5
D. 4
Lời giải:
Đáp án: D
Giải thích:
Các mệnh đề đúng: 1, 2, 6, 7.
Mệnh đề 3: Xà phòng là muối natri hoặc kali của các axit béo
Mệnh đề 4: Thủy phân chất béo trong môi trường kiềm thu được glixerol và xà phòng.
Mệnh đề 5: Chất béo lỏng thành phần chủ yếu chứa các gốc axit béo không no
Câu 6. Dãy gồm các dung dịch đều tác dụng với Cu(OH)2
A. Axit axetic, glixerol, mantozo.
B. natri axetat, saccarozo, mantozo.
C. Glucozo, glixerol, ancol etylic.
D. Ancol etylic, saccarozo, axit axetic.
Lời giải:
Đáp án: A
Câu 7. Dãy gồm các dung dịch đều tác dụng với Cu(OH)2 ở nhiệt độ thường là
A. glixerol, glucozơ, frutozơ, saccarozơ.
B. glixerol, glucozơ, anđehit axetic, etilenglicol.
C. ancol etylic, glucozơ, fructozơ, glixerol.
D. saccarozơ, glucozơ, anđehit axetic, glixerol.
Lời giải:
Đáp án: A
Câu 8. Cho các chất: CH3COOH, C2H4(OH)2, C3H5(OH)3, C2H5OH. Số chất phản ứng đi Cu(OH)2là
A. 4
B. 3
C. 2
D. 1
Lời giải:
Đáp án: B
Câu 9. Dãy gồm các chất đều tác dụng được với glixerol là (các chất xúc tác có đủ):
A. Mg, Cu(OH)2; HBr; HNO3.
B. Na, MgO, HBr, HNO3, CH3COOH.
C. Na, NaOH, Cu(OH)2, HBr, HNO3.
D. Na, CuO, CH3COOH, HNO3.
Lời giải:
Đáp án: D
Giải thích:
Đáp án A: Mg không phản ứng
Đáp án B: MgO không phản ứng
Đáp án C: NaOH không phản ứng
D. Na, CuO, CH3COOH, HNO3.
2C3H5(OH)3 + 6Na → 2C3H5(ONa)3 + 3H2
2C3H5(OH)3 + 2CuO → 3CH3COOH + 2Cu + 2H2O
5CH3COOH + 6C3H5(OH)3→ 4(CH3COO)2C3H5+ 12H2O
C3H5(OH)3 + 3HNO3 → C3H5(NO3)3 + 3H2O
Câu 10. Dùng thuốc thử AgNO3/NH3 đun nóng có thể phân biệt được cặp chất nào sau đây?
A. Glucozơ và mantozơ
B. Glucozơ và glixerol
C. Saccarozơ và glixerol
D. Glucozơ và fructozơ
Lời giải:
Đáp án: B
Giải thích:
Glucozơ có phản ứng tạo kết tủa bạc, glixerol không phản ứng.
Phương trình hóa học:
CH2OH(CHOH)4CHO + 2AgNO3 + 3NH3 + H2O → CH2OH(CHOH)4COONH4 + 2Ag↓ + 2NH4NO3.
Câu 11. Nung 6,58 gam Cu(NO3)2 trong bình kín không chứa không khí, sau một thời gian thu được 4,96 gam chất rắn và hỗn hợp khí X. Hấp thụ hoàn toàn X vào nước để được 300 ml dung dịch Y. Dung dịch Y có pH bằng
A. 2.
B. 3.
C. 4.
D. 1 .
Lời giải:
Đáp án: D
2Cu(NO3)2 → 2CuO + 4NO2 (4x) + O2 (x mol)
Áp dụng định luật bảo toàn khối lượng có:
mchất rắn ban đầu = mchất rắn sau + mkhí
→ 6,58 = 4,96 + 46.4x + 32x → x = 0,0075 mol
Dẫn khí X vào nước
O2 (0,0075) + 4NO2 (0,03) + 2H2O → 4HNO3 (0,03 mol)
CM (HNO3) = 0,03 : 0,3 = 0,1 → pH = 1.
Câu 12. Nhúng một thanh sắt nặng 100 gam vào 100 ml dung dịch hỗn hợp gồm Cu(NO3)2 0,2M và AgNO3 0,2M. Sau một thời gian lấy thanh kim loại ra, rửa sạch làm khô cân được 101,72 gam (giả thiết các kim loại tạo thành đều bám hết vào thanh sắt). Khối lượng sắt đã phản ứng là
A. 2,16 gam.
B. 0,84 gam.
C. 1,72 gam.
D. 1,40 gam.
Lời giải:
Đáp án: D
Fe (0,01) + 2Ag+ → Fe2+ + 2Ag (0,02 mol) (1)
mtăng (1) = 0,02.108 – 0,01.56 = 1,6 gam
Theo bài ra mKL tăng = 101,72 – 100 = 1,72 gam.
Tiếp tục có phản ứng:
Fe (a) + Cu2+ → Fe2+ (a mol) + Cu
mtăng (2) = 64a – 56a = 1,72 – 1,6 → a = 0,015 mol
→ mFe = (0,01 + 0,015).56 = 1,4 gam.
Câu 13. Nhận định nào sau đây là sai?
A. Đồng dẻo, dễ kéo sợi .
B. Đồng là kim loại có màu đen.
C. Đồng có thể dát mỏng hơn giấy viết từ 5 đến 6 lần.
D. Đồng dẫn nhiệt, điện tốt.
Lời giải:
Đáp án: B
Đồng là kim loại có màu đỏ.
Xem thêm các phương trình hóa học khác nhau:
Cu + HNO3 → Cu(NO3)2 + N2O + H2O | Cu ra Cu(NO3)2
Cu + H2SO4 (đặc, nóng) → CuSO4 + SO2 + H2O
Cu + AgNO3 → Cu(NO3)2 + Ag | Cu ra Cu(NO3)2
NH3 + CuO → Cu + N2 + H2O | NH3 ra N2
C3H5(OH)3 + Cu(OH)2 → [C3H5(OH)2O]2Cu + H2O | C3H5(OH)3 ra Phức đồng (II) glixerat

![C3H5(OH)3 + Cu(OH)2 → [C3H5(OH)2O]2Cu + H2O | C3H5(OH)3 ra Phức đồng (II) glixerat](https://1900.edu.vn/storage/uploads/images/banners/19312/UZHILyy1Wp3BUFVYyIrFV7iXKElm8alCATTXjLOD_903x430.png)