Phản ứng AlCl3 + NaOH → NaAlO2 + NaCl + H2O
1. Phương trình phản ứng NaOH ra NaAlO2
AlCl3 + 4NaOH → NaAlO2 + 3NaCl + 2H2O
2. Điều kiện phản ứng xảy ra
Cho từ từ dung dịch NaOH đến dư vào dung dịch AlCl3.
3. Cho NaOH dư vào dung dịch AlCl3 có hiện tượng
Ban đầu xuất hiện kết tủa keo trắng nhôm hidroxit Al(OH)3 trong dung dịch, và một lúc sau kết tủa này tan dần trong dung dịch.
Lúc đầu AlCl3 dư nên: AlCl3 + 3NaOH → Al(OH)3 ↓ + 3NaCl
Sau đó khi NaOH dư: Al(OH)3 + NaOH → NaAlO2 + 2H2O
4. Bản chất của các chất tham gia phản ứng
4.1. Bản chất của AlCl3 (Nhôm clorua)
AlCl3 mang đầy đủ tính chất hoá học của muối nên tác dụng được với dung dịch bazo.
4.2. Bản chất của NaOH (Natri hidroxit)
NaOH là một bazo mạnh nên tác dụng được với muối AlCl3.
5. Tính chất hóa học của AlCl3
Mang đầy đủ tính chất hóa học của muối
Tác dụng với dung dịch bazo:
AlCl3 + NaOH(vừa đủ) → NaCl + Al(OH)3
Tác dụng với dung dịch muối khác:
AlCl3 + AgNO3 → AgCl↓ + NaNO3
Phản ứng với kim loại mạnh hơn:
3Mg + 2AlCl3 → 3MgCl2 + 2Al
6. Bài tập vận dụng liên quan
Câu 1. Cho từ từ dung dịch NaOH đến dư vào dung dịch AlCl3 thấy xuất hiện
A. kết tủa màu xanh.
B. kết tủa keo trắng, sau đó kết tủa không tan.
C. kết tủa keo trắng, sau đó kết tủa tan dần.
D. kết tủa màu nâu đỏ.
Lời giải:
Lúc đầu AlCl3 dư nên : AlCl3 + 3NaOH 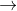 Al(OH)3 ↓ + 3NaCl
Al(OH)3 ↓ + 3NaCl
Sau đó khi NaOH dư : Al(OH)3 + NaOH 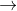 NaAlO2 + 2H2O
NaAlO2 + 2H2O
Câu 2. Cho 100 ml dung dịch AlCl3 0,15M vào 250 ml dung dịch NaOH 0,2M, sau khi phản ứng xảy ra hoàn toàn, thu được m gam kết tủa. Giá trị của m là
A. 1,56
B. 0,78
C. 1,17
D. 1,30
Lời giải:
nAlCl3=0,015mol→nAl3+=0,015mol
nNaOH=0,05mol→nOH−=0,05mol
Phương trình hóa học:
Al3++3OH−→Al0,015→0,045→0,015
Sau phản ứng, OH- dư: 0,05 – 0,045 = 0,005 mol
Al+OH−→AlO−2+2H2O0,005←0,005
Sau phản ứng: nAl(OH)3=0,015−0,005=0,01mol
→ mkết tủa = 0,01.78 = 0,78 gam
Câu 3. Cho từ từ đến hết 100 ml dung dịch NaOH 1,5M vào 50 ml dung dịch AlCl3 1,5M, sau khi các phản ứng xảy ra hoàn toàn thu được m gam kết tủa. Giá trị của m là
A. 12,4.
B. 7,8.
C. 15,6.
D. 3,9.
Lời giải:
Đáp án: D
nNaOH=0,15mol→nOH−=0,15mol
nAlCl3=0,075mol→nAl3+=0,075mol
Xét tỉ lệ nOH−nAl3+=2<3
Khi đó nAl(OH)3=nOH−3=0,153=0,05mol→m=mAl(OH)3=0,05.78=3,9gam
Câu 4. Dùng hóa chất nào sau đây để phân biệt Zn(NO3)2 và Al(NO3)3 ?
A.Dung dịch NaOH
B.Dung dịch Ba(OH)2
C.Dung dịch NH3
D.Dung dịch nước vôi trong
Lời giải:
Đáp án: C
Khi cho NH3 vào 2 dung dịch cả 2 dung dịch đều xuất hiện kết tủa hiđroxit, nhưng Zn(OH)2 tạo thành có khả năng tạo phức với NH3 nên kết tủa lại tan, còn với Al(OH)3 không tan trong NH3
Al(NO3)3 + 3NH3 + 3H2O → Al(OH)3↓ + 3NH4NO3
Zn(NO3)2 + 2NH3 + 2H2O → Zn(OH)2↓ + 2NH4NO3
Dung dịch amoniac có khả năng hòa tan hiđroxit hay muối ít tan của một số kim loại (Ag, Cu, Zn), tạo thành các dung dịch phức chất.
Câu 5. Hiện tượng nào xảy ra khi cho từ từ đến dư dung dịch NaOH vào dung dịch AlCl3?
A. Ban đầu không thấy hiện tượng, sau đó kết tủa xuất hiện
B. Xuất hiện kết tủa keo trắng ngay lập tức, sau đó kết tủa tan dần
C. Ban đầu không thấy hiện tượng, sau đó kết tủa xuất hiện, rồi tan dần.
D. Xuất hiện kết tủa keo trắng ngay lập tức và không tan.
Lời giải:
Đáp án: B
Ban đầu có kết tủa keo trắng ngay lập tức
3NaOH + AlCl3 → Al(OH)3↓ + 3NaCl
Khi NaOH dư, kết tủa tan dần
NaOH + Al(OH)3 → NaAlO2 + 2H2O
Câu 6. Để phân biệt dung dịch AlCl3 và dung dịch KCl ta dùng dung dịch
A.NaOH.
B. HCl.
C.NaNO3
D. H2SO4.
Lời giải:
Đáp án: A
Trích mẫu thử của hai dung dịch ra hai ống nghiệm có đánh số.
Nhỏ NaOH dư vào từng ống nghiệm
- Xuất hiện kết tủa trắng sau đó kết tủa tan: AlCl3
AlCl3 + 3NaOH → Al(OH)3↓ + 3NaCl
Al(OH)3 + NaOH → NaAlO2 + 2H2O
- Không có hiện tượng gì: KCl
Câu 7. Cho hỗn hợp X gồm Al và Al2O3 có tỉ lệ khối lượng tương ứng là 0,18 : 1,02. Cho X tan trong dung dịch NaOH vừa đủ thu được dung dịch Y và 0,672 lít khí H2 (đktc). Cho Y tác dụng với 200 ml dung dịch HCl được kết tủa Z. Nung Z ở nhiệt độ cao đến khối lượng không đổi được 3,57g chất rắn. Nồng độ mol của dung dịch HCl là
A. 0,35M hoặc 0,45M.
B. 0,07M hoặc 0,11M.
C. 0,07M hoặc 0,09M.
D. 0,35M hoặc 0,55M.
Lời giải:
Đáp án: D
nH2= 0,03
Bảo toàn electron: 3.nAl = 2.nH2
→ nAl = 0,02 → mAl = 0,54g
Al và Al2O3 có tỉ lệ khối lượng tương ứng là 0,18 : 1,02
→mAl2O3= 0,540,18.1,02=3,06g
→nAl2O3bđ = 0,03 mol
Bảo toàn nguyên tố Al →nNaAlO2 = nAl + 2. nAl2O3 bđ = 0,08 mol
nAl2O3thu được = 3,57 : 102 = 0,035 mol
nAl(OH)3= 0,07 mol
Trường hợp 1:
NaAlO2 + HCl + H2O → Al(OH)3 + NaCl
nHCl = nAl(OH)3 = 0,07 mol
→ CM HCl = 0,070,2= 0,35M
Trường hợp 2:
NaAlO2+HCl+H2O→Al(OH)3+NaCl0,07←0,07←0,07mol
NaAlO2+4HCl→AlCl3+NaCl+2H2O(0,08−0,07)→0,04mol
→ nHCl = 0,11 mol
→ CM HCl = 0,110,2 = 0,55M
Câu 8. Cho 100 ml dung dịch HCl 0,5M vào 100 ml dung dịch NaAlO2 1M, phản ứng xong thu được m gam kết tủa. Giá trị của m là
A. 3,90
B. 7,80.
C. 5,85.
D. 4,68.
Lời giải:
Đáp án: A
nHCl=0,05mol→nH+=0,05mol
nNaAlO2=0,1mol→nAlO−2=0,1mol
Ta thấy nH+<nAlO−2 nên khi đó nAl(OH)3=nH+=0,05mol
→m=mAl(OH)3=0,05.78=3,9gam
Câu 9. Cho 3,24 gam Al2(SO4)3 phản ứng với 25 ml dung dịch NaOH thu được 0,78 gam kết tủa trắng. Nồng độ mol của dung dịch NaOH đã dùng là
A. 1,2M và 2,4M.
B. 1,2M.
C. 2,8M.
D. 1,2M và 2,8M.
Lời giải:
Đáp án: D
nAl2(SO4)3 = 0,01 mol → nAl3+ = 2.nAl2(SO4)3 = 0,02 mol
mà nAl(OH)3= 0,7878 = 0,01 mol < 0,02 nên có 2 trường hợp
Trường hợp 1: nOH−min = 3.nAl(OH)3 = 0,03 mol
→ CM NaOH = 0,030,025 = 1,2M.
Trường hợp 2: nOH−max = 4.nAl3+ – nAl(OH)3 = 4.0,02 – 0,01 = 0,07 mol
→ CM NaOH = 0,070,025 = 2,8M
Câu 10. Cho 200 ml dung dịch HCl 2M vào 100 ml dung dịch gồm NaOH 0,6M và NaAlO2 1M, phản ứng xong thu được m gam kết tủa. Giá trị của m là
A. 7,80.
B. 3,90.
C. 3,12.
D. 1,56.
Lời giải:
Đáp án: D
nHCl=0,4mol→nH+=0,4mol
nNaOH=0,06mol→nOH−=0,06mol
nNaAlO2=0,1mol→nAlO−2=0,1mol
Phương trình hóa học:
OH−+H+→H2O0,06→0,06
AlO−2+H++H2O→Al0,1→0,1→0,1
Al+3H+→Al3++3H2O0,08←0,24
Ta có: nAl(OH)3du=0,1−0,08=0,02mol→mAl(OH)3du=0,02.78=1,56gam
Xem thêm các phương trình hóa học khác:
NH3 + AlCl3 + H2O → Al(OH)3 + NH4Cl | NH3 ra NH4Cl
Al + HCl → AlCl3 + H2 | Al ra AlCl3
NaOH + H2SO4 → Na2SO4 + H2O | NaOH ra Na2SO4
Al + NaOH + H2O → NaAlO2 + H2 | Al ra NaAlO2
NaOH + CH3COOH → CH3COONa + H2O | NaOH ra CH3COONa | CH3COOH ra CH3COONa