Bài tập về điều chế kim loại
Kiến thức cần nhớ
Nguyên tắc điều chế kim loại
Nguyên tắc điều chế kim loại là khử ion kim loại thành nguyên tử.
Mn+ + ne → M
Phương pháp điều chế kim loại
Tùy thuộc vào độ hoạt động hóa học của kim loại mà người ta lựa chọn phương pháp điều chế phù hợp.
1. Phương pháp nhiệt luyện
- Nguyên tắc: Khử ion kim loại trong hợp chất ở nhiệt độ cao bằng các chất khử như C, CO, H2 hoặc các kim loại hoạt động (như Al).
- Phạm vi áp dụng: Sản xuất các kim loại có tính khử trung bình (Zn, Fe, Sn, Pb,…) trong công nghiệp.
- Ví dụ:
Fe2O3 + 3CO to→ 2Fe + 3CO2
2. Phương pháp thuỷ luyện
- Nguyên tắc: Dùng những dung dịch thích hợp như: H2SO4, NaOH, NaCN,… để hoà tan kim loại hoặc các hợp chất của kim loại và tách ra khỏi phần không tan có ở trong quặng. Sau đó khử những ion kim loại này trong dung dịch bằng những kim loại có tính khử mạnh hơn như Fe, Zn,…
- Phạm vi áp dụng: Thường sử dụng để điều chế các kim loại có tính khử yếu.
- Ví dụ dùng Fe để khử ion Cu2+ trong dung dịch muối đồng.
Fe + CuSO4→ FeSO4 + Cu↓
Fe + Cu2+ → Fe2+ + Cu↓
3. Phương pháp điện phân
a. Điện phân hợp chất nóng chảy
- Nguyên tắc: Khử các ion kim loại bằng dòng điện bằng cách điện phân nóng chảy hợp chất của kim loại.
- Phạm vi áp dụng: Điều chế các kim loại hoạt động hoá học mạnh như K, Na, Ca, Mg, Al…
- Ví dụ điện phân Al2O3 nóng chảy là phương pháp sản xuất nhôm trong công nghiệp.
+ Ở catot (cực âm): Al3+ + 3e → Al
+ Ở anot (cực dương): 2O2- → O2 + 4e
Phương trình điện phân: 2Al2O3 4Al + 3O2
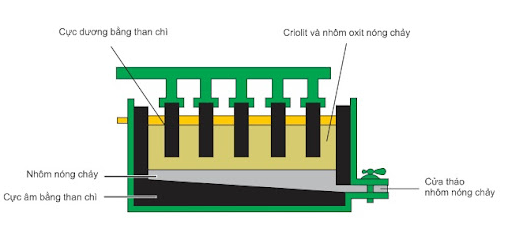
Sơ đồ thùng điện phân Al2O3 nóng chảy
b. Điện phân dung dịch
- Nguyên tắc: Khử các ion kim loại bằng dòng điện bằng cách điện phân dung dịch muối của kim loại.
- Phạm vi áp dụng: Điều chế các kim loại có độ hoạt động hoá học trung bình hoặc yếu như Zn, Cu …
- Ví dụ điện phân dung dịch CuCl2 để điều chế Cu:
+ Ở catot: Cu2+ + 2e → Cu
+ Ở anot: 2Cl- → Cl2 + 2e
Phương trình điện phân: CuCl2 dpdd→ Cu + Cl2
c. Tính lượng chất thu được ở các điện cực
Dựa vào công thức Farađây, có thể tính được khối lượng các chất thu được ở điện cực:
m=AItnF trong đó:
m: Khối lượng chất thu được ở điện cực (gam).
A: Khối lượng mol nguyên tử của chất thu được ở điện cực.
n: Số electron mà nguyên tử hoặc ion đã cho hoặc nhận.
I: Cường độ dòng điện (ampe)
t: Thời gian điện phân (giây)
F: Hằng số Farađây (F = 96500).
Các dạng bài tập về Điều chế kim loại
Dạng 1: Lí thuyết trọng tâm
Dạng 2: Oxit kim loại tác dụng với chất khử
Dạng 3: Điện phân
Bài toán 1: Xác định lượng chất trong quá trình điện phân
Bài toán 2: Xác định thời gian điện phân
Bài toán 3: Đồ thị
Ví dụ minh hoạ
Ví dụ 1: Khử hoàn toàn m gam Fe2O3 cần vừa đủ 4,704 lít khí CO (đktc). Giá trị của m là
Hướng dẫn giải chi tiết:
Khi oxit bị khử bởi CO:
nO(oxit) = nCO = 4,704/22,4 = 0,21 mol
BTNT "O": 3nFe2O3 = nO(oxit) = 0,21
=> nFe2O3 = 0,07 mol
=> m = 160.0,07 = 11,2 gam
Ví dụ 2: Hỗn hợp X gồm Fe, FeO, Fe2O3. Cho một luồng khí CO đi qua ống sứ đựng m g hỗn hợp X nung nóng. Sau khi kết thúc thí nghiệm thu được 64 g chất rắn A và 11,2 lít khí B (đktc) có tỉ khối so với hiđro là 20,4. Giá trị của a là
Hướng dẫn giải chi tiết:
Giả sử: nCO=x(mol);nCO2=y(mol)
Ta có hệ phương trình:
{nhh=x+y=0,5mhh=28x+44y=0,5.(20,4.2)→{x=0,1y=0,4
nCOpư=nCO2=0,4mol
BTKL: mCOpu+mX=mA+mCO2
→ mX=64−0.4(44−28)=70,4g
Ví dụ 3: Cho một luồng khí CO đi qua ống sứ đựng m gam Fe2O3 nung nóng. Sau một thời gian thu được 10,44 gam chất rắn X gồm Fe, FeO, Fe2O3 và Fe3O4. Hòa tan hết X trong dung dịch HNO3 đặc, nóng thu được 4,368 lít NO2 (sản phẩm khử duy nhất ở đktc). Giá trị của m là
Hướng dẫn giải chi tiết:
nNO2 = 0,195 mol
Xét toàn bộ quá trình chỉ có CO cho e (tạo CO2) và HNO3 nhận e (tạo NO2)
Bảo toàn e: 2.nCO = nNO2 => nCO = 0,0975 mol
=> nCO2= nCO = 0,0975 mol
Bảo toàn khối lượng: mCO + mFe2O3 = mCO2 + mhh oxit
=> mFe2O3 = 0,0975.44 + 10,44 – 0,0975.28 = 12 gam
Bài tập tự luyện
Câu 1: Khử hoàn toàn m gam Fe2O3 cần vừa đủ 4,704 lít khí CO (đktc). Giá trị của m là
Hướng dẫn giải chi tiết:
Khi oxit bị khử bởi CO:
nO(oxit) = nCO = 4,704/22,4 = 0,21 mol
BTNT "O": 3nFe2O3 = nO(oxit) = 0,21
=> nFe2O3 = 0,07 mol
=> m = 160.0,07 = 11,2 gam
Câu 2: Hỗn hợp X gồm Fe, FeO, Fe2O3. Cho một luồng khí CO đi qua ống sứ đựng m g hỗn hợp X nung nóng. Sau khi kết thúc thí nghiệm thu được 64 g chất rắn A và 11,2 lít khí B (đktc) có tỉ khối so với hiđro là 20,4. Giá trị của a là
Hướng dẫn giải chi tiết:
Giả sử: nCO=x(mol);nCO2=y(mol)
Ta có hệ phương trình:
{nhh=x+y=0,5mhh=28x+44y=0,5.(20,4.2)→{x=0,1y=0,4
nCOpư=nCO2=0,4mol
BTKL: mCOpu+mX=mA+mCO2
→ mX=64−0.4(44−28)=70,4g
Câu 3: Cho một luồng khí CO đi qua ống sứ đựng m gam Fe2O3 nung nóng. Sau một thời gian thu được 10,44 gam chất rắn X gồm Fe, FeO, Fe2O3 và Fe3O4. Hòa tan hết X trong dung dịch HNO3 đặc, nóng thu được 4,368 lít NO2 (sản phẩm khử duy nhất ở đktc). Giá trị của m là
Hướng dẫn giải chi tiết:
nNO2 = 0,195 mol
Xét toàn bộ quá trình chỉ có CO cho e (tạo CO2) và HNO3 nhận e (tạo NO2)
Bảo toàn e: 2.nCO = nNO2 => nCO = 0,0975 mol
=> nCO2= nCO = 0,0975 mol
Bảo toàn khối lượng: mCO + mFe2O3 = mCO2 + mhh oxit
=> mFe2O3 = 0,0975.44 + 10,44 – 0,0975.28 = 12 gam
Câu 4: Cho thanh sắt Fe vào dung dịch X chứa 0,1 mol AgNO3 và 0,2 mol Cu(NO3)2. Khi thấy thanh kim loại tăng lên 8,8 gam thì dừng lại. Tính khối lượng kim loại bám vào thanh sắt
Hướng dẫn giải chi tiết:
nAg+ = 0,1 mol; nCu2+ = 0,2 mol
Nếu Ag+ phản ứng hết :
Fe + 2Ag+ → Fe2+ + 2Ag
0,05 ← 0,1 → 0,1
=> mtăng = 0,1.108 – 0,05.56 = 8 < 8,8
=> Ag+ phản ứng hết; Cu2+ phản ứng 1 phần
Fe + Cu2+ → Fe2+ + Cu
x → x → x
=> mtăng = 64x – 56x = 8x
=> tổng khối lượng tăng ở 2 phản ứng là:
mtăng = 8 + 8x = 8,8 => x = 0,1 mol
=> mkim loại bám vào = mAg + mCu = 17,2 gam
Câu 5: Cho 0,56 gam bột sắt vào 100 ml dung dịch gồm AgNO3 0,3M và Cu(NO3)2 0,5M. Sau khi các phản ứng xảy ra hoàn toàn thu được m gam chất rắn X. Giá trị của m là
Hướng dẫn giải chi tiết:
nFe = 0,01 mol; nAgNO3 = 0,03 mol; nCu(NO3)2 = 0,05 mol
Ta thấy : ne Fe cho tối đa = 0,01.3 = 0,03 mol = ne Ag+ nhận tối đa
=> Fe phản ứng hết với Ag, tạo thành Fe3+ và Ag
=> nAg = nAgNO3 = 0,03 mol => m = 0,03.108 = 3,24 gam
Câu 6: Cho m gam Zn vào dung dịch chứa 0,15 mol FeCl3. Sau khi phản ứng xảy ra hoàn toàn thu được 3,92 gam chất rắn. Giá trị của m là:
Hướng dẫn giải chi tiết:
nFeCl3 = 0,15mol => mFe tối đa sinh ra = 0,15 . 56 = 8,4 gam > 3,92 gam
=> chất rắn chỉ có Fe, còn Zn đã phản ứng hết
nFe = 3,92 / 56 = 0,07 mol
FeCl3 phản ứng với Zn tạo thành Fe (0,07 mol) và FeCl2 (0,15 – 0,07 = 0,08 mol)
Bảo toàn e: 2nZn = 3nFe + nFeCl2 => nZn = 0,145 mol
=> m = 9,425 gam
Câu 7: Điện phân 400 ml dung dịch CuSO4 0,2M với cường độ dòng điện 10A trong một thời gian thu được 0,224 lít khí (đktc) ở anot. Biết điện cực đã dùng là điện cực trơ và hiệu suất điện phân là 100%. Khối lượng catot tăng là
Hướng dẫn giải chi tiết:
nCuSO4=0,4.0,2=0,08mol
Khí thu được ở anot là O2 → nO2=0,22422,4=0,01(mol)
Tại anot (+): 2H2O→4H++O2+4e
→ne(anot)=4nO2=0,04(mol)
Ta thấy: 2nCu2+(bandau)>4nO2 → Tại catot Cu2+ chưa bị điện phân hết
Tại catot (-): Cu2++2e→Cu
0,04 → 0,02 (mol)
→ mcatot tăng = mCu = 0,02.64 = 1,28 gam
Câu 8: Điện phân dung dịch CuSO4 với điện cực trơ, cường độ dòng điện 10A. Khi ở anot có 4 gam khí oxi bay ra thì ngưng. Phát biểu nào sau đây là đúng ?
A. Khối lượng đồng thu được ở catot là 16 gam.
B. Thời gian điện phân là 9650 giây.
C. pH của dung dịch trong quá trình điện phân luôn giảm.
D. Không có khí thoát ra ở catot.
Hướng dẫn giải chi tiết:
nO2 = 0,125 mol
Catot: Cu2+ + 2e → Cu
Anot: 2H2O → O2 ↑ + 4H+ + 4e
=> ne trao đổi = 4.nO2 = 0,5 mol
=> nCu = 0,5 / 2 = 0,25 mol => m = 16 gam => A đúng
t = n.F / I = 4825s => B sai
+) pH của dung dịch ban đầu giảm, khi hết Cu2+ thì nước điện phân ở catot tạo OH-, ở anot tạo ra H+ và nOH- = nH+ nên pH không đổi => C sai
+) hết Cu2+, nước điện phân ở catot tạo khí H2 => D sai
Câu 9: Hòa tan hoàn toàn hỗn hợp X gồm KCl và CuSO4 vào nước, thu được dung dịch Y. Điện phân dung dịch Y với điện cực trơ màng ngăn xốp, đến khi H2O bị điện phân tại cả 2 điện cực thì dừng điện phân. Số mol khí ở anot thoát ra bằng 4 lần số mol khí thoát ra tại catot. Phần trăm khối lượng của CuSO4 trong X là
Hướng dẫn giải chi tiết:
Tại A có 2Cl- → Cl2 + 2e
Tại K có Cu+2 +2e → Cu
2H2O + 2e → 2OH- +H2
Bảo toàn e có 2nCl2 = 2nCu + 2nH2
Vì nCl2 = 4nH2 nên 2nCl2 = 2nCu + ½ nCl2 → nCu = ¾ . nCl2
→ nCuSO4nKCl=38
→ %CuSO4=3.1603.160+8.74,5.100%=44,61%
2. Bài tập tự luyện có hướng dẫn
(Xem thêm ở file bên dưới)
Xem thêm các dạng bài tập và câu hỏi liên quan khác
95 Bài tập về Polime (có đáp án năm 2024) hay nhất
70 Bài tập về Peptit và protein (có đáp án năm 2023) - Hóa học 12
70 Bài tập về Amino axit (có đáp án năm 2023) - Hóa học 12
70 Bài tập về Amin (có đáp án năm 2023) - Hóa học 12
70 Bài tập về Saccarozơ, tinh bột và xenlulozơ (có đáp án năm 2023) - Hóa học 12












