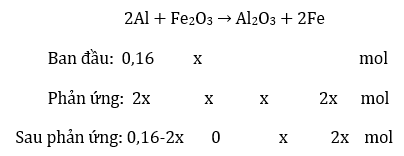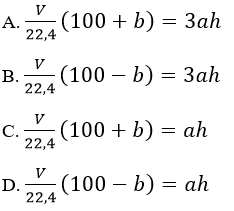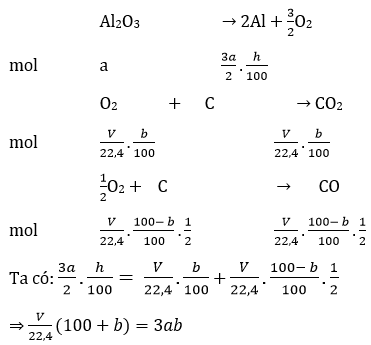Video giải Hóa 12 Bài 27: Nhôm và hợp chất của nhôm
Bài tập Nhôm và hợp chất của Nhôm
Kiến thức cần nhớ
NHÔM
I. VÍ TRÍ VÀ CẤU TẠO
- Al: 1s22s22p63s23p1
=> Số hiệu nguyên tử 13, thuộc nhóm IIIA, chu kì 3.
- Trong hợp chất, Al có số OXH bền là +3
- Nhôm có cấu tạo mạng tinh thể lập phương tâm diện
II. TÍNH CHẤT VẬT LÍ
- Nhôm là kim loại nhẹ, màu trắng bạc.
- Nhôm rất dẻo, dẫn điện, dẫn nhiệt rất tốt.
III. TÍNH CHẤT HÓA HỌC
1. Tác dụng với phi kim
- Với oxi: Ở to thường tạo lớp màng oxit bảo vệ. Nếu đốt bột nhôm thì sẽ phản ứng mạnh.
4Al + 3O2 2Al2O3
- Với phi kim khác:
+ Với Cl2, Br2 phản ứng ngay ở to thường tạo thành AlCl3, AlBr3 phản ứng bốc cháy.
Ví dụ:
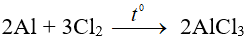
+ Khi đun nóng, phản ứng được với I2, S. Khi đun nóng mạnh, phản ứng được với N2, C.
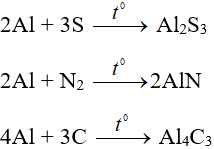
2. Tác dụng với axit
- Al + dung dịch axit (HCl, H2SO4) → muối + H2
2Al + 6H+ → 2Al3+ + 3H2
- Al + dung dịch axit (có tính OXH mạnh) → muối + sản phẩm khử + H2O
4Al + 4HNO3 loãng Al(NO3)3 + NO + 2H2O
2Al + 6H2SO4 đặc Al2(SO4)3 + 3SO2 + 6H2O
- Al không tác dụng với H2SO4, HNO3 đặc nguội.
3. Tác dụng với oxit kim loại
Ở nhiệt độ cao, Al khử được nhiều oxit kim loại như Fe2O3, Cr2O3,... thành kim loại tự do.
2Al + Fe2O3 Al2O3 + 2Fe
4. Tác dụng với dung dịch kiềm
2Al + 2NaOH + 6H2O → 2Na(dd) + 3H2
IV. ỨNG DỤNG VÀ SẢN XUẤT
1. Ứng dụng
- Người ta dùng nhôm để chế tạo vỏ máy bay, tên lửa, tàu vũ trụ do đặc tính nhẹ, bền với không khí và nước
- Làm dây dẫn điện cao áp, đồ nội thất, làm vật trao đổi nhiệt
- Chế tạo hỗn hợp tecmit (Al và Fe2O3) được dùng để hàn gắn đường ray.
2. Sản xuất
Điện phân nóng chảy Al2O3
2Al2O3 4Al + 3O2
MỘT SỐ HỢP CHẤT QUAN TRỌNG CỦA NHÔM
I. NHÔM OXIT
Tính chất vật lí : là chất rắn màu trắng, không tan trong nước nóng chảy ở 2050 độ C
Tính chất hóa học : Al2O3 là oxit lưỡng tính, tác dụng được với dung dịch axit và dung dịch kiềm:
Al2O3 + 6HCl → 2AlCl3 + 3H2O
Al2O3 + 2NaOH + 3H2O → 2Na
Ứng dụng :
- Tinh thể Al2O3 (corinđon) được dùng làm đồ trang sức, chế tạo các chi tiết trong các ngành kĩ thuật chính xác, như chân kính đồng hồ, thiết bị phát tia lade,...
- Bột Al2O3 có độ cứng cao được dùng làm vật liệu mài.
- Boxit Al2O3.2H2O là nguyên liệu sản xuất nhôm kim loại.
II. NHÔM HIDROXIT
Tính chất vật lí: Là chất kết tủa keo, màu trắng, không tan trong nước, dễ bị nhiệt phân hủy
Tính chất hóa học :
- Dễ bị nhiệt phân thành nhôm oxit :
2Al(OH)3 Al2O3 + 3H2O
- Là hợp chất lưỡng tính, tan trong axit và bazo
Al(OH)3 + 3HCl → AlCl3 + 3H2O
Al(OH)3 + NaOH → Na
Điều chế: Cho muối nhôm phản ứng với dung dịch NH3 hoặc muối Na2CO3 :
2AlCl3 + 3Na2CO3 + 3H2O → 2Al(OH)3↓ + 6NaCl + 3CO2↑
III. NHÔM SUNFAT
- Al2(SO4)3: là chất bột màu trắng, bị phân hủy nhiệt trên 770oC
- Phèn chua: K2SO4.Al2(SO4)3.24H2O hoặc : KAl(SO4)2.12H2O tồn tại ở dạng tinh thể có vị hơi chua và chát.
Các dạng bài tập Nhôm và hợp chất của nhôm
Dạng 1: Lí thuyết trọng tâm
Dạng 2: Nhôm hoặc nhôm oxit tác dụng với dung dịch bazơ
Dạng 3: Bài toán muối Al3+ tác dụng với dung dịch kiềm
Bài toán 1: Xác định sản phẩm
Bài toán 2: Xác định chất tham gia
Dạng 4: Bài toán hỗn hợp gồm Al với kim loại Na (hoặc K hoặc Ba) tác dụng với nước hoặc tác dụng với dung dịch kiềm dư
Dạng 5: Bài toán nhiệt nhôm
Bài toán 1: Phản ứng nhiệt nhôm xảy ra hoàn toàn
Bài toán 2: Phản ứng nhiệt nhôm không hoàn toàn
Dạng 6: Bài toán Al tác dụng với dung dịch HNO3
Dạng 7: Bài toán cho muối aluminat tác dụng với dung dịch axit
Bài toán 1: Xác định sản phẩm
Bài toán 2: Xác định chất tham gia
Dạng 8: Bài toán đồ thị
Bài toán 1: Đồ thị muối nhôm tác dụng với dung dịch kiềm
Bài toán 2: Đồ thị muối aluminat tác dụng với dung dịch axit
Bài tập
1. Bài tập vận dụng (có đáp án)
Bài 1: Hỗn hợp bột X gồm Al và Fe2O3. Nếu cho m gam hỗn hợp X tác dụng hết với dung dịch NaOH loãng thu được 5,376 lít H2 (đktc). Nếu nung nóng m gam hỗn hợp X để thực hiện hoàn toàn phản ứng nhiệt nhôm, thu được chắt rắn y. Cho Y phản ứng vừa du với V mi dung dịch hỗn hợp HCl 1M và H2SO4 0,5M tạo 4,4352 lít H2 (đklc) Giá trị cua V là :
A, 300 ml. B. 450 ml. C. 360 ml. D. 600 ml.
Đáp án: B
X phản ứng với NaOH được 5,376 lít H2 (đktc) ⇒ nAl = 0,16 mol
Phản ứng nhiệt nhôm:
Al và Fe phản ứng với hỗn hợp axit tạo khí ⇒ x = 0,042 mol
Từ các phản ứng của Al, Fe2O3, Al2O3, Fe với H+ trong V ml dung dịch hốn hợp HCl 1M và H2SO4 0,5M, tính được V = 450ml
Bài 2: Cho từ từ dung dịch Ba(OH)2 đến dư vào dung dịch chứa a mol Al2(SO4)3. Kết quả thí nghiệm được biểu diễn trên đồ thị bên.
Giá trị a là
A. 0,030 B. 0,045.
C. 0,050 D. 0,075.
Đáp án: A
Khi nBa(OH)2 0,060 mol hay 0,115 mol thì số mol kết tủa thu được là như nhau
Khi nBa(OH)2 = 0,06 mol thì 2a mol Al3+ chưa kết tủa hết
Phản ứng:
3Ba(OH)2 + 2Al2(SO4)3 → 3BaSO4 + 2Al(OH)3
Số mol kết tủa thu được là 0,1 mol
Khi nBa(OH)2 = 0,115 mol, 2a mol Al3+ đã kết tủa hết, sau đó kết tủa tan ra.
nBaSO4 + nAl(OH)3 còn lại = 0,1 mol
3a + 2(4a -0,115) = 0,1
⇒ a = 0,03 mol
Bài 3: Hỗn hợp X gồm Al và Fe3O4. Nung hỗn hợp X ở nhiệt độ cao thu được hỗn hợp Y. Chia Y làm 2 phần bằng nhau:
• Phần 1 cho vào dung dịch NaOH lấy dư, sau phản ứng thu được 1,344 lít khí (đktc).
• Phần 2 hòa tan hết trong 310 ml dung dịch H2SO4 1M (loãng) thu được 3,36 lít khí (đktc).
Hiệu suất của phản ứng nhiệt nhôm là ?( Giả sử Fe3O4 chỉ bị khử về Fe)
A. 60%. B. 66,67%.
C. 75%. D. 80%.
Đáp án: D
Al + Fe3O4 -to→ Y
Phần 1: Y + NaOHdư Al + Fe3O4 → H2 (0,06 mol)
Y có Al dư nAl dư = 2/3. nH2 = 0,04 mol
Phần 2: Bảo toàn electron → 2nH2 = 3nAl + 2nFe → 2. 0,15 = 3. 0,04 + 2nFe → nFe = 0,09 mol
8Al + 3Fe3O4 -to→ 9Fe + 4Al2O3
Có nFe = 0,09 mol → nAl2O3 = 0,04 mol
Có nH2SO4 = 4nFe3O4 dư + 3nAl2O3 + 1,5nAl dư + nFe
nFe3O4 dư = (0,31 - 3. 0,04 - 1,5. 0,04 - 0,09)/4 = 0,01 mol
nAl = nAl dư + nAl pư = 0,04 + 0,08 = 0,12 mol
nFe3O4 = nFe3O4 dư + nFe3O4 pư = 0,01 + 0,03 = 0,04
ta có: nAl / 8 > nFe3O4 / 3 ⇒ Hiệu suất tính theo Fe3O4
H% = 0,03 : 0,04 x 100% = 75%
Bài 4: Trong các cặp chất sau đây, cặp chất nào có thể cùng tồn tại trong một dung dịch?
A. AlCl3 và Na2CO3
B. HNO3 và NaHCO3
C. NaAlO2 và KOH
D. NaCl và AgNO3
Đáp án: A
Bài 5: Dùng hóa chất nào sau đây để phân biệt Zn(NO3)2 và Al(NO3)3 ?
A. Dung dịch NaOH
B. Dung dịch Ba(OH)2
C. Dung dịch NH3
D. Dung dịch nước vôi trong
Đáp án: C
Khi cho NH3 vào 2 dung dịch cả 2 dung dịch đều xuất hiện kết tủa hidroxit, nhưng Zn(OH)2 tạo thành có khả năng tạo phức với NH3 nên kết tủa lại tan, còn với Al(OH)3 không tan trong NH3
Bài 6: Thực hiện các thí nghiệm sau :
(a) Cho từ từ NaOH đến dư vào dung dịch Al2(SO4)3,
(b) Cho từ từ Al2(SO4)3 đến dư vào dung dịch NaOH,
(c) Cho từ từ NH3 đến dư vào dung dịch Al2(SO4)3,
(d) Cho từ từ Al2(SO4)3 đến dư vào dung dịch NH3.
(e) Cho từ từ HCl đến dư vào dung dịch NaAlO2 .
(f) Cho từ từ NaAlO2 đến dư vào dung dịch HCl
(g) Cho từ từ Al2(SO4)3 đến dư vào dung dịch NaAlO2
Trong các thí nghiệm trên, số thí nghiệm xuất hiện kết tủa là
A. 2. B. 3. C. 5. D, 7.
Đáp án: C
Bài 7: Cho 3,82 gam hợp kim Ba, Al vào nước dư chỉ thu được dung dịch chưa duy nhất một muối. Khối lượng Ba là:
A. 3.425 gam. B. 1,644 gam.
C. 1,370 gam, D. 2,740 gam
Đáp án: D
Công thức muối Ba(AlO2)2 ⇒ nAl = 2nBa ⇒ mBa = 2,740 gam
Bài 8: Điện phân a mol Al2O3 nóng cháy với điện cực bằng than chi. Hiệu suất điện phản là h%. Sau điện, tại anot thoát ra V lit khí (đktc) gồm khí ( O2 và CO, trong đó phần trăm CO2 là b% về thể tích. Biểu thức liên hệ giữa a b, V và h là:
Đáp án: A
Bài 9: Cho m gam hỗn hợp X gồm 2 kim loại kiềm thuộc 2 chu kì liên tiếp tác dụng với 180 ml dung dịch Al2(SO4)3 1M thu được 15,6 gam kết tủa; khí H2 và dung dịch A. Nếu cho m gam hỗn hợp X tác dụng với 240 gam dung dịch HCI 18,25% thu được dung dịch B và H2. Cô cạn dung dịch B thu được 83,704 gam chất rắn khan. Biết rằng m < 45 gam. Phần trăm khối lượng của kim loại kiềm có nguyên tử khối nhỏ hơn trong X là:
A. 48,57%. B. 37,10%. C. 16,43%. D. 28,22%.
Đáp án: D
Đặt công thức chung của 2 kim loại là X : nAl3+ = 0,36 mol; nAl(OH)3 = 0,2 mol
Trường hợp 1: OH- phản ứng với AlAl3+ dư:
nOH- = 3n↓ = 0,6 = nX
trường hợp 2: OH- dư phản ứng AlAl3+
nOH- = 3nAlAl3+ + (nAlAl3+ - n↓) = 1,24 = nX
Nếu nX = 0,6 < nHCl ⇒ 83,704 gam muối XCl
⇒ nCl- = 0,6 mol hay mCl- = 21,3 gam ⇒ mX = 62,404 gam > 45(loại)
Nếu nX = 1,24 mol > nHCl ⇒ 83,704 gam gồm muối XCl( 1,2 mol) và XOH ( 0,04 mol)
⇒ mX = 40,424 < 45 . Ta có: X = 32,6
Hai kim loại kiềm là Na và K
Tính được số mol Na và K lần lượt là 0,496 và 0,744
%mNa = 28,22%
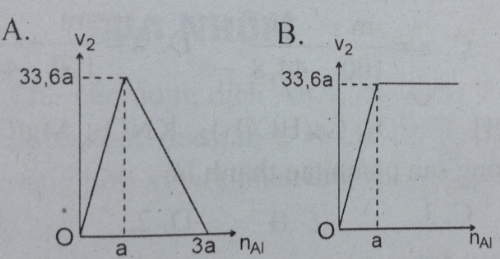
Bài 10: Cho a mol Na vào nước thu được V1 lít khí. Sau đó thêm từ từ bột nhôm vào dung dịch thu được V2 lít khí ở đktc. Đồ thị biểu diễn mối quan hệ giữa V2 và so mol nhôm thêm vào là:
Đáp án: B
Bài 11: Cho các quặng sau: pirit, thạch cao, mica, apatit, criolit, boxit, dolomit. Số quặng chứa nhôm là:
A.2. B. 3. C. 4. D. 5.
Đáp án: B
Bài 12: Cho một lá nhôm vào ống nghiệm chứa dung dịch Hg(NO3)2, thấy có một lớp thủy ngân bám trên bề mặt nhôm. Hiện tượng tiếp theo quan sát được là:
A. khí hiđro thoát ra mạnh.
B. khí hiđro thoát ra sau đó dừng lại ngay.
C. lá nhôm bốc cháy.
D. lá nhôm tan ngay trong thủy ngân và không có phản ứng.
Đáp án: A
2Al + 3Hg(NO3)2 → 2Al(NO3)3 + 3Hg
Al sẽ tạo với Hg hỗn hống. Hỗn hống Al tác dụng với nước
2Al + 6H2O → 2 Al(OH)3 + 3H2
Bài 13: Cho sơ đồ phản ứng : Al → X→Al2O3→Al
X có thể là
A. AlCl3. B. NaAlO2. C. Al(NO3)3. D. Al2(SO4)3.
Đáp án: C
Bài 14: Phát biểu nào sau đây là sai ?
A. Dung dịch AlCl3 và Al2(SO3)3 làm quỳ tím hóa hồng
B. Al(OH)3, Al2O3, Al đều là các chất lưỡng, tính,
C. Nhôm là kim loai nhẹ và có khả năng dẫn điện Iot
D. Từ Al2O3 có thế điều chế được Al.
Đáp án: B
Bài 15: Hiện tượng nào xảy ra khi cho từ từ đến dư dung dịch NaOH vào dung dịch AlCl3 ?
A. Ban đầu không thấy hiện tượng, sau đó kết tủa xuất hiện
B. Xuất hiện kết tủa keo trắng ngay lập tức, sau đó kết tủa tan dần
C. Ban đầu không thấy hiện tượng, sau đó kết tủa xuất hiện, rồi tan dần.
D. Xuất hiện kết tủa keo trắng ngay lập tức và không tan,
Đáp án: B
2. Bài tập tự luyện có hướng dẫn
(Xem thêm ở file bên dưới)
Xem thêm các dạng bài tập và câu hỏi liên quan khác
50 Bài tập về Este (có đáp án)
70 Bài tập về Saccarozơ, tinh bột và xenlulozơ (có đáp án)
70 Bài tập về Lipit (có đáp án)