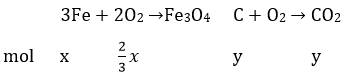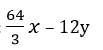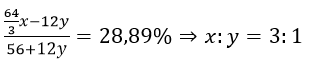Bài tập hợp kim
Kiến thức cần nhớ
Khái niệm
Hợp kim là vật liệu kim loại có chứa một kim loại cơ bản và một số kim loại hoặc phi kim khác.
Ví dụ:
+ Thép là hợp kim của sắt với cacbon và một số nguyên tố khác.

Thép
+ Đuyra là hợp kim của nhôm với đồng, mangan, magie, silic.
Tính chất của hợp kim
- Tính chất của hợp kim phụ thuộc vào thành phần các đơn chất tham gia cấu tạo nên mạng tinh thể hợp kim.
- Nhìn chung, hợp kim có nhiều tính chất hóa học tương tự tính chất của các đơn chất tham gia tạo thành hợp kim.
Ví dụ: Hợp kim Cu-Zn
+ Tác dụng với dung dịch NaOH: Chỉ có Zn phản ứng
Zn + 2NaOH → Na2ZnO2 + H2↑
+ Tác dụng với dung dịch H2SO4 đặc, nóng: Cả 2 đều phản ứng
Cu + 2H2SO4 đặc CuSO4 + SO2 + 2H2O
Zn + 2H2SO4 đặc ZnSO4 + SO2 + 2H2O
- Tính chất vật lý và tính chất cơ học của hợp kim lại khác nhiều với tính chất của các đơn chất. Ví dụ:
+ Hợp kim không bị ăn mòn: Fe, Cr, Mn (thép inox), …
+ Hợp kim siêu cứng: W – Co; Co – Cr – W – Fe, …
+ Hợp kim có nhiệt độ nóng chảy thấp: Sn – Pb (thiếc hàn nóng chảy ở 210oC), có hợp kim gồm Bi – Pb – Sn nóng chảy ở 65oC.
+ Hợp kim nhẹ, cứng và bền: Al – Si; Al – Cu – Mn – Mg.

Inox
Ứng dụng của hợp kim
Hợp kim được sử dụng rộng rãi trong các ngành kinh tế quốc dân:
- Những hợp kim nhẹ,bền chịu được nhiệt độ cao và áp suất cao dùng để chế tạo tên lửa, tàu vũ trụ, máy bay, ô tô,…
- Những hợp kim có tính bền hoá học và cơ học cao dùng để chế tạo các thiết bị trong ngành dầu mỏ và công nghiệp hoá chất.
- Những hợp kim cứng và bền dùng để xây dựng nhà cửa và cầu cống.
- Những hợp kim không gỉ dùng để chế tạo các dụng cụ y tế, dụng cụ làm bếp,…
- Hợp kim của vàng với Ag, Cu (vàng tây) đẹp và cứng dùng để chế tạo đồ trang sức và trước đây ở một số nước còn dùng để đúc tiền.
Các dạng bài tập hợp kim
Dạng 1: Lí thuyết về hợp kim
Ví dụ 1: Phát biểu nào sau đây sai?
A. Hợp kim là vật liệu kim loại có chứa một kim loại cơ bản và một số kim loại khác hoặc phi kim.
B. Tính chất của hợp kim phụ thuộc vào thành phần, cấu tạo của hợp kim.
C. Hợp kim có tính chất hóa học khác tính chất của các kim loại tạo ra chúng.
D. Hợp kim có tính chất vật lí và tính cơ học khác nhiều các kim loại tạo ra chúng.
Hướng dẫn giải
Hợp kim là vật liệu kim loại có chứa một kim loại cơ bản và một số kim loại hoặc phi kim khác A đúng.
Tính chất của hợp kim phụ thuộc vào thành phần các đơn chất tham gia, cấu tạo mạng tinh thể của hợp kim B đúng.
Hợp kim có nhiều tính chất hóa học tương tự tính chất của các đơn chất tham gia tạo thành hợp kim, nhưng tính chất vật lí và tính chất cơ học của hợp kim lại khác nhiều với tính chất các đơn chất C sai, D đúng.
Chọn C.
Ví dụ 2: Phát biểu nào sau đây sai về tính chất của hợp kim?
A. Liên kết trong đa số tinh thể hợp kim vẫn là liên kết kim loại.
B. Hợp kim thường dẫn nhiệt và dẫn điện tốt hơn kim loại nguyên chất.
C. Độ cứng của hợp kim thường lớn hơn độ cứng của kim loại nguyên chất.
D. Nhiệt độ nóng chảy của hợp kim thường thấp hơn nhiệt độ nóng chảy của kim loại nguyên chất.
Hướng dẫn giải
Đáp án B sai vì hợp kim còn chứa một số kim loại hoặc phi kim khác nên làm giảm độ dẫn điện và dẫn nhiệt của kim loại nguyên chất.
Chọn B.
Ví dụ 3: Một hợp kim gồm các kim loại sau: Ag, Zn, Fe, Cu. Hóa chất có thể hòa tan hoàn toàn hợp kim trên thành dung dịch là
A. dung dịch NaOH.
B. dung dịch H2SO4 đặc, nguội.
C. dung dịch HCl.
D. dung dịch HNO3 loãng.
Hướng dẫn giải
Để hòa tan hoàn toàn hợp kim thì dung dịch đó phải hòa tan tất cả các kim loại có trong hợp kim.
Dung dịch NaOH không hòa tan được Ag, Fe, Cu Loại A.
Dung dich H2SO4 đặc nguội không hòa tan được Fe Loại B.
Dung dịch HCl không hòa tan được Ag và Cu Loại C.
Dung dịch HNO3 hòa tan được các kim loại trong hợp kim.
Chọn D.
Dạng 2: Bài toán về hợp kim
Phương pháp giải
- Hàm lượng kim loại A trong hợp kim:
- Xác định công thức hợp kim: AxByCz…
Ta có:
Ví dụ 1: Trong hợp kim Al - Mg, cứ có 9 mol Al thì có 1 mol Mg. Thành phần phần trăm khối lượng của hợp kim là
A. 80% Al và 20% Mg.
B. 81% Al và 19% Mg.
C. 91% Al và 9% Mg.
D. 83% Al và 17% Mg
Hướng dẫn giải
Trong hợp kim Al - Mg, cứ 9 mol Al thì có 1 mol Mg nên công thức của hợp kim là Al9Mg.
Chọn C.
Ví dụ 2: Một loại đồng thau có chứa 59,63% Cu và 40,37% Zn. Hợp kim này có cấu tạo tinh thể của hợp chất hóa học giữa đồng và kẽm. Công thức hóa học của hợp chất là
A. Cu3Zn2.
B. Cu2Zn3.
C. Cu2Zn.
D. CuZn2.
Hướng dẫn giải
Gọi công thức tổng quát của hợp chất là: CuxZny.
Xét tỉ lệ:
Chọn x = 3, y = 2
Vậy công thức hóa học là Cu3Zn2.
Chọn A.
Bài tập tự luyện
Bài 1: Một hợp kim có chứa 2,8 gam Fe và 0,81 gam Al. Cho hợp kim vào 200ml dung dịch X chứa AgNO3 và Cu(NO3)2 sau khi phản ứng kết thúc được dung dịch Y và 8,12 gam chất rắn Z gồm 3 kim loại. Cho chất rắn Z tác dụng với dung dịch HCl dư được 0,672 lít H2 (ở đktc). Nồng độ mol của dung dịch AgNO3 là:
A. 0,1 B. 0,15 C. 0,28 D. 0,25
Đáp án: B
Z gồm 3 kim loại Ag, Cu và Fe dư
Đặt số mol Ag, Cu và Fe trong Z lần lượt là a, b, c
mhỗn hợp = 108a + 64b + 56c = 8,12 (1)
khi cho Z tác dụng với HCl, chỉ có Fe phản ứng tạo khí
Fe + HCl → FeCl2 + H2
nFe = nH2 = 0,03 mol, hay c = 0,03 mol (2)
xét phản ứng của 2,8 gam Fe ( 0,05 mol) và 0,81 gam Al ( 0,03 mol) với dung dịch X.
Sau phản ứng này Fe còn dư ( 0,03 mol) nên toàn bộ Al đã phửn ứng hết
Bảo toàn e: a + 2b = 0,13 (3)
Từ (1), (2) và (3), suy ra: a = 0,03 mol; b = 0,05 mol; c = 0,03 mol
CM(AgNO3) = 0,15M
Bài 2: Liên kết hoá học chủ yếu trong họp kim là
A. liên kết kim loại và liên kết cộng hoá trị.
B. liên kết cộng hoá trị và liên kết ion.
C. liên kết ion và tương tác yếu giữa các phân tử (tương tác Van der Waals).
D. tương tác yếu giữa các phân tử (tương tác Van der Waals) và liên kết kim loại.
Đáp án: A
Bài 3: Cho các tính chất sau :
( 1 ) Tính chất vật lí ; (2) Tính chất hoá học ; (3) Tính chất cơ học.
Hợp kim và các kim loại thành phần tạo hợp kim đỏ có tính chất nào tương tự ?
A. (1) B. (2) và (3) C. (2) D.(l)và(3)
Đáp án: C
Bài 4: Một mẫu kim loại thủy ngân có lẫn tạp chất kẽm, thiếc, chì. Để làm sạch các tạp chất này có thể cho mẫu thủy ngân trên tác dụng với lượng dư của dung dịch nào sau đây ?
A. Hg(NO3)2 B. Zn(NO3)2 C. Sn(NO3)2 D. Pb(NO3)2
Đáp án: A
Khi cho mẫu thuỷ ngân lẫn các tạp chất kém, thiếc, chì phản ứng với Hg(HNO3)2 dư sẽ xảy ra các phản ứng:
Zn + Hg(NO3)2 → Zn(NO3)2 + Hg
Sn + Hg(NO3)2 → Sn(NO3)2 + Hg
Pb + Hg(NO3)2 → Pb(NO3)2 + Hg
Vậy toàn bộ các tạp chất được loại bỏ khỏi Hg
Bài 5: Có 3 mẫu họp kim gồm Ag-Cu, Cu-Al và Fe-Cr-Mn. Dùng dung dịch nào sau đây có thể phân biệt được 3 hợp kim trên ?
A. HNO3 B. HCl
C. AgNO3 D. H2SO4đặc, nóng
Đáp án: D
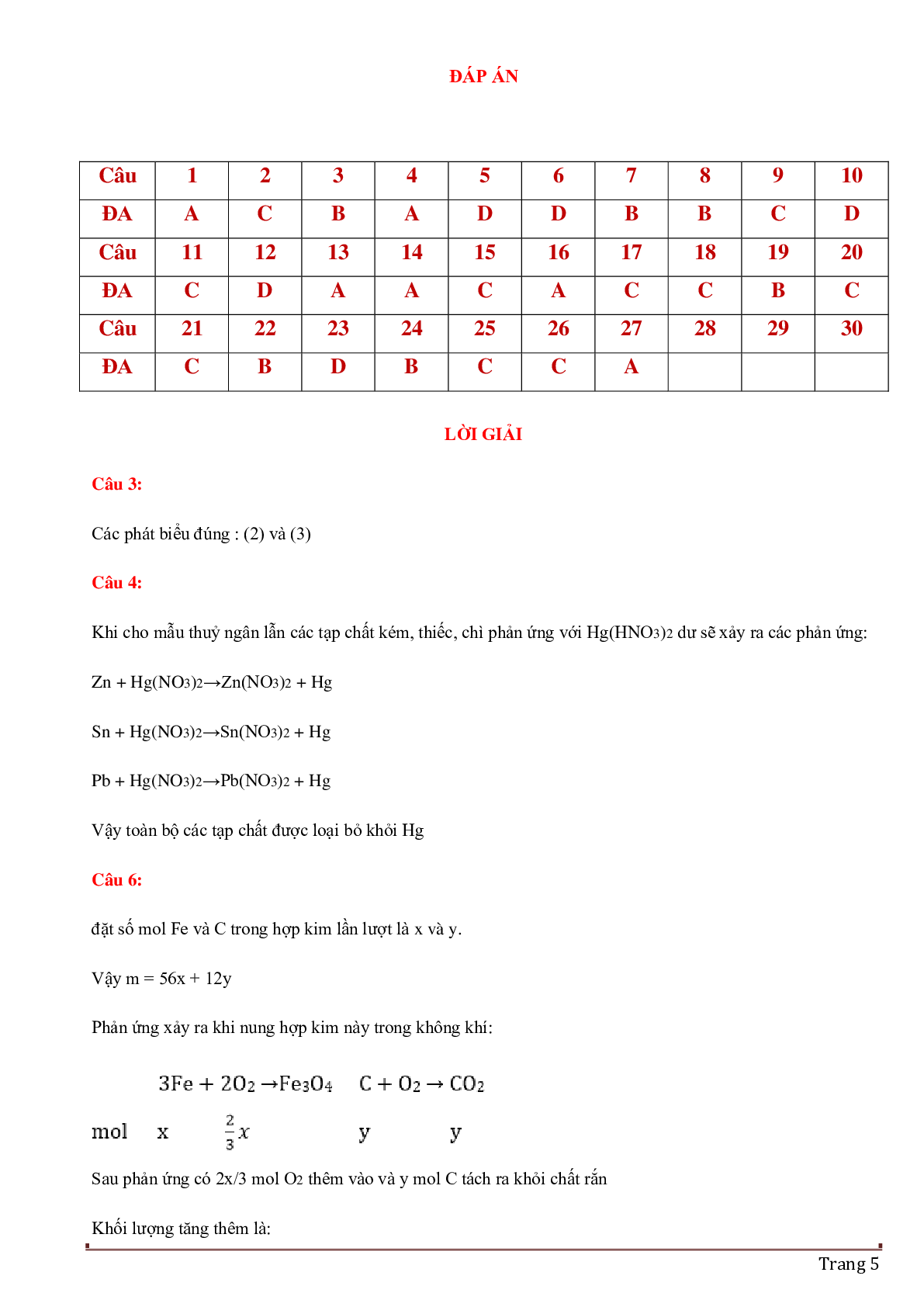
Bài 6: Để xác định hàm lượng C trong một mẫu hợp kim Fe-C, người ta đem nung m gam hợp kim này trong không khí. Sau phản ứng hoàn toàn, chất rắn thu được có khối lượng tăng 28,89% so với lượng chất rắn ban đầu
a) Công thức hoá học của loại hợp kim trên là
A. FeC. B. FeC2. C. FeC3. D. Fe3C.
b) Hàm lượng % của C trong hợp kim trên là
A. 17,65. B. 30,00%. C. 39,13%. D. 6,67%.
Đáp án: a/ D, b/ D
đặt số mol Fe và C trong hợp kim lần lượt là x và y.
Vậy m = 56x + 12y
Phản ứng xảy ra khi nung hợp kim này trong không khí:
Sau phản ứng có 2x/3 mol O2 thêm vào và y mol C tách ra khỏi chất rắn
Khối lượng tăng thêm là:
Theo đề ta có:
Vậy công thức hợp kim là Fe3C và hàm lượng C là 6,67%
Bài 7: Có các phát biểu sau:
(1) Hợp kim thép (Fe-C) ít bị ăn mòn hơn sắt.
(2) Hợp kim Al-Cu-Mn-Mg nhẹ và cứng, dùng trong chế tạo tên lửa, tàu vũ trụ.
(3) Hợp kim vàng tây (Au-Ag-Cu) cứng hơn vàng nguyên chất.
(4) Hợp kim Bi-Pb-Sn có nhiệt độ nóng chảy rất cao.
Trong các phát biểu trên, số phát biểu đúng là
A.l. B. 2. C.3. D. 4.
Đáp án: B
Các phát biểu đúng: (2) và (3)
Xem thêm các dạng câu hỏi và bài tập liên quan khác:
70 Bài tập về Kim loại kiềm và hợp chất quan trọng của kim loại kiềm (2024) có đáp án chi tiết nhất
70 Bài tập về Kim loại kiềm thổ (2024) có đáp án chi tiết nhất
70 Bài tập sắt và hợp chất của sắt (2024) có đáp án (chi tiết nhất)
70 Bài tập Nhôm và hợp chất của nhôm (2024) có đáp án chi tiết nhất
Tính chất hóa học của rượu Etylic (ancol etylic hoặc etanol) chi tiết nhất (2024)