Bài tập về Axit photphoric và muối photphat
Kiến thức cần nhớ
Axit photphoric H3PO4
I. Cấu tạo phân tử
- Công thức cấu tạo:
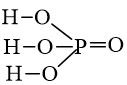
- Trong hợp chất H3PO4, photpho có số oxi hóa cao nhất là +5.
II. Tính chất vật lí
- Là chất rắn dạng tinh thể trong suốt, nóng chảy ở 42,5ºC, rất háo nước nên dễ chảy rữa và tan vô hạn trong nước.
- Axit photphoric thường dùng là dung dịch đặc, sánh, không màu, có nồng độ 85%.
III. Tính chất hóa học
Khác với axit nitric, axit photphoric không có tính oxi hóa.
1. Axit photphoric là axit ba nấc
- Trong dung dịch nước, axit photphoric phân li theo từng nấc:
Nấc 1:
Nấc 2:
Nấc 3:
- Sự phân li chủ yếu xảy ra theo nấc 1, nấc 2 kém hơn và nấc 3 rất yếu.
- Như vậy trong dung dịch axit photphoric có các ion: và các phân tử H3PO4 không phân li (không kể các ion H+ và OH- do nước phân li ra).
2. Axit photphoric có độ mạnh trung bình
- Dung dịch axit photphoric có những tính chất chung của axit như làm quỳ tím hóa đỏ, tác dụng với oxit bazơ, bazơ, muối, kim loại.
Lưu ý: Khi tác dụng với dung dịch kiềm, tùy theo lượng chất tác dụng mà axit photphoric tạo ra muối trung hòa, muối axit hoặc hỗn hợp muối.
Thí dụ:
H3PO4+NaOH→NaH2PO4+H2O
H3PO4+2NaOH→Na2HPO4+2H2O
H3PO4+3NaOH→Na3PO4+3H2O
IV. Ứng dụng và điều chế
1. Ứng dụng
- Một lượng lớn axit photphoric dùng để điều chế các muối photphat và sản xuất phân lân, thuốc trừ sâu,…

Hình 1: Phân lân nung chảy dạng viên
- Axit H3PO4 tinh khiết được dùng trong công nghiệp dược phẩm.
2. Điều chế
a) Trong phòng thí nghiệm
P+5HNO3đặcH3PO4+H2O+5NO2
b) Trong công nghiệp
+ Cho H2SO4 đặc tác dụng với quặng photphorit hoặc quặng apatit:
Ca3(PO4)2+3H2SO4đặc3CaSO4↓+2H3PO4
→ Điều chế bằng phương pháp này không tinh khiết và lượng chất thấp.
+ Để điều chế H3PO4 có độ tinh khiết và nồng độ cao hơn người ta đốt cháy P để được P2O5, rồi cho P2O5 tác dụng với nước:
4P+5O22P2O5
P2O5+3H2O→2H3PO4
MUỐI PHOTPHAT
Axit photphoric tác dụng với dung dịch kiềm, tạo ra 3 loại muối:
- Muối photphat trung hòa: Na3PO4, Ca3(PO4)2, …
- Muối đihiđrophotphat: NaH2PO4, Ca(H2PO4)2, …
- Muối hiđrophotphat: Na2HPO4, CaHPO4, …
1. Tính tan
Tất cả các muối đihiđrophotphat đều tan trong nước. Các muối hiđrophotphat và photphat trung hòa đều không tan hoặc ít tan trong nước (trừ muối natri, kali, amoni).
2. Nhận biết ion photphat ()
- Thuốc thử là bạc nitrat.
- Hiện tượng: Xuất hiện kết tủa màu vàng.
- Phương trình ion rút gọn:
3Ag+ + → Ag3PO4↓ (màu vàng)
Lưu ý: Kết tủa Ag3PO4 không tan trong nước, nhưng tan trong dung dịch axit nitric loãng.

Hình 2: Cho AgNO3 tác dụng với Na3PO4.
Các dạng bài tập về Axit photphoric và muối photphat
Dạng 1: Bài tập lí thuyết về sự điện li, hóa học và phương pháp điều chế , muối photphat
Dạng 2: Axit phophoric tác dụng với kiềm
Bài tập tự luyện
Câu 1: Để nhận biết ion PO43- trong dung dịch muối, người ta dùng thuốc thử là
A. dung dịch AgNO3
B. dung dịch NaOH
C. dung dịch HNO3
D. dung dịch Br2
Hướng dẫn giải chi tiết:
Ta dùng ion Ag+ để nhận biết ion PO43- do tạo kết tủa màu vàng:
Ag+ + PO43- → Ag3PO4 ↓ vàng
Đáp án A
Câu 2: Thuốc thử để nhận biết các dung dịch : HCl, NaCl, Na3PO4, H3PO4 là
A. BaCl2 và quỳ tím.
B. AgNO3 và quỳ tím.
C. H2SO4 và quỳ tím.
D. Quỳ tím.
Hướng dẫn giải chi tiết:
Dùng dung dịch AgNO3 và quỳ tím
|
|
HCl |
NaCl |
Na3PO4 |
H3PO4 |
|
Quỳ tím |
Chuyển đỏ |
Không đổi màu |
Chuyển xanh |
Chuyển đỏ |
|
Dung dịch AgNO3 |
↓ trắng |
|
|
↓ vàng |
Đáp án B
Câu 3: Chọn câu sai:
A. Tất cả các muối đihiđrophotphat đều tan trong nước.
B. Tất cả các muối hiđrophotphat đều tan trong nước.
C. Các muối photphat trung hòa của natri, kali, amoni đều tan trong nước.
D. Các muối photphat trung hòa của hầu hết các kim loại đều không tan trong nước.
Hướng dẫn giải chi tiết:
- Tất cả muối H2PO4- đều tan;
- Muối PO43- và HPO42- chỉ có muối của kim loại kiềm và amoni tan được.
=> câu sai là B. Tất cả các muối hiđrophotphat đều tan trong nước.
Đáp án B
Câu 4: Cho 200 ml dung dịch H3PO4 0,3M vào 500 ml dung dịch Ba(OH)2 0,16M. Sau khi phản ứng xảy ra hoàn toàn. Khối lượng muối có phân tử khối bé hơn là
Hướng dẫn giải chi tiết:
= 0,06 mol
= 0,08 mol = 0,16 mol
Ta thấy 2 < 2,67
BT nguyên tố P:
=> x + y = 0,06 (1)
BT điện tích:
=> 2x + 3y = 0,16 (2)
Từ (1) và (2) => x = 0,02 mol; y = 0,04 mol
Ta có:
= 0,02 mol
= 0,02.233 = 4,66 gam
= 0,02 mol
0,02.601 = 12,02 gam
Câu 5: Cho 14,2 gam P2O5 vào 200 gam dung dịch NaOH 8% thu được dung dịch A. Muối thu được và nồng độ % tương ứng là
Hướng dẫn giải chi tiết:
P2O5 + 3H2O → 2H3PO4 (1)
0,1 → 0,2 mol
Tỉ lệ Sản phẩm tạo thành là Na2HPO4
Bảo toàn nguyên tố P:
Khối lượng dung dịch sau phản ứng là :
=>
Câu 6: Cho 200 ml dung dịch NaOH 2M tác dụng với 100 ml dung dịch H3PO4 aM thu được 25,95 gam hai muối. Giá trị của a là:
Hướng dẫn giải chi tiết:
Ta có:
nNaOH =0,4(mol)
vì dung dịch sau phản ứng có hai muối => NaOH phản ứng hết
OH- + H+ → H2O
Mol : 0,4 → 0,4 → 0,4
Bảo toàn khối lượng có : mNaOH + mH3PO4 = mmuối + mH2O
=> mH3PO4 = 25,95 + 0,4.18 – 0,4.40 = 17,15 gam
=>nH3PO4 = 0,175 => CH3PO4= 1,75(M)
Câu 7: Từ quặng photphorit, có thể điều chế axit photphoric theo sơ đồ sau :
Biết hiệu suất chung của quá trình là 90%. Để điều chế được 1 tấn dung dịch H3PO4 49%, cần khối lượng quặng photphorit chứa 73% Ca3(PO4)2 là
Hướng dẫn giải chi tiết:
mH3PO4 = 1.49 / 100 = 0,49 tấn
Ca3(PO4)2 → 2H3PO4
310 196
0,775 tấn ← 0,49 tấn
=> mCa3(PO4)2 thực tế dùng = 0,775.100 / 90 = 31/36 tấn
=> mquặng = 31/36 . 100/73 = 1,18 tấn
Câu 8: Hòa tan 142 gam P2O5 vào 500 gam dung dịch H3PO4 24,5%. Nồng độ % của H3PO4 trong dung dịch thu được là
Hướng dẫn giải chi tiết:
nP2O5 = 1 mol; nH3PO4 ban đầu = 1,25 mol
P2O5 + 3H2O → 2H3PO4
1 mol → 2 mol
=> tổng số mol H3PO4 trong dung dịch thu được
= 2 + 1,25 = 3,25 mol
=> mH3PO4 = 318,5 gam
mdung dịch thu được = mP2O5 + mdung dịch ban đầu
= 142 + 500 = 642 gam
=> C% = 318,5 / 642 . 100% = 49,61%
Câu 9: Lấy 124 gam P đem điều chế H3PO4 với hiệu suất phản ứng đạt 100%. Thể tích dung dịch H3PO4 35% (D = 1,25 gam/ml) có thể thu được là
Hướng dẫn giải chi tiết:
nP = 124 : 31 = 4 (mol)
Áp dụng định luật bảo toàn nguyên tố P
=> n P = n H3PO4 = 4 (mol)
m H3PO4 = 4 . 98 = 392 (gam)
m dd = m ct : C% = 392 : 35% = 1120 gam
=> V dd = 1120 : 1,25 = 896 ml
Xem thêm các dạng câu hỏi và bài tập liên quan khác:
30 bài tập về Andehit (2024) có đáp án chi tiết nhất
30 bài tập về Sulfuric acid và muối sulfate (2024) có đáp án chi tiết nhất
30 bài tập về Ammonia. Muối ammonium (2024) có đáp án chi tiết nhất
30 Bài tập về Khái niệm về cân bằng hoá học (2024) có đáp án chi tiết nhất
30 Bài tập về Cân bằng trong dung dịch nước (2024) có đáp án chi tiết nhất











