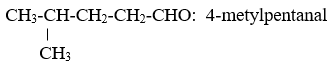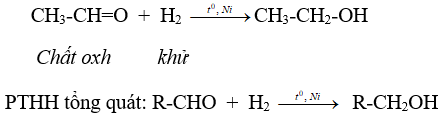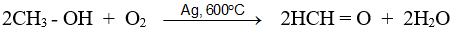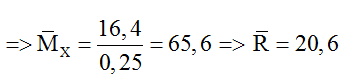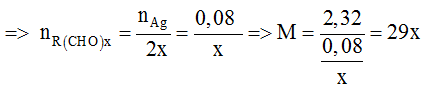ANĐEHIT
I. Lý thuyết và phương pháp giải
1. Đặc điểm cấu tạo, phân loại
a/ Cấu tạo
– Công thức tổng quát của anđehit là: R(CHO)m (m ≥ 1)
R có thể là H hoặc gốc hiđrocacbon và đặc biệt có hợp chất CHO-CHO, trong đó m = 2, R không có.
– Công thức của anđehit no đơn chức, mạch thẳng:
CnH2n+1CHO (n ≥ 0)
– Trong phân tử anđehit có nhóm chức -CHO liên kết với gốc R có thể no hoặc không no.
b/ Phân loại
- Dựa vào đặc điểm cấu tạo gốc hidrocacbon:
+ Anđehit no
+ Anđehit không no
+ Anđehit thơm
- Dựa vào số nhóm –CHO
+ Anđehit đơn chức
+ Anđehit đa chức
CH2=CH-CH=O propenal: Anđehit không no
C6H5-CH=O benzanđehit: Anđehit thơm
O=CH-CH=O anđehit oxalic: Anđehit đa chức
2. Danh pháp
- Tên thay thế: Tên hiđrocacbon no tương ứng với mạch chính + al
- Tên thông thường: anđehit + tên axit tương ứng.
| Anđehit | Tên thay thế | Tên thông thường |
|
HCH=O CH3CH=O CH3CH2CH=O (CH3)2CHCH2CH=O CH3CH=CHCH=O |
metanal etanal propanal 3-metylbutanal but-2-en-1-al |
fomanđehit (anđehit fomic) axetanđehit (anđehit axetic) Propionanđehit (anđehit propionic) isovaleranđehit (anđehit isovaleric) crotonanđehit (anđehit crotonic) |
3. Tính chất vật lý
- Ở đk thường, các anđehit đầu dãy là các chất khí và tan rất tốt trong nước. Các anđehit tiếp theo là các chất lỏng hoặc rắn, độ tan giảm khi phân tử khối tăng.
– Nhiệt độ sôi của anđehit thấp hơn của rượu tương ứng vì giữa các phân tử anđehit không có liên kết hidro.
- Dung dịch bão hòa của anđehit fomic (37 - 40%) được gọi là fomalin.
4. Tính chất hóa học
a. Phản ứng cộng hiđro
b. Phản ứng oxi hóa không hoàn toàn
HCHO + 2AgNO3 + H2O + 3NH3 −tº→ H-COONH4 + 2NH4NO3 + 2Ag
TQ: R-CH=O + 2AgNO3 + H2O + 3NH3 −tº→ R-COONH4 + 2NH4NO3 + 2Ag
Pư trên còn được gọi là pư tráng bạc.
Hay: 2CH3-CH=O + O2 −tº, xt→ 2CH3-COOH
2R-CHO + O2 −tº, xt→ 2R-COOH
Nhận xét: Anđehit vừa thể hiện tính oxi hóa vừa thể hiện tính khử.
c. Tác dụng với brom và kali pemanganat
Anđehit rất dễ bị oxi hoá, nó làm mất màu nước brom, dung dịch kali pemanganat và bị oxi hoá thành axit cacboxylic, thí dụ :
RCH=O + Br2 + H2O → R-COOH + 2HBr
* Chú ý : Đối với HCHO phản ứng xảy ra như sau :
HCH=O + 2Br2 + H2O → CO2 + 4HBr
5. Điều chế, ứng dụng
a. Điều chế
- Từ ancol: Oxi hóa ancol bậc I.
R-CH2OH + CuO −tº→ R-CHO + H2O + Cu
- Fomanđehit được điều chế trong công nghiệp bằng cách oxi hoá metanol nhờ oxi không khí ở 600ºC - 700ºC với xúc tác là Cu hoặc Ag :
- Từ hiđrocacbon
CH4 + O2 −tº, xt→ HCHO + H2O
2CH2=CH2 + O2 −tº, xt→ 2CH3-CHO
CH CH + H2O −HgSO4→ CH3-CHO
b. Ứng dụng
- Fomanđehit :
Fomanđehit được dùng chủ yếu để sản xuất poli(phenolfomanđehit) (làm chất dẻo) và còn được dùng trong tổng hợp phẩm nhuộm, dược phẩm.
Dung dịch 37- 40% fomanđehit trong nước gọi là fomalin (còn gọi là fomol) được dùng để ngâm xác động vật, thuộc da, tẩy uế, diệt trùng...
- Axetanđehit : Axetanđehit chủ yếu được dùng để sản xuất axit axetic.
6. Phương pháp giải
+ Bước 1: Tính số mol các chất đề bài đã cho số liệu và viết phương trình phản ứng hóa học xảy ra.
+ Bước 2: Tính toán luôn theo phương trình phản ứng hóa học hoặc đặt ẩn nếu đề bài là hỗn hợp.
+ Bước 3: Lập phương trình toán học và giải phương trình Số mol các chất cần tìm.
+ Bước 4: Tính toán theo yêu cầu đề bài.
Lưu ý: Trong một hỗn hợp mà có nhiều phản ứng xảy ra thì phản ứng trung hoà được ưu tiên xảy ra trước.
II. Ví dụ minh họa
Ví dụ 1: Cho 16,4 gam hỗn hợp X gồm 2 axit cacboxylic là đồng đẳng kế tiếp nhau phản ứng hoàn toàn với 200 ml dung dịch NaOH 1M và KOH 1M, thu được dung dịch Y. Cô cạn dung dịch Y, thu được 31,1 gam hỗn hợp chất rắn khan. Công thức của 2 axit trong X là
A. C2H4O2 và C3H4O2.
B. C2H4O2 và C3H6O2.
C. C3H4O2 và C4H6O2.
D. C3H6O2 và C4H8O2.
Lời giải:
Đáp án B
Hướng dẫn Gọi CTPT của hỗn hợp X là
nNaOH = 0,2 mol; nKOH = 0,2 mol
Áp dụng định luật bảo toàn khối lượng: mX + mNaOH + mKOH = mmuối + mH2O
=> mH2O = 4,5 gam => nH2O = 0,25 mol
=> 2 axit là CH3COOH và C2H5COOH
Ví dụ 2: Cho các chất : (1) axit propionic ; (2) axit axetic ; (3) etanol ; (4) đimetyl ete. Nhiệt độ sôi biến đổi :
A. (2) >(1) >(3) >(4)
B. (2) >(3) >(1) >(4)
C. (1) >(2) >(3) >(4)
D. (4) >(3) >(2) >(1)
Lời giải:
Đáp án C
Hướng dẫn Theo chiều giảm nhiệt độ sôi : axit > ancol > anđehit
=> thứ tự giảm dần là : (1) axit propionic > (2) axit axetic > (3) etanol > (4) đimetyl ete.
Ví dụ 3: Quá trình nào sau đây không tạo ra anđehit axetic ?
A. CH3COOCH=CH2 + NaOH.
B. CH2=CH2 + H2O (to, HgSO4).
C. CH2=CH2 + O2 (to, xt).
D. C2H5OH + CuO (to).
Lời giải:
Đáp án B
Hướng dẫn
A. CH3COOCH=CH2 + NaOH → CH3COONa + CH3CHO
B. CH2=CH2 + H2O → CH3CH2OH
C. 2CH2=CH2 + O2 PdCl2, CuCl2→ 2CH3CHO
D. C2H5OH + CuO → CH3CHO + Cu + H2O
III. Bài tập tự luyện
Bài 1: Có thể dùng một chất nào trong các chất dưới đây để nhận biết được các chất: ancol etylic, glixerol, dung dịch anđehit axetic đựng trong ba lọ mất nhãn?
A. Cu(OH)2/OH-
B. Quỳ tím
C. Kim loại Na
D. dd AgNO3/NH3.
Lời giải:
Đáp án A
Hướng dẫn
- Dùng Cu(OH)2/OH- thực hiện theo 2 bước như sau:
| C2H5OH | C3H5(OH)3 | CH3CHO | Bước 1: Cu(OH)2/OH- (to thường) | Không phản ứng | Phức màu xanh | Không phản ứng | Bước 2: Cu(OH)2/OH- đun nóng | Không phản ứng | Kết tủa đỏ gạch |
Bài 2: Có bao nhiêu anđehit 2 chức có CTĐGN là C2H3O?
A. 2
B. 4
C. 1
D. 3
Lời giải:
Đáp án A
Hướng dẫn Anđehit 2 chức có 2 nhóm –CHO => phân tử có 2 nguyên tử O
=> CTPT: C4H6O2
Có 2 công thức thỏa mãn là
OHC-CH2-CH2-CHO
CH3-CH(CHO)2
Bài 3: Đốt cháy hoàn toàn 0,2 mol anđehit A no, mạch hở, đơn chức thu được tổng khối lượng CO2 và H2O là 49,6 gam. Anđehit A là
A. C2H4O
B. C3H6O2
C. C4H8O
D. C5H10O
Lời giải:
Đáp án C
Hướng dẫn
Đốt cháy anđehit no, mạch hở đơn chức thu được nCO2 = nH2O = a mol
=> mCO2 + mH2O = 49,6 => 44a + 18a = 49,6 => a = 0,8 mol
=> số C trong A = nCO2 / nA = 0,8 / 0,2 = 4 => CTPT của A là C4H8O
Bài 4: Hợp chất A chứa C, H, O có M < 90 đvC. A tham gia phản ứng tráng bạc và có thể tác dụng với H2 (xt Ni) sinh ra ancol chứa C bậc IV trong phân tử. Công thức của A là
A. (CH3)2CHCHO.
B. (CH3)2CH-CH2CHO.
C. (CH3)3C-CH2CHO.
D. (CH3)3CCHO.
Lời giải:
Đáp án D
Hướng dẫn
A có khả năng tráng bạc => A chứa gốc –CHO
Ancol chứa C bậc IV => có dạng (CH3)3C-R-CHO
Vì M < 90 => 57 + R + 29 < 90 => R = 0
=> A là (CH3)3CCHO.
Bài 5: Hiện nay nguồn nguyên liệu chính để sản xuất anđehit axetic trong công nghiệp là
A. etanol.
B. etan.
C. axetilen.
D. etilen.
Lời giải:
Đáp án D
Hướng dẫn
Nguồn nguyên liệu chính để sản xuất anđehit axetic trong công nghiệp là etilen
2CH2=CH2 + O2 PdCl2, CuCl2→ 2CH3CHO
Bài 6: Trong các chất sau đây, chất nào có nhiệt độ sôi cao nhất ?
A. CH3CH2OH.
B. CH3COOH.
C. CH3CHO.
D. CH3CH3.
Lời giải:
Đáp án B
Hướng dẫn
Axit có nhiệt độ sôi cao hơn ancol có khối lượng phân tử tương đương vì phân tử axit tạo được 2 liên kết hiđro và liên kết hiđro giữa các phân tử axit bền hơn liên kết hiđro giữa các phân tử ancol.
=> chất có nhiệt độ sôi cao nhất là axit CH3COOH.
Bài 7: Chuyển hóa hoàn toàn 2,32 gam anđehit X mạch hở bằng phản ứng tráng gương với dung dịch AgNO3/NH3 dư rồi cho lượng Ag sinh ra tác dụng hết với dung dịch HNO3 dư tạo ra 3,808 lít NO2 ở 27oC và 1,033 atm. Tên gọi của anđehit là:
A. anđehit fomic
B. anđehit axetic
C. anđehit acrylic
D. anđehit oxalic
Lời giải:
Đáp án D
Hướng dẫn nNO2 = PV / RT = 1,033.3,808 / (0,082.(273 + 27)) = 0,16 mol
Bảo toàn e: ne cho = ne nhận
=> nAg = nNO2 = 0,16 mol
TH1: X là anđehit fomic => nHCHO = nAg / 4 = 0,04 mol
=> M = 2,32 / 0,04 = 58 (loại vì MHCHO = 30)
TH2: X có dạng R(CHO)x (R ≠ H; x ≥ 1)
+) Với x = 1 => M = 29 (loại)
+) Với x = 2 => M = 58 => X là OHC-CHO : anđehit oxalic
Bài 8: Trong các chất: ancol propylic, anđehit fomic, axit butiric và etilen glycol, chất có nhiệt độ sôi nhỏ nhất là
A. axit oxalic
B. anđehit fomic
C. axit butiric
D. etilen glycol
Lời giải:
Đáp án B
Hướng dẫn Theo chiều giảm nhiệt độ sôi : axit > ancol > anđehit
=> chất có nhiệt độ sôi nhỏ nhất là anđehit fomic
Bài 9: Để trung hòa 6,72 gam một axit cacboxylic Y (no, đơn chức), cần dùng 200 gam dung dịch NaOH 2,24%. Công thức của Y là
A. CH3COOH.
B. HCOOH.
C. C2H5COOH.
D. C3H7COOH.
Lời giải:
Đáp án A
Hướng dẫn nNaOH = 0,112 mol
Y là axit no, mạch hở => nRCOOH = nNaOH = 0,112 mol
=> M = 6,72 / 0,112 = 60 => Y là CH3COOH
Bài 10: Đốt cháy hoàn toàn m gam anđehit A không no (trong phân tử chứa 1 liên kết đôi C=C), mạch hở, 2 chức bằng O2 vừa đủ, hấp thụ toàn bộ sản phẩm sinh ra vào dung dịch Ba(OH)2 dư, thấy có 394 gam kết tủa và khối lượng dung dịch giảm đi 284,4 gam. CTPT của A là
A. C4H6O2
B. C5H6O2
C. C6H8O2
D. C5H8O2
Lời giải:
Đáp án B
Hướng dẫn Anđehit A không no (trong phân tử chứa 1 liên kết đôi C=C), mạch hở, 2 chức có CTPT dạng CnH2n-4O2
CnH2n-4O2 + O2 → nCO2 + (n – 2)H2O
=> đốt cháy A thu được nCO2 – nH2O = 2.nA
nBaCO3 = 2 mol => nCO2 = 2 mol
mdung dịch giảm = mBaCO3 – (mCO2 + mH2O) = 284,4 => mH2O = 394 – 2.44 – 284,4 = 21,6 gam
=> nH2O = 1,2 mol
=> nA = (2 – 1,2) / 2 = 0,4 mol
=> Số C trong A = nCO2 / nA = 2 / 0,4 = 5
=> CTPT của A là C5H6O2
Bài 11: Đun nóng 24 gam axit axetic với lượng dư ancol etylic (xúc tác H2SO4 đặc), thu được 26,4 gam este. Hiệu suất của phản ứng este hóa là
A. 75%
B. 44%
C. 55%
D. 60%
Lời giải:
Đáp án A
Hướng dẫn
CH3COOH + C2H5OH H2SO4, to⇔ CH3COOC2H5 + H2O
nCH3COOC2H5 theo pt = nCH3COOH = 0,4 mol
Mà nCH3COOC2H5 thực tế thu được = 0,3 mol
=> H = nCH3COOC2H5 thực tế thu được / nCH3COOC2H5 theo pt = 0,3 / 0,4 = 75%
Bài 12: Trung hoà 3,88 gam hỗn hợp X gồm hai axit cacboxylic no, đơn chức, mạch hở bằng dung dịch NaOH, cô cạn toàn bộ dung dịch sau phản ứng thu được 5,2 gam muối khan. Nếu đốt cháy hoàn toàn 3,88 gam X thì thể tích oxi (đktc) cần dùng là
A. 1,12 lít.
B. 3,36 lít.
C. 4,48 lít.
D. 2,24 lít.
Lời giải:
Đáp án B
Hướng dẫn Gọi X có dạng CnH2nO2
CnH2nO2 → CnH2n-1O2Na
=> nCnH2nO2 = nCnH2n-1O2Na = (5,2 – 3,88) / 22 = 0,06 mol
Đốt cháy hỗn hợp X thu được nCO2 = nH2O = n.nCnH2nO2 = 0,06n = 0,06.7/3 = 0,14 mol
Bảo toàn O: nO trong axit + 2.nO2 = 2.nCO2 + nH2O
=> nO2 = (0,14.3 – 0,06.2) / 2 = 0,15 mol
=> V = 3,36 lít
Bài 13: Cho 3,6 gam axit cacboxylic no, đơn chức X tác dụng hoàn toàn với 500 ml dung dịch gồm KOH 0,12M và NaOH 0,12M. Cô cạn dung dịch thu được 8,28 gam hỗn hợp chất rắn khan. Công thức phân tử của X là
A. C2H5COOH.
B. CH3COOH.
C. HCOOH.
D. C3H7COOH.
Lời giải:
Đáp án B
Hướng dẫn nKOH = 0,06 mol; nNaOH = 0,06 mol
Bảo toàn khối lượng: mX + mNaOH + mKOH = mrắn khan + mH2O
=> mH2O = 1,08 gam => nH2O = 0,06 mol
Vì X là axit đơn chức => nX = nROH = nH2O = 0,06 mol
=> MX = 3,6 / 0,06 = 60
=> X là CH3COOH
Bài 14: Một anđehit X trong đó oxi chiếm 37,21% về khối lượng. Cho 1 mol X tham gia phản ứng tráng bạc tạo tối đa 4 mol Ag. Khối lượng muối hữu cơ sinh ra khi cho 0,25mol X tác dụng với lượng dư AgNO3 trong dung dịch NH3 là:
A. 38g
B. 34,5g
C.41g
D. 30,25g
Lời giải:
Đáp án A
Hướng dẫn 1 mol X phản ứng tạo 4 mol Ag => X là HCHO hoặc là anđehit 2 chức
+) Nếu là HCHO => %mO = 53,33% => Loại
=> X có 2 nhóm CHO : R(CHO)2 => MX = 86g = R + 29.2 => R = 28
=> X là C2H4(CHO)2 khí phản ứng với AgNO3/NH3 tạo muối C2H4(COONH4)2
=> mmuối = 38g
Bài 15: Hỗn hợp Z gồm hai axit cacboxylic đơn chức X và Y (MX > MY) có tổng khối lượng là 8,2 gam. Cho Z tác dụng vừa đủ với dung dịch NaOH, thu được dung dịch chứa 11,5 gam muối. Mặt khác, nếu cho Z tác dụng với một lượng dư dung dịch AgNO3 trong NH3, thu được 21,6 gam Ag. Công thức và phần trăm khối lượng của X trong Z là
A. C3H5COOH và 54,88%.
B. C2H3COOH và 43,90%.
C. C2H5COOH và 56,10%.
D. HCOOH và 45,12%.
Lời giải:
Đáp án B
Hướng dẫn Z có phản ứng tráng gương => Y là HCOOH
nY = nAg / 2
nX + nY = (mmuối – mZ) / 22 = 0,15 mol => nX = 0,05
mZ = 0,05.MX + 0,1.46 = 8,2
=> MX = 72 => X là CH2=CH-COOH
=> %mX = 0,05.72/8,2 . 100% = 43,90%
Bài 16: Hỗn hợp X gồm axit panmitic, axit stearic và axit linoleic. Để trung hòa m gam X cần 40 ml dung dịch NaOH 1M. Mặt khác, nếu đốt cháy hoàn toàn m gam X thì thu được 15,232 lít khí CO2 (đktc) và 11,7 gam H2O. Số mol của axit linoleic trong m gam hỗn hợp X là
A. 0,01.
B. 0,015.
C. 0,020.
D. 0,005.
Lời giải:
Đáp án B
Hướng dẫn nCO2 = 0,68 mol; nH2O = 0,65 mol
Axit panmitic, axit stearic cháy cho nCO2 = nH2O
=> nC17H31COOH = (nCO2 – nH2O) / 2 = 0,015 mol
Bài 17: X có CTPT C20H36Om. Biết X là 1 anđehit no, mạch hở. Giá trị của m là
A. 4
B. 3
C. 2
D. 1
Lời giải:
Đáp án B
Hướng dẫn X là 1 anđehit no, mạch hở => trong X chỉ chứa liên kết π ở chức CHO
=> số chức m = số nguyên tử O = độ bất bão hòa k
=> độ bất bão hòa k = (2.20 + 2 – 36) / 2 = m => m = 3
Bài 18: Hỗn hợp gồm 0,1 mol một axit cacboxylic đơn chức và 0,1 mol muối của axit đó với kim loại kiềm có tổng khối lượng là 15,8 gam. Tên của axit trên là
A. axit propanoic.
B. axit etanoic.
C. axit metanoic.
D. axit butanoic.
Lời giải:
Đáp án B
Hướng dẫn Giả sử axit trên là RCOOH => muối là RCOOM (M là kim loại kiềm)
15,8 = 0,1.(R + 45) + 0,1.(R + 44 + M)
=> R = 34,5 – 0,5M
Với M = 23 => R = 23 (loại)
Với M = 39 (K) => R = 15 (CH3)
=> axit etanoic CH3COOH
Bài 19: Cho sơ đồ sau: C3H6 → C3H7Br → C3H8O → C3H6O (X). Biết các chất đều là sản phẩm chính. X có những tính chất là
A. phản ứng cộng với H2.
B. phản ứng tráng bạc.
C. phản ứng với Cu(OH)2/OH- (to).
D. cả A, B, C.
Lời giải:
Hướng dẫn CH2=CH-CH3 → CH3-CHBr-CH3 → CH3-CH(OH)-CH3 → CH3-CO-CH3
=> X là xeton chỉ có phản ứng cộng với H2
Bài 20: Đốt cháy hoàn toàn m gam hỗn hợp A gồm 2 anđehit X và Y no, mạch hở, 2 chức, là đồng đẳng liên tiếp (MX < MY) bằng V lít khí O2 (đktc), hấp thụ hết sản phẩm thu được vào 250 ml dung dịch Ca(OH)2 0,5M thấy xuất hiện 9 gam kết tủa và khối lượng bình tăng 9,29 gam. CTPT của Y là
A. C4H8O
B. C4H6O2
C. C5H8O2
D. C5H10O
Lời giải:
Đáp án C
Hướng dẫn Gọi CTPT chung của anđehit X và Y no, mạch hở, 2 chức là CaH2a-2O2
=> đốt cháy hỗn hợp A thu được nCO2 – nH2O = nA
nCa(OH)2 = 0,125 mol; nCaCO3 = 0,09 mol
TH1: Chỉ thu được 1 kết tủa CaCO3
=> nCO2 = nCaCO3 = 0,09 mol
mbình tăng = mCO2 + mH2O = 9,29 => nH2O = 0,296 > nCO2 => loại
TH2: Thu được 2 muối CaCO3 và Ca(HCO3)2
Bảo toàn Ca: nCa(HCO3)2 = nCa(OH)2 – nCaCO3 = 0,125 – 0,09 = 0,035 mol
Bảo toàn C: nCO2 = 2.nCa(HCO3)2 + nCaCO3 = 2.0,035 + 0,09 = 0,16 mol
mbình tăng = mCO2 + mH2O = 9,29 => mH2O = 2,25 gam => nH2O = 0,125 mol
=> nA = nCO2 – nH2O = 0,16 – 0,125 = 0,035 mol
=> số C trung bình = 0,16 / 0,035 = 4,57
=> X và Y lần lượt là C4H6O2 và C5H8O2
Bài 21: Hỗn hợp X gồm 1 ancol và 2 sản phẩm hợp nước của propen. Tỉ khối hơi của X so với hiđro bằng 23. Cho m gam X đi qua ống sứ đựng CuO dư nung nóng. Sau khi các phản ứng xảy ra hoàn toàn thu được hỗn hợp Y gồm 3 chất hữu cơ và hơi nước, khối lượng ống sứ giảm 3,2 gam. Cho Y tác dụng hoàn toàn với lượng dư dung dịch AgNO3/NH3 tạo ra 48,6 gam Ag. Phần trăm khối lượng của propan-1-ol trong X là
A. 16,3%.
B. 65,2%.
C. 48,9%.
D. 83,7%.
Lời giải:
Đáp án A
Hướng dẫn
X chứa C3H7OH và có M = 46 => ancol còn lại là CH3OH
Gọi nCH3CH2CH2OH = a mol; nCH3COCH3 = b mol => nCH3OH = a + b mol
=> nO = a + b + a + b = 0,2 (1)
Y gồm CH3CH2CHO (a mol) ; CH3-CO-CH3 (b mol) và HCHO (a + b) mol
=> nAg = 2.nCH3CH2CHO + 4.nHCHO = 2a + 4.(a + b) = 0,45 (2)
Từ (1) và (2) => a = 0,025; b = 0,075
=> %mCH3CH2CH2OH = 16,3%
Bài 22: Hiđro hóa hoàn toàn 2,9 gam một anđehit A được 3,1 gam ancol. A có công thức phân tử là
A. CH2O.
B. C2H4O.
C. C3H6O.
D. C2H2O2.
Lời giải:
Đáp án A
Hướng dẫn Pứ anđehit + H2 => Ancol
=> mH2 = mAncol – mAnđehit => nH2 = 0,2 mol
(Với x là số liên kết π trong anđehit, và H2 cộng vào liên kết pi)
=> Manđehit = 29x
A, B, C đều có 1 liên kết π => x = 1 => A đúng
D có 2 liên kết π => x = 2 nhưng M = 58 # 56
Xem thêm các dạng câu hỏi và bài tập liên quan khác
30 Bài tập về Axit nitric và muối nitrat (có đáp án)
30 Bài tập về photpho (có đáp án)
30 Bài tập về phân bón hóa học (có đáp án)
50 Bài tập về Axit photphoric và muối photphat (có đáp án)
30 Bài tập về Phản ứng trao đổi ion trong dung dịch các chất điện li (có đáp án)