Bài tập về sự điện li
Kiến thức cần nhớ
Hiện tượng điện li
1. Thí nghiệm
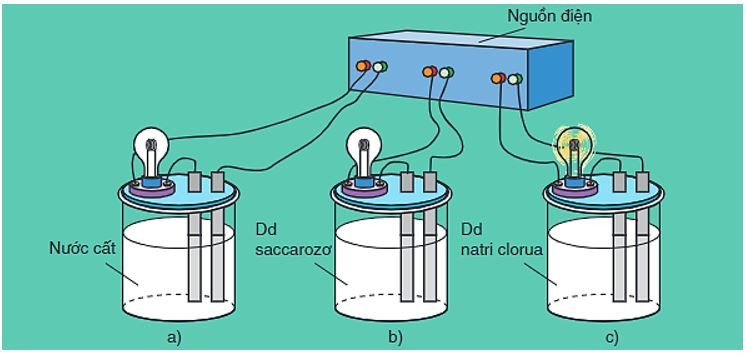
Hình 1: Bộ dụng cụ chứng minh tính dẫn điện của dung dịch
- Khi nối các đầu dây dẫn điện với cùng một nguồn điện, ta chỉ thấy bóng đèn ở cốc đựng dung dịch NaCl bật sáng.
⇒ Dung dịch NaCl dẫn điện, còn nước cất và dung dịch saccarozơ không dẫn điện.
- Nếu làm các thí nghiệm tương tự, người ta thấy:
+ NaCl rắn, khan; NaOH rắn, khan; các dung dịch ancol etylic (C2H5OH), glixerol (C3H5(OH)3) không dẫn điện.
+ Các dung dịch axit, bazơ và muối đều dẫn điện.
2. Nguyên nhân tính dẫn điện của các dung dịch axit, bazơ và muối trong nước
Nguyên nhân: Các dung dịch axit, bazơ và muối dẫn điện được là do trong dung dịch của chúng có các tiểu phân mang điện tích chuyển động tự do được gọi là các ion.
3. Các khái niệm cần nắm vững
- Sự điện li là quá trình phân li các chất trong nước ra ion.
- Chất điện li là những chất khi tan trong nước phân li ra ion.
⇒ Axit, bazơ và muối là những chất điện li.
- Sự điện li được biểu diễn bằng phương trình điện li.
Ví dụ:
- Muối phân li thành cation kim loại (hoặc cation amoni) và anion gốc axit:
NaCl→Na+
NH4Cl → NH4+ + Cl-
- Axit phân li thành cation H+ và anion gốc axit:
- Bazơ phân li thành cation kim loại và anion hiđroxit:
Chú ý: Nhiều chất khi nóng chảy cũng phân li ra ion, nên ở trạng thái nóng chảy các chất này dẫn điện được.
Phân loại các chất điện li
Dựa vào mức độ phân li ra ion, chất điện li được chia thành hai loại:
1. Chất điện li mạnh
- Chất điện li mạnh là chất khi tan trong nước, các phân tử hoà tan đều phân li ra ion.
- Những chất điện li mạnh là:
+ Các axit mạnh như HCl, HNO3, HClO4, H2SO4, ...;
+ Các bazơ mạnh như NaOH, KOH, Ba(OH)2 ,...
+ Hầu hết các muối.
- Phương trình điện li, người ta dùng một mũi tên chỉ chiều của quá trình điện li.
Ví dụ:
2. Chất điện li yếu
- Chất điện li yếu là chất khi tan trong nước chỉ có một phần số phân tử hoà tan phân li ra ion, phần còn lại vẫn tồn tại dưới dạng phân tử trong dung dịch.
- Những chất điện li yếu là:
+ Các axit yếu như CH3COOH, HClO, H2S, HF, H2SO3, ... ;
+ Các bazơ yếu như Bi(OH)3, Mg(OH)2, ...
+ Một số muối: HgCl2; Hg(CN)2; …
+ Nước (H2O).
- Trong phương trình điện li của chất điện li yếu, người ta dùng hai mũi tên ngược chiều nhau.
- Sự phân li của chất điện li yếu là quá trình thuận nghịch, khi nào tốc độ phân li và tốc độ kết hợp các ion tạo thành phân tử bằng nhau cân bằng của quá trình điện li được thiết lập.
Ví dụ:
Lưu ý: Cân bằng điện li là cân bằng động và tuân theo nguyên lí chuyển dịch cân bằng Lơ Sa-tơ-li-ê.
Các dạng bài tập về sự điện li
Dạng 1: Xác định chất điện li
Phương pháp giải
Những chất tan trong nước phân li ra ion được gọi là những chất điện li.
Các dung dịch axit, bazơ và muối là các chất điện li.
Dạng 2: Phân biệt chất điện li mạnh, chất điện li yếu
Phương pháp giải
+ Chất điện li mạnh
Các axit mạnh: HCl, HNO3, H2SO4…
Các bazơ mạnh: NaOH, Ba(OH)2…
Hầu hết các muối: NaCl, K2SO4…
+ Chất điện li yếu
Axit yếu và trung bình: CH3COOH, HClO, H2S…
Bazơ yếu: Mg(OH)2, Fe(OH)3…
Một số muối: CaCO3, BaSO4…
Dạng 3: Cách nhận dạng phương trình điện li viết đúng của các chất (nếu có)
Phương pháp giải
- Trong phương trình điện li của chất điện li mạnh người ta dùng một mũi tên chỉ chiều của quá trình điện li.
- Trong phương trình điện li của chất điện li yếu người ta dùng hai mũi tên chỉ ngược chiều nhau.
Dạng 4: Xác định nồng độ các ion trong dung dịch chất điện li
Phương pháp giải
Để làm được dạng bài tập này:
- Viết phương trình điện li
- Tính số mol chất điện li đang xét
=> Số mol ion có trong dung dịch chất điện li => Nồng độ ion có trong dung dịch chất điện li.
* Lưu ý: Khi trộn 2 thể tích dung dịch, các em cần tính tổng thể tích dung dịch lúc sau
Dạng 5: Bài toán liên quan đến độ điện li α.
Phương pháp giải
Để làm được dạng bài tập này ta cần:
- Viết phương trình điện li
- Xác định nồng độ chất tại các thời điểm: ban đầu, cân bằng, sau phản ứng.
- Kết hợp cả công thức tính độ điện li để giải quyết được yêu cầu bài toán
Độ điện li: (α) : α = =
Với : n là số phân tử phân li ra ion, nolà số phân tử hòa tan.
C là nồng độ mol chất tan phân li thành ion, Co là nồng độ mol chất hòa tan.
Ví dụ minh hoạ
Ví dụ 1: Phương trình điện li nào sau đây không đúng ?
A. HCl → H+ + Cl-
B. CH3COOH ⇌ CH3COO- + H+
C. H3PO4 → 3H+ + PO43-
D. Na3PO4 → 3Na+ + PO43-
Đáp án: C
Ví dụ 2: Phương trình điện li nào sau đây viết đúng ?
A. H2SO4 ⇌ H+ + HSO4-
B. H2CO3 ⇌ 2H+ + HCO3-
C. H2SO3 → 2H+ + SO32-
D. Na2S ⇌ 2Na+ + S2-
Đáp án: B
Ví dụ 3: Các chất dẫn điện là
A. KCL nóng chảy, dung dịch NaOH, dung dịch HNO3.
B. dung dịch glucozơ , dung dịch ancol etylic , glixerol.
C. KCL rắn khan, NaOH rắn khan, kim cương.
D. Khí HCL, khí NO, khí O3.
Đáp án: A
Ví dụ 4: Dãy các chất đều là chất điện li mạnh là
A. KOH, NaCL, H2CO3.
B. Na2S, Mg(OH)2 , HCl.
C. HClO, NaNO3, Ca(OH)3.
D. HCl, Fe(NO3)3, Ba(OH)2.
Đáp án: D
Ví dụ 5: Trong dung dịch CH3COOH 0,043M, cứ 100 phân tử hòa tan có 2 phân tử phân li thành ion. Nồng độ của ion H+ là
A. 0,001M. B. 0,086M. C. 0,00086M. D. 0,043M.
Đáp án: C
Độ điện li của CH3COOH là 0,02.
CM H+ = 0,043. 0,02 = 0,00086 (mol)
Bài tập tự luyện
Bài 1: Có 4 dung dịch: Natri clorua, rượu etylic, axit axetic, kali sunfat đều có nồng độ 0,1 mol/l. Khả năng dẫn điện của các dung dịch đó tăng dần theo thứ tự nào trong các thứ tự sau:
A. NaCl < C2H5OH < CH3COOH < K2SO4.
B. C2H5OH < CH3COOH < NaCl < K2SO4.
C. C2H5OH < CH3COOH < K2SO4 < NaCl.
D. CH3COOH < NaCl < C2H5OH < K2SO4.
Đáp án: B
Bài 2: Trong dung dịch axit nitric (bỏ qua sự phân li của H2O) có những phần tử nào ?
A. H+, NO3-.
B. H+, NO3-, H2O.
C. H+, NO3-, HNO3.
D. H+, NO3-, HNO3, H2O.
Đáp án: B
Bài 3: Trong dung dịch axit axetic (bỏ qua sự phân li của H2O) có những phần tử nào ?
A. H+, CH3COO-.
B. H+, CH3COO-, H2O.
C. CH3COOH, H+, CH3COO-, H2O.
D. CH3COOH, CH3COO-, H+.
Đáp án: C
Bài 4: Cho các chất: phèn K – Al; C2H5OH; glucozơ; saccarozơ; tinh bột; dầu ăn; CH3COOH; HCOOCH3; CH3CHO; C3H6; Ca(OH)2; CH3COONH4; NaHCO3; KAlO2; C2H4(OH)2; Phèn amoni – sắt. Số chất điện li là:
A. 6 B. 7
C. 9 D. 8
Đáp án: B
Các chất điện li: phèn K – Al (là muối của K và Al); CH3COOH; Ca(OH)2; CH3COONH4; NaHCO3; KAlO2, Phèn amoni – sắt ( muối của sắt và amoni)
Bài 5: Chất nào sau đây không dẫn điện được ?
A. KCl rắn, khan. C. CaCl2 nóng chảy.
B. NaOH nóng chảy. D. HBr hòa tan trong nước
Đáp án: A
Bài 6: Trộn 200 ml dung dịch chứa 12 gam MgSO4 với 300 ml dung dịch chứa 34,2 gam Al2(SO4)3 thu được dung dịch X. Nồng độ ion SO42- trong X là
A. 0,2M. B. 0,8M. C. 0,6M. D. 0,4M.
Đáp án: B
Phản ứng điện li:
MgSO4 → Mg2+ + SO42-
Al2(SO4)3 → 2Al3+ + 3SO42-
nSO42- = 0,4 mol
⇒ CM(SO42-) = 0,4 / 0,5 = 0,8 (M)
Bài 7: Trộn 400 ml dung dịch Fe2(SO4)3 0,2M với 100 ml dung dịch FeCl3 0,3m thu được dung dịch Y. Nồng độ ion Fe3+ trong Y là
A. 0.38M. B. 0,22M. C. 0,19M. D. 0,11M.
Đáp án: A
Bài 8: Một dung dịch chứa các ion : Cu2+ (0,02 mol), K+ (0,10 mol), NO3- (0,05 mol) và SO42- (x mol). Giá trị của x là
A. 0,050. B. 0.070. C. 0,030. D. 0,045.
Đáp án: D
Theo bảo toàn điện tích: 2nCu2+ + nK+ = nNO3- + nSO42-
⇒ 2.0,02 + 0,1 = 0,05 + 2x ⇒ x = 0,045 (mol)
Bài 9: Một dung dịch chứa Mg2+ (0,02 mol), K+ (0,03 mol) , Cl- (0,04 mol) và ion Z (y mol). Ion Z và giá trị của y là
A. NO3- (0,03). B. CO32- (0,015). C. SO42- (0,01). D. NH4+ (0,01)
Đáp án: A
Gọi điện tích của ion Z là x, số mol là y
Theo bảo toàn điện tích: 2nMg2+ + nK+ + (-1)nCl- + xy = 0
⇒ xy = -0,03
Vậy Z là anion
Đáp án phù hợp là A: x = -1, y = 0,03 mol. Anion là NO3-
Nếu x = -2, y = 0,015 mol, anion là CO32- loại, vì ion này tạo kết tủa với Mg2+
Bài 10: Dung dịch X gồm : 0,09 mol Cl- , 0,04 mol Na+ , a mol Fe3+ và b mol SO . Khi cô cạn X thu được 7,715 gam muối khan. Giá trị của a và b lần lượt là
A. 0.05 và 0,05. B. 0,03 và 0,02.
C. 0,07 và 0,08. D. 0,018 và 0,027.
Đáp án: B
Theo bảo toàn điện tích: 3a + 0,04 = 0,09 + 2b (1)
Theo bảo toàn khối lượng: 56a + 0,04. 23 + 0,09. 35,5 + 96b = 7,715 (2)
Giải hệ 1 và 2 ⇒ a = 0,03 và b = 0,02
Xem thêm các dạng câu hỏi và bài tập liên quan khác:
30 bài tập về Sulfuric acid và muối sulfate (2024) có đáp án chi tiết nhất
30 bài tập về Andehit (2024) có đáp án chi tiết nhất
500 Bài tập Hóa 11 Chương 8: Dẫn xuất halogen - Ancol - Phenol (có đáp án)
500 Bài tập Hóa 11 Chương 5: Hiđrocacbon no (có đáp án)
70 Bài tập về Anđehit – Xeton (2024) có đáp án chi tiết nhất











