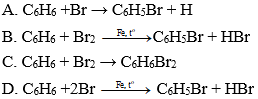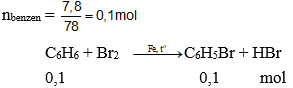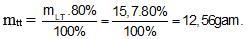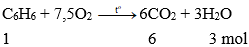Bài tập về Benzen
I. Lý thuyết và phương pháp giải
1. Tính chất vật lý
– Benzen C6H6 là chất lỏng, không màu, không tan trong nước, nhẹ hơn nước.
– Benzen hòa tan nhiều chất như: dầu ăn, cao su, nến, iot,…
– Benzen độc.
2. Cấu tạo phân tử
Từ công thức cấu tạo của benzen, ta thấy sáu nguyên tử cacbon liên kết với nhau tạo thành vòng sáu cạnh đều, có ba liên kết đôi xen kẽ ba liên kết đơn.
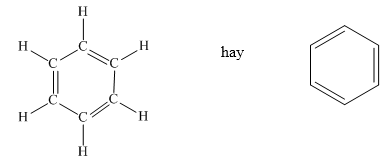
3. Tính chất hóa học
a. Tác dụng với oxi
– Khi đốt benzen cháy trong không khí tạo ra CO2 và H2O, ngọn lửa có nhiều khói đen (muội than)
C6H6 + O2 → 6CO2 + 3H2O
– Muội than sinh ra là do trong không khí không cung cấp đủ oxi để đốt cháy hoàn toàn C6H6
b. Phản ứng thế với với brom
– Benzen không làm mất màu dung dịch brom như etilen và axetilen. Nó chỉ tham gia phản ứng thế với brom lỏng và cần có xúc tác là bột sắt.
C6H6 + Br2 → HBr + C6H5Br (brombenzen)
Benzen chỉ phản ứng với brom nguyên chất, không phản ứng với dung dịch nước brom hay benzen không làm mất màu dung dịch brom ở điều kiện thường.
c. Phản ứng cộng:
– Benzen khó tham gia phản ứng cộng hơn etilen và axetilen. Tuy nhiên, trong điều kiện thích hợp benzen có phản ứng cộng với một số chất như H2, Cl2,…
C6H6 + 3H2 → C6H12
C6H6 + 3Cl2 → C6H6Cl6
(Hexacloxiclohexan) Thuốc trừ sâu 6,6,6
– Do phân tử có cấu tạo đặc biệt nên benzen vừa có phản ứng thế, vừa có phản ứng cộng. Tuy nhiên phản ứng cộng của benzen xảy ra khó hơn etilen và axetilen.
4. Ứng dụng
– Benzen là nguyên liệu quan trọng để sản xuất chất dẻo, phẩm nhuộm, dược phẩm, thuốc trừ sâu..
– Benzen làm dung môi hòa tan nhiều chất hữu cơ trong công nghiệp và trong phòng thí nghiệm.
5. Phương pháp giải
+ Bước 1: Tính số mol các chất đề bài đã cho số liệu và viết phương trình phản ứng hóa học xảy ra.
+ Bước 2: Tính toán luôn theo phương trình phản ứng hóa học hoặc đặt ẩn nếu đề bài là hỗn hợp.
+ Bước 3: Lập phương trình toán học và giải phương trình Số mol các chất cần tìm.
+ Bước 4: Tính toán theo yêu cầu đề bài.
Lưu ý: Trong một hỗn hợp mà có nhiều phản ứng xảy ra thì phản ứng trung hoà được ưu tiên xảy ra trước.
II. Ví dụ minh họa
Ví dụ 1: Phản ứng đặc trưng của benzen là
A. phản ứng cháy.
B. phản ứng trùng hợp.
C. phản ứng thế với brom (có bột sắt xúc tác).
D. phản ứng hóa hợp với brom (có bột sắt xúc tác).
Đáp án: C
Ví dụ 2: Trong các phản ứng sau phản ứng hóa học đúng là
Đáp án: B
Ví dụ 3: Một hợp chất hữu cơ A có phân tử khối là 78 đvC. Vậy A là
A. axetilen.
B. metan.
C. etilen.
D. benzen.
Đáp án: D
III. Bài tập tự luyện
Bài 1: Tính khối lượng benzen cần dùng để điều chế 23,55 gam brombenzen. Biết hiệu suất phản ứng đạt 85%.
A. 11,7 gam.
B. 13,77 gam.
C. 14,625 gam.
D. 9,945 gam.
Lời giải
![]()
Phương trình phản ứng:
C6H6Br + Br2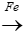 C6H5Br + HBr
C6H5Br + HBr
0,15 ← 0,15 ← 0,15 (mol)
mbenzentheolíthuyết = 0,15.78 = 11,7 gam.
Vì hiệu suất chỉ đạt 85% => khối lượng benzen cần dùng là:
mbenzen = ![]()
Đáp án: B
Bài 2: Cho brom phản ứng với benzen tạo ra brombenzen (bột sắt làm xúc tác). Tính khối lượng benzen cần dùng để điều chế 15,7 gam brombenzen. Biết hiệu suất của quá trình phản ứng là 80%.
A. 9,75 gam.
B. 6,24 gam.
C. 7,80 gam.
D. 10,53 gam
Lời giải
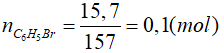
Phương trình hóa học:
![]()
0,1 ← 0,1 (mol)
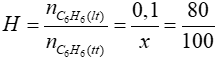
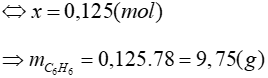
Đáp án: A
Bài 3: Đốt cháy hòa toàn 15,6 gam benzen rồi hấp thụ sản phẩm cháy vào bình đựng dung dịch nước vôi trong dư. Khối lượng dung dịch tăng hay giảm bao nhiêu gam?
A. tăng 56,4 gam.
B. giảm 28,2 gam.
C. giảm 56,4 gam.
D. tăng 28,2 gam
Lời giải
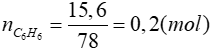
Phương trình hóa học:
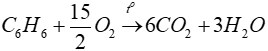
0,2 → 1,2 → 0,6 (mol)
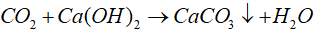
1,2 → 1,2 (mol)
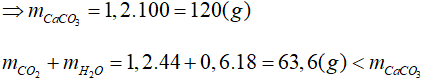
⇒ khối lượng dung dịch giảm là:
120 − 63,6 = 56,4 ( g )
Đáp án: C
Bài 4: Phản ứng nào sau đây không xảy ra?
A. Benzen + Cl2 (as).
B. Benzen + H2 (Ni, p, to).
C. Benzen + Br2 (dd).
D. Benzen + HNO3 (đ)/H2SO4 (đ).
Lời giải
Phản ứng không xảy ra là: benzen + Br2 (dd).
Benzen chỉ phản ứng với brom nguyên chất và có mặt xúc tác Fe, không phản ứng với dung dịch nước brom
Đáp án: C
Bài 5: Tính chất nào không phải của benzen là
A. Dễ thế.
B. Khó cộng.
C. Bền với chất oxi hóa.
D. Kém bền với các chất oxi hóa.
Lời giải
Tính chất nào không phải của benzen là kém bền với các chất oxi hóa.
Đáp án: D
Bài 6: Cho benzen + Cl2 (as) ta thu được dẫn xuất clo A. Vậy A là:
A. C6H5Cl.
B. C6H4Cl2.
C. C6H6Cl6.
D. C6H3Cl3.
Lời giải
Cho benzen + Cl2 (as) ta thu được dẫn xuất clo A.
C6H6 + 3Cl2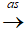 C6H6Cl6
C6H6Cl6
Đáp án: C
Bài 7: Tính chất nào không phải của benzen ?
A. Tác dụng với Br2 (to, Fe).
B. Tác dụng với HNO3 /H2SO4 (đ).
C. Tác dụng với dung dịch KMnO4.
D. Tác dụng với Cl2 (as).
Lời giải
Tính chất không phải của benzen là tác dụng với dung dịch KMnO4
Đáp án: C
Bài 8: Cho 7,8 gam benzen phản ứng với brom dư (có bột sắt xúc tác) hiệu suất phản ứng là 80%. Khối lượng brombenzen thu được là
A. 12,56 gam.
B. 15,7 gam.
C. 19,625 gam.
D. 23,8 gam.
Đáp án: A
Khối lượng brombenzen tính theo lý thuyết là: mLT = 0,1.157 = 15,7 gam.
Do hiệu suất phản ứng là 80% nên khối lượng brombenzen thực tế thu được là:
Bài 9: Đốt cháy chất nào sau đây thu được số mol CO2 lớn hơn số mol nước?
A. metan.
B. etilen.
C. benzen.
D. etilen và benzen.
Đáp án: C
Vậy đốt cháy benzen thu được số mol CO2 lớn hơn số mol nước.
Bài 10: Benzen có ứng dụng nào sau đây?
A. Làm nguyên liệu sản xuất chất dẻo, thuốc trừ sâu, dược phẩm…
B. Làm nhiên liệu trong đèn xì.
C. Làm nguyên liệu sản xuất PE.
D. Kích thích hoa quả mau chín.
Đáp án: A
Bài 11: Tính chất vật lý nào sau đây của benzen là sai?
A. Benzen là chất lỏng, không màu.
B. Benzen độc.
C. Benzen không tan trong nước.
D. Benzen nặng hơn nước.
Đáp án: D
D sai vì benzen nhẹ hơn nước.
Bài 12: Cấu tạo đặc biệt của phân tử benzen là
A. Phân tử có vòng.
B. Phân tử có 3 liên kết đôi.
C. Phân tử có vòng 6 cạnh, chứa các liên kết đôi.
D. Phân tử có vòng 6 cạnh, chứa 3 liên kết đôi xen kẽ với 3 liên kết đơn.
Đáp án: D
Xem thêm các dạng câu hỏi và bài tập liên quan khác:
30 Bài tập về Etilen (2024) có đáp án chi tiết nhất
30 Bài tập về Axetilen (2024) có đáp án chi tiết nhất
30 Bài tập về Dầu mỏ và khí thiên nhiên (2024) có đáp án chi tiết nhất