Giải Sách bài tập Hóa học 10 Bài 2: Thành phần của nguyên tử
Bài 2.1 trang 4 SBT Hóa học 10: Phát biểu nào sau đây là không đúng?
A. Tất cả các nguyên tử đều có proton, neutron và electron.
B. Proton và electron là các hạt mang điện, neutron là hạt không mang điện.
C. Electron tạo nên lớp vỏ nguyên tử.
D. Số lượng proton và electron trong nguyên tử là bằng nhau.
Lời giải:
Đáp án đúng là: A
Nguyên tử hydrogen chỉ gồm proton và electron, không có neutron.
Bài 2.2 trang 4 SBT Hóa học 10: Chọn từ thích hợp điền vào chỗ trống trong mỗi phát biểu sau:
a) Trong nguyên tử, khối lượng tập trung chủ yếu ở …..
b) Kích thước hạt nhân rất ….. so với kích thước nguyên tử.
c) Trong nguyên tử, phần không gian ….. chiếm chủ yếu.
d) Trong thí nghiệm của Thomson, hạt tạo nên tia âm cực là …..
Lời giải:
a) Trong nguyên tử, khối lượng tập trung chủ yếu ở hạt nhân.
b) Kích thước hạt nhân rất nhỏ so với kích thước nguyên tử.
c) Trong nguyên tử, phần không gian rỗng chiếm chủ yếu.
d) Trong thí nghiệm của Thomson, hạt tạo nên tia âm cực là electron.
Bài 2.3 trang 4 SBT Hóa học 10: Những phát biểu nào sau đây là đúng?
A. Nếu một nguyên tử có 17 electron thì nguyên tử đó cũng có 17 proton.
B. Nếu một nguyên tử có 17 electron thì nguyên tử đó cũng có 17 neutron.
C. Nếu một nguyên tử có 17 electron thì ion tạo ra từ nguyên tử đó có 17 proton.
D. Nếu một nguyên tử có 17 electron thì ion tạo ra từ nguyên tử đó có 17 neutron.
E. Nếu một nguyên tử có 17 electron thì ion tạo ra từ nguyên tử đó có 17 electron.
Lời giải:
Đáp án đúng là: A và C
Trong nguyên tử, số proton bằng số electron. Các ion được tạo ra từ nguyên tử đó có số proton bằng số proton của nguyên tử nhưng khác số electron.
B sai vì số neutron trong nguyên tử có thể bằng hoặc khác số electron, không thể xác định số neutron của nguyên tử bằng cách dựa vào số electron.
D sai vì không thể xác định số neutron của ion bằng việc dựa vào số electron.
E sai vì số electron của ion khác số electron của nguyên tử. Nếu nguyên tử mất electron thì tạo ion dương; nếu nguyên tử nhận electron thì tạo ion âm.
|
Loại hạt |
Khối lượng (amu) |
Điện tích (e0) |
|
(1) |
(2) |
0 |
|
(3) |
0,00055 |
(4) |
|
(5) |
(6) |
(7) |
Lời giải:
|
Loại hạt |
Khối lượng (amu) |
Điện tích (e0) |
|
neutron |
1 |
0 |
|
electron |
0,00055 |
-1 |
|
proton |
1 |
+1 |
Bài 2.5 trang 4 SBT Hóa học 10: Những phát biểu nào dưới đây không đúng?
A. Điện tích của proton và electron có cùng độ lớn nhưng ngược dấu.
B. Có những nguyên tử không chứa neutron nào.
C. Một số nguyên tử không có bất kì proton nào.
D. Điện tích của proton và neutron có cùng độ lớn nhưng ngược dấu.
E. Trong nguyên tử, số hạt proton luôn bằng số hạt electron.
G. Khối lượng của proton và neutron xấp xỉ bằng nhau và lớn hơn nhiều khối lượng của electron.
Lời giải:
Đáp án đúng là C và D.
Phát biểu C sai vì nguyên tử bắt buộc phải có proton.
Phát biểu D sai vì neutron không mang điện.
A. Nguyên tử đồng có 29 electron.
B. Hạt nhân nguyên tử đồng trên có tổng số hạt là 63.
C. Ion Cu+ có 28 electron.
D. Ion Cu+ có 30 electron.
E. Ion Cu+ có 28 proton.
Lời giải:
Đáp án đúng là: A, B, C
A đúng vì nguyên tử đồng có số electron = số proton = 29.
B đúng vì số hạt trong hạt nhân nguyên tử đồng = 29 + 34 = 63.
C đúng, D sai vì Cu nhường 1 electron tạo ion Cu+. Số electron của Cu+ = 29 – 1 = 28.
E sai vì ion Cu+ có số proton là 29 (bằng số proton của Cu).
H2+H+2→H+H+3
Biết nguyên tử H có 1 proton và 1 electron. Số proton, neutron và electron của ion H+3 lần lượt là
A. 2 p; 1 n và 1 e.
B. 2 p; 1 n và 2 e.
C. 3 p; 0 n và 1 e.
D. 3 p; 0 n và 2 e.
Lời giải:
Đáp án đúng là: D
+ Số proton của ion H+3 bằng tổng số proton của 3 nguyên tử H là 3.
+ Nguyên tử H không có neutron nên ion H+3 cũng không có neutron.
+ Vì ion H+3 mang điện tích 1+ nên số proton nhiều hơn số electron là 1, vậy ion H+3 có 2 electron.
|
Cột A |
Cột B |
|
a) Phân tử CO b) Phân tử CO2 |
1. có số proton và số neutron bằng nhau. 2. có khối lượng xấp xỉ 28 amu. 3. có khối lượng xấp xỉ 44 amu. 4. có 22 electron. 5. có số hạt mang điện nhiều gấp hai lần số hạt không mang điện. |
Lời giải:
a nối với 1, 2, 5.
b nối với 1, 3, 4, 5.
Giải thích:
- Phân tử CO:
+ Có số proton = số neutron = 6 + 8 = 14
+ Khối lượng = (6 . 1 + 6 . 1) + (8 . 1 + 8 . 1) = 28 amu
+ Số hạt mang điện là 2 . (6 + 8) = 28 gấp đôi số hạt không mang điện là 14
- Phân tử CO2:
+ Có số proton = số neutron = số electron = 6 + 8 . 2 = 22
+ Khối lượng = (6 . 1 + 6 . 1) + 2.(8 . 1 + 8 . 1) = 44 amu
+ Số hạt mang điện là 2 . (6 + 8.2) = 44 gấp đôi số hạt không mang điện là 22
A. 11 proton và 10 electron.
B. 11 proton và 11 electron.
C. 10 proton và 11 electron.
D. 10 proton và 10 electron.
Lời giải:
Đáp án đúng là: A
|
Nguyên tử/ ion |
Số proton |
Số electron |
|
N |
7 |
7 |
|
H |
1 |
1 |
|
NH4+ |
7 + 4 . 1 = 11 |
7 + 4 . 1 – 1 = 10 |
Lời giải:
Đường kính hạt nhân nguyên tử trong mô hình bằng: 1 × 10-5 = 10-5 m = 0,01 mm.
0,01 mm rất nhỏ nên mô hình hạt nhân nguyên tử này không thể chế tạo được bằng dụng cụ thông thường và không phù hợp để quan sát được bằng mắt thường.
Biết rằng 1 fm = 10-15 m, 1 pm = 10-12m.
Lời giải:
Coi nguyên tử và hạt nhân nguyên tử có dạng hình cầu.
Đổi 2,7 fm = 2,7 × 10-15 m.
70 pm = 70 × 10-12 m = 7 × 10-11 m.
Thể tích của hạt nhân nguyên tử là:
Vhn=43πr3hn=43π(2,7×10−15)3=8,24.10−44(m3)
Thể tích của nguyên tử là: Vnt=43πr3nt=43π(7×10−11)3=1,44.10−30(m3)
Phần trăm thể tích nguyên tử carbon bị chiếm bởi hạt nhân là:
8,24×10−441,44×10−30×100%=5,72×10−12%
Lời giải:
Do kích thước hạt nhân bằng 10-5 lần kích thước nguyên tử nên nếu giả thiết chỉ còn x hạt nhân nguyên tử sắp xếp chặt khít cạnh nhau trong một khối cầu thì bán kính Trái Đất còn:
6 371 × 10-5 = 0,06371 km = 63,71 m.
Hay bán kính Trái Đất khi đó nhỏ đi 105 lần.
a) Tính khối lượng riêng của neutron, coi neutron có dạng hình cầu.
b) Giả sử một ngôi sao neutron có cùng khối lượng riêng với neutron, hãy tính khối lượng (theo kg) của một mảnh ngôi sao neutron có kích thước bằng một hạt cát hình cầu với bán kính 0,10 mm.
Lời giải:
a) Khối lượng của 1 neutron ≈ 1u ≈ 1,6605 × 10-27 kg.
Coi neutron có dạng hình cầu, thể tích của 1 neutron là:
V=43πr3=43π(1×10−13)3=4,1867×10−39cm3=4,1867×10−45m3
Khối lượng riêng của neutron là: d=mV=1,6605.10−274,1867.10−45=3,9661.1017kg/m3
b) Thể tích của mảnh sao là:
V=43πr3=43π(0,1)3=0,0041867 (mm3)=4,1867.10−12(m3)
Khối lượng của mảnh sao là:
m = d. V = 3,9661 × 1017 × 4,1867 × 10-12 = 1,6605 × 106 kg = 1660,5 tấn.
a) Hãy cho biết trong trường hợp này, cơ thể chúng ta đã nhận thêm hay mất đi electron.
b) Tổng khối lượng của các electron mà cơ thể đã nhận thêm hoặc mất đi là bao nhiêu kilôgam? Cho khối lượng của 1 electron là 9,1 × 10-31 kg.
Biết rằng 1 μC = 10-6 C.
Lời giải:
a) Do cơ thể tích một lượng điện tích âm nên đã nhận thêm electron.
b) Điện tích của 1 electron là – 1,602 × 10-19 C.
Số lượng electron ứng với điện tích – 10 μC (micrôculông) là: −10×10−6−1,602×10−19=6,242×1013(electron)
Tổng khối lượng electron là: 9,1 × 10-31 × 6,242 × 1013 = 5,7 × 10-17 (kg).
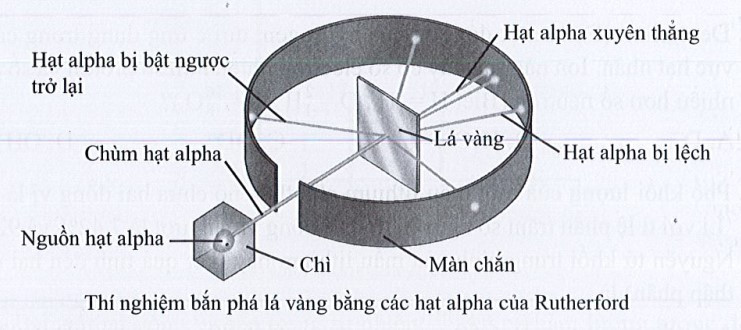
- Hầu hết các hạt α xuyên thẳng qua lá vàng.
- Một số ít hạt α bị lệch quỹ đạo so với ban đầu.
- Một số rất ít hạt α bị bật ngược trở lại.
Từ kết quả này, em có nhận xét gì về cấu tạo nguyên tử?
Lời giải:
Trong thí nghiệm của Rutherford, khi sử dụng các hạt alpha (ion He2+, kí hiệu là α) bắn vào lá vàng thì:
- Hầu hết các hạt α xuyên thẳng qua lá vàng chứng tỏ nguyên tử có cấu tạo rỗng.
- Một số ít hạt α bị lệch quỹ đạo so với ban đầu chứng tỏ hạt nhân nguyên tử cùng điện tích dương như hạt hạt alpha (ion He2+, kí hiệu là α).
- Một số rất ít hạt α bị bật ngược trở lại chứng tỏ kích thước hạt nhân nhỏ hơn rất nhiều so với kích thước của nguyên tử và khối lượng nguyên tử tập trung chủ yếu ở hạt nhân.
Xem thêm lời giải sách bài tập Hóa học lớp 10 Cánh diều với cuộc sống hay, chi tiết khác:
Bài 4: Cấu trúc lớp vỏ electron của nguyên tử




