Giải Sách bài tập Hóa học 10 Bài 17: Nguyên tố và đơn chất halogen
A. Có 7 electron hóa trị.
B. Theo chiều tăng dần của điện tích hạt nhân nguyên tử thì độ âm điện giảm.
C. Theo chiều tăng dần điện tích hạt nhân nguyên tử thì khả năng hút cặp electron liên kết giảm.
D. Theo chiều tăng dần điện tích hạt nhân nguyên tử thì bán kính nguyên tử giảm.
Lời giải:
Đáp án đúng là: D
Phát biểu D không đúng vì: Trong nhóm VIIA, theo chiều tăng dần điện tích hạt nhân nguyên tử thì bán kính nguyên tử tăng.
Bài 17.2 trang 56 SBT Hóa học 10:
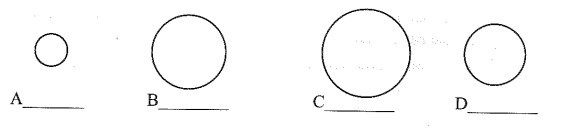
b) Viết công thức phân tử đơn chất của mỗi nguyên tố tương ứng.
c) Ở điều kiện nhiệt độ, áp suất thông thường, các đơn chất này tồn tại ở trạng thái nào? Từ đó, dự đoán thứ tự tăng nhiệt độ nóng chảy, nhiệt độ sôi tương ứng giữa chúng trong cùng điều kiện áp suất.
Lời giải:
a) Từ fluorine đến iodine bán kính nguyên tử tăng dần. Ta có kết quả điền như sau:
A: Fluorine, F;
B: Bromine, Br;
C: Iodine, I;
D: Chlorine, Cl.
b) Công thức phân tử đơn chất của mỗi nguyên tố tương ứng:
A: Fluorine, F2;
B: Bromine, Br2;
C: Iodine, I2;
D: Chlorine, Cl2.
c) Trạng thái các đơn chất ở điều kiện nhiệt độ, áp suất thông thường:
|
Đơn chất |
F2 |
Cl2 |
Br2 |
I2 |
|
Trạng thái |
Khí |
Khí |
Lỏng |
Rắn |
Từ trạng thái này dự đoán nhiệt độ nóng chảy, nhiệt độ sôi của các halogen tăng dần theo thứ tự: F2, Cl2, Br2, I2.
Bài 17.3 trang 56 SBT Hóa học 10: Nguyên nhân dẫn đến nhiệt độ nóng chảy, nhiệt độ sôi của các đơn chất halogen tăng từ fluorine đến iodine là do từ fluorine đến iodine,
A. khối lượng phân tử và tương tác van der Waals đều tăng.
B. tính phi kim giảm và tương tác van der Waals tăng.
C. khối lượng phân tử tăng và tương tác van der Waals giảm.
D. độ âm điện và tương tác van der Waals đều giảm.
Lời giải:
Đáp án đúng là: A
Nguyên nhân dẫn đến nhiệt độ nóng chảy, nhiệt độ sôi của các đơn chất halogen tăng từ fluorine đến iodine là do từ fluorine đến iodine, khối lượng phân tử và tương tác van der Waals đều tăng.
Bài 17.4 trang 57 SBT Hóa học 10: Phát biểu nào sau đây là không đúng khi nói về đơn chất nhóm VIIA?
A. Tính chất đặc trưng là tính oxi hoá.
B. Màu sắc đậm dần từ fuorine đến iodine.
C. Từ fluorine đến bromine rồi iodine, trạng thái của các đơn chất chuyển từ khí đến lỏng rồi rắn.
D. Khả năng phản ứng với nước tăng từ fluorine đến iodine.
Lời giải:
Đáp án đúng là: D
Phát biểu D không đúng vì: Khả năng phản ứng với nước giảm từ fluorine đến iodine.
A. Tính oxi hoá giảm dần từ fluorine đến iodine.
B. Phản ứng với nhiều kim loại, tạo thành hợp chất ion. Phản ứng với một số phi kim, tạo thành hợp chất cộng hoá trị.
C. Khi phản ứng với đơn chất hydrogen, các đơn chất nhóm VIIA thể hiện tính khử.
D. Khi phản ứng với đơn chất hydrogen, mức độ phản ứng giảm dần từ fluorine đến iodine.
Lời giải:
Đáp án đúng là: A, B, D
Phát biểu C sai vì: Khi phản ứng với đơn chất hydrogen, các đơn chất nhóm VIIA thể hiện tính oxi hóa.
|
Cột A |
Cột B |
|
a) Chlorine, Cl2 b) Iodine, I2 |
1. Hầu như không tan trong nước. 2. Là chất khí ở điều kiện thường. 3. Là chất rắn ở điều kiện thường. 4. Là chất oxi hoá khi phản ứng với kim loại. 5. Có độc tính cao. 6. Có tương tác van der Waals mạnh nhất trong nhóm đơn chất halogen. 7. Dùng để xử lí nước sinh hoạt. |
Lời giải:
- a ghép với 2, 4, 5, 7
a) Chlorine, Cl2:
2. Là chất khí ở điều kiện thường.
4. Là chất oxi hoá khi phản ứng với kim loại.
5. Có độc tính cao.
7. Dùng để xử lí nước sinh hoạt.
- b ghép với 1, 3, 4, 6
b) Iodine, I2:
1. Hầu như không tan trong nước.
3. Là chất rắn ở điều kiện thường.
4. Là chất oxi hoá khi phản ứng với kim loại.
6. Có tương tác van der Waals mạnh nhất trong nhóm đơn chất halogen.
A. Các phản ứng đều phát nhiệt mạnh và kèm hiện tượng nổ.
B. Phản ứng giữa fluorine với hydrogen diễn ra mãnh liệt nhất.
C. Điều kiện và mức độ phản ứng phù hợp với xu hướng giảm dần tính oxi hóa từ fluorine đến iodine.
Lời giải:
Đáp án đúng là: B, C, D
A sai vì phản ứng giữa H2 và Br2 cần đun nóng, phản ứng diễn ra chậm; phản ứng giữa I2 và H2 cần đun nóng để diễn ra, phản ứng là thuận nghịch.
A. Các đơn chất nhóm VIIA vừa thể hiện tính oxi hoá, vừa thể hiện tính khử; mức độ phản ứng giảm dần từ fluorine đến iodine.
B. Fluorine phản ứng rất mạnh với nước tạo dung dịch có tính oxi hoá mạnh, có thể dùng để sát khuẩn.
C. Phản ứng của bromine hoặc chlorine với nước đều là phản ứng thuận nghịch.
D. Iodine tan rất ít và hầu như không phản ứng với nước.
Lời giải:
Đáp án đúng là: C, D
A sai vì fluorine chỉ thể hiện tính oxi hóa.
B sai vì 2F2 + 2H2O → O2 + 4HF; HF có tính oxi hóa yếu và không được dùng để sát khuẩn.
A. Bromine phản ứng dễ dàng với dung dịch sodium fluoride để tạo ra đơn chất fluorine.
B. Khi cho vào dung dịch sodium chloride, fluorine sẽ ưu tiên phản ứng với nước.
C. Có thể sục khí chlorine vào dung dịch chứa potassium iodide để thu được iodine.
D. Iodine khó tan trong dung dịch sodium chloride.
Lời giải:
Đáp án đúng là: A
Bromine không phản ứng với dung dịch sodium fluoride.
A. Khí chlorine có thể được dùng để tạo môi trường sát khuẩn cho nguồn nước cấp.
B. Khí chlorine phản ứng với dung dịch sodium hydroxide tạo dung dịch nước Javel dùng để sát khuẩn trong công nghiệp và trong gia đình.
C. Khí chlorine được sử dụng để sản xuất hydrogen chloride, từ đó tạo hydrochloric acid.
D. Do có độc tính, khí chlorine được sử dụng để trừ sâu trong nông nghiệp.
Lời giải:
Đáp án đúng là: D
Khí chlorine không được sử dụng để trừ sâu trong nông nghiệp.
Bài 17.11 trang 58 SBT Hóa học 10: Những phát biểu nào sau đây là đúng?
A. Đơn chất chlorine có tính oxi hóa mạnh hơn đơn chất bromine và iodine.
B. Tương tác van der Waals của các đơn chất halogen tăng từ fluorine đến iodine đã góp phần làm tăng nhiệt độ sôi của chúng.
C. Thành phần của nước bromine gồm các chất: Br2, H2O, HBr, HBrO.
D. Hóa trị phổ biến của nguyên tố halogen là 1.
E. Đơn chất iodine phản ứng được với nước và với dung dịch sodium bromide.
Lời giải:
Đáp án đúng là: A, B, C, D
Phát biểu E sai vì iodine hầu như không phản ứng với nước và không phản ứng với dung dịch sodium bromide.
Lời giải:
Dung dịch nước chlorine gồm nước; hydrochloric acid (HCl); hypochlorous acid (HClO) và chlorine.
Nhúng giấy quỳ vào dung dịch nước chlorine thì thấy giấy quỳ chuyển sang màu đỏ do trong dung dịch nước chlorine có chứa các acid.
Nhưng ngay sau đó, màu đỏ trên giấy quỳ sẽ biến mất vì HClO có tính oxi hóa mạnh có thể phá hủy các hợp chất màu.
Lời giải:
Nước sinh hoạt (nước máy) có chứa hàm lượng chlorine (trong ngưỡng cho phép với con người). Để đảm bảo sức sống cho cá cảnh, người ta không cho trực tiếp nước sinh hoạt (nước máy) vào bồn cá. Nước này phải được chứa trong xô, thau, chậu khoảng một ngày rồi mới được cho vào bồn nuôi cá nhằm làm giảm lượng chlorine dư trong nước sinh hoạt (chlorine dư phát tán vào không khí).
a) Các hoá chất nào thường được sử dụng để xử lí vi khuẩn có trong nước hồ bơi?
b) Nhờ đâu mà các hoá chất ấy giúp xử lý vi khuẩn có trong nước hồ bơi?
c) Để bảo đảm an toàn cho người bơi trong hồ, cần lưu ý gì khi sử dụng các hoá chất ấy?
Lời giải:
a) Do khó bảo quản trong vận chuyển và lưu trữ, nước chlorine ít được sử dụng để khử khuẩn nước hồ bơi.
Trong thực tế người ta sử dụng nước Javel hoặc chlorine 70 (Ca(OCl)2 hay Ca(ClO)2, calcium hypochlorite dạng bột, dễ bảo quản, lưu trữ và sử dụng).
Ngoài ra người ta còn sử dụng hóa chất TCCA 90 dạng viên chứa hợp chất trichloroisocyanuric (C3Cl3N3O3).
b) Các hóa chất này giúp khử khuẩn trong nước hồ bơi do cung cấp hàm lượng ion hypochlorite có tính oxi hóa mạnh.
c) Để bảo đảm an toàn cho người bơi trong hồ, cần sử dụng hóa chất này theo đúng tỉ lệ nhất định được tính toán kĩ với lượng nước trong hồ và hàm lượng tồn dư các hóa chất này trong nước phải đạt tiêu chuẩn cho phép.
A. 0,10 mol.
B. Ít hơn 0,06 mol.
C. Nhiều hơn 0,12 mol.
D. 0,07 mol.
Lời giải:
Đáp án đúng là: B
Phản ứng có thể được viết như sau:
Theo đặc điểm của phản ứng: Khi 1 mol hỗn hợp muối (NaBr; KBr) chuyển thành 1 mol hỗn hợp muối (NaCl; KCl) thì khối lượng giảm:
80 – 35,5 = 45,5 (gam)
Theo đề bài: Khối lượng muối trong thí nghiệm đã giảm 4,45 gam.
Vậy nmuối = nCl- phản ứng =
Nên
Bài 17.16 trang 59 SBT Hóa học 10:
A. Sulfuric acid 98%.
B. Sodium hydroxide khan.
C. Calcium oxide khan.
D. Dung dịch sodium chloride bão hòa.
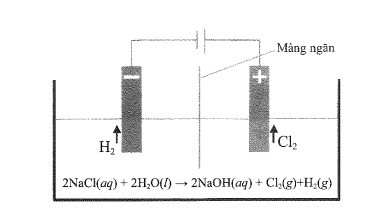
b) Từ quá trình điện phân nêu trên, một lượng chlorine và hydrogen sinh ra được tận dụng để sản xuất hydrochloric acid đặc thương phẩm (32%, D = 1,153 g mL-1 ở 30oC).
Một nhà máy với quy mô sản xuất 200 tấn xút mỗi ngày thì đồng thời sản xuất được bao nhiêu m3 acid thương phẩm trên. Biết rằng, tại nhà máy này, 60% khối lượng chlorine sinh ra được dùng tổng hợp hydrochloric acid và hiệu suất của toàn bộ quá trình từ chlorine đến acid thương phẩm đạt 80% về khối lượng.
Lời giải:
a) Đáp án đúng là: A
Chất được dùng làm khô chlorine phải hút được nước và không tác dụng với chlorine.
Vậy sulfuric acid 98% thỏa mãn.
b) Khối lượng acid thương phẩm được tạo ra cùng 200 gam xút:
Khối lượng dung dịch acid thương phẩm 32% được tạo ra cùng 200 gam xút:
Thể tích dung dịch acid thương phẩm 32% được tạo ra cùng 200 gam xút:
Vậy với 200 tấn = 200 × 106 gam xút thì lượng acid thương phẩm được tạo thành tương ứng là: 237,4 × 106 (mL) = 237,4 (m3).
Vai trò của KI trong phản ứng trên là gì?
C. Vừa là chất oxi hóa, vừa là chất khử.
D. Không phải là chất oxi hóa cũng không phải là chất khử.
Lời giải:
Đáp án đúng là: D
Có thể nhận thấy potassium không thay đổi số oxi hóa (+1 trong các hợp chất).
Số oxi hóa của iodine trong đơn chất và potassium iodide lần lượt là 0 và -1 và giữa chúng không có số oxi hóa trung gian.
Như vậy, trong phản ứng này không có sự thay đổi số oxi hóa của các nguyên tố, do đó không phải là phản ứng oxi hóa – khử.
Thực tế, phản ứng này là sự kết hợp giữa ion I- và phân tử I2 tạo ion I3- bằng một liên kết cho – nhận.
Trong thực tế, phản ứng này giúp chuyển iodine (I2, ít tan trong nước) thành ion triodine (I3-, tan tốt trong nước) phân tán dễ dàng vào dung dịch. Dung dịch này có tính sát khuẩn.
A. +1 và -1.
B. -1.
C. 0 và -1.
D. 0.
Lời giải:
Đáp án đúng là: A
CaOCl2 là muối hỗn tạp, được tạo nên bởi 1 cation kim loại và 2 anion gốc axit.
Công thức cấu tạo của CaOCl2 là:
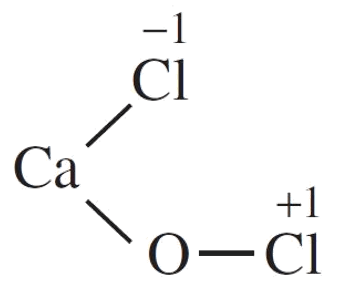
Bài 17.19 trang 60 SBT Hóa học 10: Xét các phản ứng:
với X lần lượt là Cl, Br, I.
Giá trị năng lượng liên kết (kJ mol-1) một số chất được cho trong Phụ lục 2, SGK Hóa học 10, Cánh Diều.
a) Hãy tính biến thiên enthalpy chuẩn của mỗi phản ứng (*).
b) Hãy sắp xếp các phản ứng (*) theo thứ tự giảm dần của nhiệt lượng tỏa ra.
Lời giải:
a) Xét các phản ứng:
Biến thiên enthalpy chuẩn được tính theo công thức:
Với phản ứng:
Cl2(g) + H2(g) → 2HCl(g)
= (243 + 436) – 2 × 431 = -183 (kJ)
Với phản ứng:
Br2(g) + H2(g) → 2HBr(g)
= (193 + 436) – 2 × 364 = -99 (kJ).
Với phản ứng:
I2(g) + H2(g) → 2HI(g)
= (151 + 436) – 2 × 297 = -7 (kJ).
b) Nhiệt lượng tỏa ra trong phản ứng của Cl2 > Br2 > I2.
Phản ứng có giá trị biến thiên enthalpy chuẩn càng âm thì tỏa nhiệt càng nhiều.
Bài 17.20 trang 61 SBT Hóa học 10: Từ bảng giá trị năng lượng liên kết (kJ mol-1) dưới đây:

Hãy cho biết:
a) Liên kết nào bền nhất, liên kết nào kém bền nhất?
b) Giá trị biến thiên enthalpy chuẩn của hai phản ứng sau là bao nhiêu?
F2(g) + H2(g) → 2HF(g) (1)
O2(g) + 2H2(g) → 2H2O(g) (2)
c) Trong hai phản ứng (1) và (2), phản ứng nào tỏa nhiệt nhiều hơn?
Lời giải:
a) Liên kết bền nhất là H – F. Năng lượng liên kết càng lớn thì liên kết càng bền.
b) F2(g) + H2(g) → 2HF(g) (1)
= 159 + 436 – 2 × 565 = -535 (kJ).
O2(g) + 2H2(g) → 2H2O(g) (2)
= 498 + 2 × 436 – 4 × 464 = -486 (kJ).
c) Phản ứng (1) tỏa nhiều nhiệt hơn. Phản ứng có giá trị biến thiên enthalpy chuẩn âm hơn thì sẽ tỏa nhiệt nhiều hơn.
Bài 17.21 trang 61 SBT Hóa học 10: Người ta thường tách bromine trong rong biển bằng quá trình sục khí chlorine vào dung dịch chiết chứa ion bromide. Phương trình hóa học của phản ứng có thể được mô tả dạng thu gọn như sau:
2Br-(aq) + Cl2(aq) → 2Cl-(aq) + Br2(aq)
Cho các số liệu enthalpy tạo thành chuẩn trong bảng dưới đây:

a) Tính biến thiên enthalpy chuẩn phản ứng trên.
b) Phản ứng trên có thuận lợi về năng lượng không?
Lời giải:
a) Với phản ứng:
2Br-(aq) + Cl2(aq) → 2Cl-(aq) + Br2(aq)
Dựa vào enthalpy tạo thành chuẩn của các chất, biến thiên enthalpy chuẩn của phản ứng được tính như sau:
= 2 × (-167,16) + (-2,16) – 2 × (-121,55) – (-17,3) = -76,08 (kJ).
b) Đây là phản ứng tỏa nhiệt nên thuận lợi về mặt năng lượng. Thực tế phản ứng trên diễn ra dễ dàng.
Tỉ lệ số nguyên tử của hai đồng vị cũng là tỉ lệ độ cao h1 và h2 (hay tỉ lệ cường độ tương đối) của hai tín hiệu:
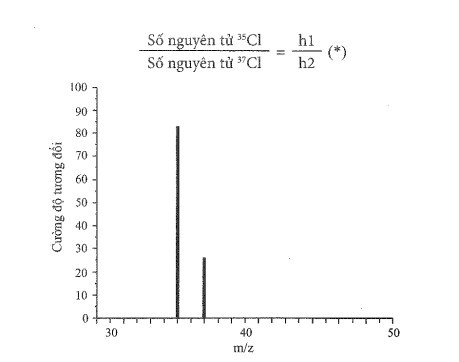
a) Dùng thước (độ chia nhỏ nhất là mm) để đo h1 và h2. Từ đó tính tỉ lệ h1 : h2.
b) Số nguyên tử đồng vị 35Cl gấp bao nhiêu lần số nguyên tử đồng vị 37Cl?
c) Xác định phần trăm số nguyên tử của mỗi đồng vị?
d) Xác định nguyên tử khối trung bình của chlorine.
Lời giải:
a) Dùng thước ta đo được:
h1 = 50 mm; h2 = 15 mm.
Vậy h1 : h2 = 50 : 15 = 10 : 3.
b) Số nguyên tử đồng vị 35Cl gấp lần số nguyên tử đồng vị 37Cl.
c) Phần trăm số nguyên tử của mỗi đồng vị là:
%37Cl = 100% - 76,9% = 23,1%.
d) Nguyên tử khối trung bình của chlorine là:
Xem thêm lời giải sách bài tập Hóa học lớp 10 Cánh diều với cuộc sống hay, chi tiết khác:
Bài 13: Phản ứng oxi hóa – khử
Bài 14: Phản ứng hóa học và enthalpy
Bài 15: Ý nghĩa và cách tính biến thiên enthalpy phản ứng hóa học




