Phản ứng C6H5OH + Br2 → C6H2Br3OH + HBr
1. Phương trình phản ứng Phenol Br2
C6H5OH + 3Br2 → C6H2Br3OH + 3HBr
↓ trắng
2. Điều kiện phản ứng C6H5OH + Br2
Không có
3. Hiện tượng nhận biết phản ứng Phenol tác dụng với brom
Dung dịch Brom (Br2) bị mất màu, dần xuất hiện kết tủa trắng.
4. Bản chất của các chất tham gia phản ứng
4.1. Bản chất của C6H5OH (Phenol)
- Có nhân thơm nên tham gia phản ứng thế H ở vòng benzen tạo kết tủa trắng.
- Do có nhóm OH đẩy e làm tăng mật độ electron trong vòng benzen nên tham gia phản ứng dễ dàng (Chú ý: Phản ứng dùng để nhận biết phenol khi không có mặt anilin)
4.2. Bản chất của Br2 (Brom)
Brom thuộc nhóm halogen nên phản ứng với hidro để tạo thành hidro halogenua.
5. Mở rộng phương trình phản ứng Phenol và Br2
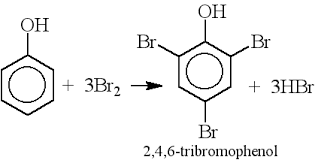
Các bạn có thể viết phương trình dưới dạng cấu tạo để có thể thấy rõ cơ chế phản ứng.
6. Tính chất hóa học của Phenol
6.1.Tác dụng với kim loại kiềm
C6H5OH + Na → C6H5ONa + 1/2 H2↑
6.2. Tác dụng với bazo mạnh tạo muối phenolate
C6H5OH (rắn, không tan) + NaOH → C6H5ONa (tan, trong suốt) + H2O
→ Phenol có tính axit, tính axit của phenol rất yếu; dung dịch phenol không làm đổi màu quỳ tím.
⇒ Có phản ứng:
C6H5ONa (dung dịch trong suốt) + H2O + CO2 → C6H5OH (vẩn đục) + NaHCO3
C6H5OH + Na2CO3 → C6H5ONa + NaHCO3
6.3. Tính chất của nhân thơm - Phản ứng thế H ở vòng benzen
Thế Brom: Phenol tác dụng với dung dịch brom tạo 2,4,6 – tribromphenol kết tủa trắng:
C6H5OH + 3Br2→ C6H2Br3OH + 3HBr
Phản ứng này dùng để nhận biết phenol khi không có mặt của anilin. Phenol tham gia phản ứng thế brom dễ hơn benzen do có nhóm OH đẩy e làm tăng mật độ electron trong vòng benzen.
Thế Nitro: Phenol tác dụng với HNO3 đặc có xúc tác H2SO4đặc, nóng tạo 2,4,6 – trinitrophenol (axit picric):
C6H5OH + 3HNO3 → C6H2(NO2)3OH + 3H2O
7. Bài tập vận dụng
Câu 1. Một dung dịch A chứa 5,4 gam chất đồng đẳng của phenol đơn chức. Cho dung dịch M phản ứng với nước brom (dư), thu được 17,25 gam hợp chất B chứa 3 nguyên tử brom trong phân tử, giả sử phản ứng xảy ra hoàn toàn. Công thức phân tử chất đồng đẳng của phenol là
A.(CH3)2C6H3-OH.
B.CH3 -C6H4-OH.
C.C6H5-CH2-OH.
D.C3H7-C6H4-OH.
Lời giải:
Đáp án: B
Giải thích:
A + 3Br2→ B+ 3HBr
x 3x 3x
nBr2 = nHBr = xnBr2 = nHBr = x
Áp dụng định luật bảo toàn khối lượng ta có:
mA + mBr2 = mhợp chất + mHBr
=> 5,4 + 160.3x = 17,25 + 81.3x => x = 0,05 mol
=> MA = 5,4/0,05 = 108
=> A chỉ có thể là CH3 -C6H4-OH.
Câu 2. Để điều chế axit picric, người ta cho 7,05 gam phenol tác dụng với HNO3 đặc, H2SO4 đặc. Biết lượng axit HNO3đã lấy dư 25% so với lượng cần thiết. Số mol HNO3 cần dùng và khối lượng axit picric tạo thành là :
A. 0,5625 mol; 34,75 gam.
B. 0,5625 mol; 34,35 gam.
C. 0,28125 mol; 17,175 gam.
D. 0,45 mol; 42,9375 gam.
Lời giải:
Đáp án: C
Giải thích:
Phương trình hóa học:
C6H5OH + 3HNO3 → C6H2(NO2)3OH + 3H2O
Phương trình: 94 → 189 → 229 (g)
Theo đề bài m phenol = 7,05 gam
⇒ mHNO3 = 7,05.189/94 = 14,175 gam ⇒ nHNO3 = 0,225 mol
⇒ nHNO3 dùng = 0,225 + 25%.0,225 = 0,28125 mol
maxit picric = 7,05.229/94 = 17,175 gam
Câu 3. Nhận định nào sau đây là đúng về phenol?
A. Phenol làm đổi màu quỳ tím sang đỏ.
B. Phenol là một rượu thơm.
C. Phenol tác dụng được với HCl.
D. Phenol tham gia phản ứng thế brom dễ hơn benzen.
Lời giải:
Đáp án: D
Giải thích:
A Sai: Phenol không làm đổi màu quỳ tím sang đỏ.
B sai: Phenol không phải là một rượu thơm.
C sai Phenol không tác dụng được với HCl.
D đúng: Phenol tham gia phản ứng thế brom dễ hơn benzen.
Câu 4. Có 2 lọ dung dịch mất nhãn là etanol và phenol. Dùng hóa chất nào sau đây để nhận biết 2 lọ trên?
A. Na
B. dung dịch brom
C. HBr
D. KMnO4
Lời giải:
Đáp án: B
Giải thích:
Để nhận biết etanol và phenol ta dùng dung dịch brom. Etanol không phản ứng, phenol làm mất màu dung dịch, tạo kết tủa trắng.
Câu 5. Nếu cho cùng một lượng chất tác dụng với Na hoặc với NaOH thì số mol X phản ứng bằng số mol NaOH và bằng số mol H2 sinh ra. X là
A. CH2(OH)CH2OH
B. HOC6H4-CH2OH
C. HOC6H4OH
D. Tất cả các chất trên.
Lời giải:
Đáp án: B
Giải thích:
Số mol X bằng số mol NaOH phản ứng => X chứa 1 nhóm –OH phenol
Số mol X bằng số mol H2 sinh ra => X chứa 2 nhóm –OH trong phân tử
=> X chứa 1 nhóm –OH phenol và 1 nhóm –OH ancol
Câu 6. Phenol không phản ứng với chất nào sau đây?
A. Na.
B. NaOH.
C. NaHCO3.
D. Br2.
Lời giải:
Đáp án: C
Giải thích:
C6H5OH + 3Br2→ C6H2Br3OH + 3HBr
C6H5OH + Na → C6H5ONa + 1/2H2
C6H5OH + NaOH → C6H5ONa + H2O
Câu 7. Cho các phát biểu sau về phenol:
(a) Phenol vừa tác dụng được với dung dịch NaOH vừa tác dụng được với Na.
(b) phenol tan được trong dung dịch KOH.
(c) Nhiệt độ nóng chảy của phenol lớn hơn nhiệt độ nóng chảy của ancol etylic.
(d) phenol phản ứng được với dung dịch KHCO3 tạo CO2.
(e) Phenol là một ancol thơm.
Trong các trường hợp trên, số phát biểu đúng là
A. 5
B. 2
C. 3
D. 4.
Lời giải:
Đáp án: C
Giải thích:
(a) Phenol vừa tác dụng được với dung dịch NaOH vừa tác dụng được với Na.
(b) phenol tan được trong dung dịch KOH.
(c) Nhiệt độ nóng chảy của phenol lớn hơn nhiệt độ nóng chảy của ancol etylic.
Câu 8. Hợp chất hữu cơ X( phân tử chứa vòng benzen) có công thức phân tử là C7H8O2. Khi X tác dụng với Na dư, số mol H2 thu được bằng số mol X tham gia phản ứng. Mặt khác, X tác dụng được với dung dịch NaOH theo tỉ lệ số mol 1 : 1. Công thức cấu tạo thu gọn của X là
A. C6H5CH(OH)2.
B. HOC6H4CH2OH
C. CH3C6H3(OH)2.
D. CH3OC6H4OH.
Lời giải:
Đáp án: B
Giải thích:
Chất X phản ứng với Na tạo ra nH2 = nX => có 2 nhóm -OH. X phản ứng với NaOH theo tỉ lệ 1:1 => Có 1 nhóm OH gắn vào nhân thơm.
=> X là: X là HOC6H4CH2OH.
=> Đáp án B
Câu 9. Để nhận biết ba lọ mất nhãn: phenol, stiren, ancol benzylic, người ta dùng một thuốc thử duy nhất là:
A. Na
B. Dung dịch NaOH
C. Nước brom
D. Ca(OH)2
Lời giải:
Đáp án: C
Giải thích:
Dùng nước brom, chất nào làm mất màu dung dịch brom ⇒ stiren; chất nào tạo kết tủa trắng với nước brom ⇒ phenol; còn lại không hiện tượng gì là ancol benzylic
Trích mẫu thử và đánh số thứ tự
Để nhận biết các dung dịch trên ta sử dụng thuốc thử dung dịch brom
Cho vài giọt dung dịch brom vào các ống nghiệm đựng các dung dịch trên:
Mẫu thử nào thấy xuất hiện kết tủa trắng, thì chất ban đầu là phenol
C6H5OH + 3Br2 → C6H2Br3OH + 3HBr
Kết tủa trắng
Mẫu thử nào làm mất màu dung dịch brom, thì chất ban đầu là Stiren
C6H5-CH=CH2 + Br2 → C6H5-CHBr-CH2Br
Mẫu thử còn lại không xảy ra hiện tượng gì là ancol benzylic
Câu 10. Khi thổi khí CO2 dư vào dd C6H5ONa muối vô cơ thu được phải là NaHCO3 vì:
A. phênol là chất kết tinh, ít tan trong nước lạnh.
B. tính axit của H2CO3 > C6H5OH > HCO3-.
C. CO2 là một chất khí.
D. Nếu tạo ra Na2CO3 thì nó sẽ bị CO2 dư tác dụng tiếp theo phản ứng: Na2CO3 + CO2 + H2O → 2NaHCO3.
Lời giải:
Đáp án: B
Giải thích:
Ta có H2CO3 có Ka 1 = 4,2 x 10-7; Ka 2 = 4,8 x 10-11; C6H5OH có
Ka = 1,047 x 10-10
→ tính axit của H2CO3 > C6H5OH > HCO3-
Câu 11. Dung dịch A gồm phenol và xiclohexanol trong hexan (làm dung môi). Chia dung dịch A làm hai phần bằng nhau:
-
Phần một cho tác dụng với Na (dư) thu được 3,808 lít khí H2 (đktc).
-
Phần hai phản ứng với nước brom (dư) thu được 59,58 gam kết tủa trắng.
Khối lượng của phenol và xiclohexanol trong dung dịch A lần lượt là:
A. 25,38 g và 15 g
B. 16 g và 16,92 g
C. 33,84 g và 32 g
D. 16,92 g và 16 g
Lời giải:
Đáp án: C
Giải thích:
Gọi số mol trong 1/2 dung dịch A là: nC6H5OH = x mol; nC6H11OH = y mol
nH2 = 1/2. nC6H5OH + 1/2. nC6H11OH = 0,17 mol ⇒ x + y = 0,34 mol
n↓ = nC6H2OHBr3 = nC6H5OH = 0,18 mol ⇒ x = 0,18 ⇒ y = 0,16
⇒ mphenol = 0,18.94.2 = 33,84g; mxiclohexanol = 0,16.100.2 = 32g
Câu 12. Hãy chọn các phát biểu đúng về phenol (C6H5OH):
(1). phenol có tính axit nhưng yếu hơn axit cacbonic;
(2). phenol làm đổi màu quỳ tím thành đỏ;
(3). hiđro trong nhóm –OH của phenol linh động hơn hiđro trong nhóm –OH của etanol,như vậy phenol có tính axit mạnh hơn etanol;
(4). phenol tan trong nước (lạnh) vô hạn vì nó tạo được liên kết hiđro với nước;
(5). axit picric có tính axit mạnh hơn phenol rất nhiều;
(6). phenol không tan trong nước nhưng tan tốt trong dung dịch NaOH.
A. (1), (2), (3), (6).
B. (1), (2), (4), (6).
C. (1), (3), (5), (6).
D. (1), (2), (5), (6).
Lời giải:
Đáp án: C
Giải thích:
(2) sai vì phenol có tính axit rất yếu nên không làm đổi màu quỳ tím.
(4) sai vì phenol tan ít trong nước lạnh, tan vô hạn ở 66oC, tan tốt trong etanol, ete và axeton,...
Có 4 phát biểu đúng là (1), (3), (5), (6)
Câu 13. Phát biểu không đúng là:
A. Dung dịch natri phenolat phản ứng với khí CO2, lấy kết tủa vừa tạo ra cho tác dụng với dung dịch NaOH lại thu được natri phenolat
B. Phenol phản ứng với dung dịch NaOH, lấy muối vừa tạo ra cho tác dụng với dung dịch HCl lại thu được phenol
C. Axit axetic phản ứng với dung dịch NaOH, lấy dung dịch muối vừa tạo ra cho tác dụng với khí CO2 lại thu được axit axetic
D. Anilin phản ứng với dung dịch HCl, lấy muối vừa tạo ra cho tác dụng với dung dịch NaOH lại thu được anilin
Lời giải:
Đáp án: C
Giải thích:
Axit axetic mạnh hơn H2CO3 nên CO2 không thể phản ứng được với muối axetat để tạo axit axetic.
Câu 14. Để nhận biết 3 lọ mất nhãn: phenol, stiren, ancol benzylic, người ta dùng một thuốc thử duy nhất là:
A. Na
B. Dung dịch NaOH
C. Nước brom
D. Ca(OH)2
Lời giải:
Đáp án: C
Trích mẫu thử và đánh số thứ tự
Ta dùng nước brom phản ứng lần lượt với 3 lọ mất nhãn
Nếu xuất hiện ↓ → phenol
C6H5OH + 3Br2 → C6H2Br3OH + 3HBr
Nếu brom mất màu → stiren:
C6H5CH=CH2 + 3Br2 → C6H5CHBr-CH2Br
Nếu không có hiện tượng gì → ancol benzylic.
Câu 15. Hãy chọn phát biểu sai:
A. Phenol có tính axit yếu nhưng mạnh hơn H2CO3.
B. Phenol là chất rắn kết tinh dễ bị oxi hóa trong không khí.
C. Khác với benzen, phenol phản ứng dễ dàng với Br2 tạo kết tủa trắng.
D. Nhóm –OH và gốc phenyl ở phenol có ảnh hưởng qua lại lẫn nhau.
Lời giải:
Đáp án: A
Giải thích: Phenol có tính axit yếu hơn cả H2CO3.
Câu 16. C6H5Cl NaOH→X+(CO2+H2O)→Ydd Br2→Z. Tên gọi của hợp chất Z là:
A. 1,3,5-tribromphenol
B. 2,4,6-tribromphenol
C. 3,5-dibromphenol
D. phenolbromua
Lời giải:
Đáp án: B
Giải thích:
C6H5Cl + 2NaOH to,p→C6H5ONa (X) + NaCl + H2O
C6H5ONa + CO2 + H2O → C6H5OH (Y) + NaHCO3
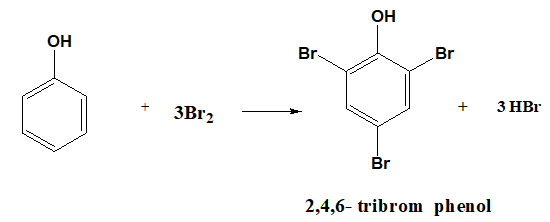
Xem thêm các phương trình hóa học liên quan khác:
C6H5NH2 + Br2 → C6H2Br3NH2 + HBr | C6H5NH2 ra C6H2Br3NH2
C6H5-CH=CH2 + Br2 → C6H5-CHBr-CH2Br | C6H5-CH=CH2 ra C6H5-CHBr-CH2Br
SO2 + Br2 + H2O → HBr + H2SO4 | SO2 ra H2SO4
H2S + Br2 + H2O → H2SO4 + HBr l H2S ra H2SO4
C6H5CH3 + Br2 → C6H5CH2Br + HBr | C6H5CH3 ra C6H5CH2Br | Toluen + Br2 (tỉ lệ 1:1)




