Câu hỏi:
05/01/2024 107
Hãy viết phương trình hóa học để chứng minh chlorine có tính oxi hóa mạnh hơn bromine.
Hãy viết phương trình hóa học để chứng minh chlorine có tính oxi hóa mạnh hơn bromine.
Trả lời:
 Giải bởi Vietjack
Giải bởi Vietjack
Các halogen có tính oxi hóa mạnh hơn sẽ phản ứng với muối halide của halogen có tính oxi hóa yếu hơn để tạo ra các halogen có tính oxi hóa yếu hơn.
Cl2 + 2NaBr → 2NaCl + Br2
\[ \Rightarrow \] Cl2 có tính oxi hóa mạnh hơn sẽ phản ứng với NaBr tạo thành halogen có tính oxi hóa yếu hơn là Br2.
\[ \Rightarrow \] Chlorine có tính oxi hóa mạnh hơn bromine.
Các halogen có tính oxi hóa mạnh hơn sẽ phản ứng với muối halide của halogen có tính oxi hóa yếu hơn để tạo ra các halogen có tính oxi hóa yếu hơn.
Cl2 + 2NaBr → 2NaCl + Br2
\[ \Rightarrow \] Cl2 có tính oxi hóa mạnh hơn sẽ phản ứng với NaBr tạo thành halogen có tính oxi hóa yếu hơn là Br2.
\[ \Rightarrow \] Chlorine có tính oxi hóa mạnh hơn bromine.
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Câu 1:
Phản ứng đốt cháy hoàn toàn 1 mol carbon graphite trong khí oxygen dư (ở điều kiện chuẩn) tạo ra 1 mol CO2, nhiệt lượng toả ra là 393,5 kJ. Nhiệt tạo thành chuẩn của CO2(g) là
Câu 2:
Quá trình Ostwald dùng để sản xuất nitric acid từ ammonia được đề xuất vào năm 1902. Ở giai đoạn đầu của quá trình, ammonia bị oxi hoá bởi oxygen ở nhiệt độ cao khi có chất xúc tác:
4NH3 + 5O2 4NO + 6H2O
Chất bị oxi hoá trong quá trình trên là
Quá trình Ostwald dùng để sản xuất nitric acid từ ammonia được đề xuất vào năm 1902. Ở giai đoạn đầu của quá trình, ammonia bị oxi hoá bởi oxygen ở nhiệt độ cao khi có chất xúc tác:
4NH3 + 5O2 4NO + 6H2O
Chất bị oxi hoá trong quá trình trên là
Câu 3:
Nhỏ vài giọt dung dịch nào sau đây vào dung dịch AgNO3 thu được kết tủa màu vàng nhạt.
Câu 4:
Cho bột Fe vào dung dịch HCl loãng. Sau đó đun nóng hỗn hợp này. Phát biểu nào sau đây không đúng?
Câu 5:
Hydrogen peroxide phân hủy theo phản ứng sau: 2H2O2 → 2H2O + O2.
Tại thời điểm ban đầu, thể tích khí oxygen là 0 cm3, sau thời gian 15 phút thể tích khí oxygen là 16 cm3. Tốc độ trung bình của phản ứng trong 15 phút đầu tiên là
Hydrogen peroxide phân hủy theo phản ứng sau: 2H2O2 → 2H2O + O2.
Tại thời điểm ban đầu, thể tích khí oxygen là 0 cm3, sau thời gian 15 phút thể tích khí oxygen là 16 cm3. Tốc độ trung bình của phản ứng trong 15 phút đầu tiên là
Câu 6:
Cho các phản ứng hóa học sau, phản ứng nào chứng minh Cl2 có tính oxi hoá mạnh hơn Br2?
Câu 7:
Cho phản ứng tạo thành propene từ propyne:
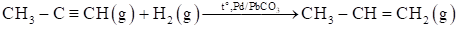
Cho giá trị trung bình của các năng lượng liên kết ở điều kiện chuẩn:
Liên kết
C – H
C – C
C = C
C ≡ C
H - H
Eb (kJ/mol)
413
347
614
839
432
Biến thiên enthalpy chuẩn của phản ứng là
Cho phản ứng tạo thành propene từ propyne:
![]()
Cho giá trị trung bình của các năng lượng liên kết ở điều kiện chuẩn:
|
Liên kết |
C – H |
C – C |
C = C |
C ≡ C |
H - H |
|
Eb (kJ/mol) |
413 |
347 |
614 |
839 |
432 |
Biến thiên enthalpy chuẩn của phản ứng là
Câu 8:
Cho sodium iodide (NaI) tác dụng với potassium permanganate (KMnO4) trong dung dịch sulfuric acid (H2SO4) thu được 3,02 gam manganese(II) sulfate (MnSO4), I2 và Na2SO4.
a) Viết phương trình hoá học xảy ra, chỉ rõ chất khử, chất oxi hoá, quá trình khử, quá trình oxi hoá.
Cho sodium iodide (NaI) tác dụng với potassium permanganate (KMnO4) trong dung dịch sulfuric acid (H2SO4) thu được 3,02 gam manganese(II) sulfate (MnSO4), I2 và Na2SO4.
a) Viết phương trình hoá học xảy ra, chỉ rõ chất khử, chất oxi hoá, quá trình khử, quá trình oxi hoá.
Câu 10:
Bằng phương pháp hóa học, hãy phân biệt các dung dịch sau chứa trong các lọ riêng biệt mất nhãn: HCl, NaCl, NaI.
Bằng phương pháp hóa học, hãy phân biệt các dung dịch sau chứa trong các lọ riêng biệt mất nhãn: HCl, NaCl, NaI.
Câu 11:
Cho lượng dư dung dịch AgNO3 tác dụng với 100 ml dung dịch hỗn hợp NaF 0,05M và NaCl 0,1M. Khối lượng kết tủa thu được là
Câu 13:
Khí oxygen được điều chế trong phòng thí nghiệm bằng cách nhiệt phân potassium chlorate với xúc tác manganes dioxide. Để thí nghiệm thành công và rút ngắn thời gian tiến hành có thể dùng một số biện pháp sau:
(1) Trộn đều bột potassium chlorate và xúc tác.
(2) Nung ở nhiệt độ cao.
(3) Dùng phương pháp dời nước để thu khí oxygen.
(4) Nghiền nhỏ potassium chlorate.
Số biện pháp dùng để tăng tốc độ phản ứng là
Khí oxygen được điều chế trong phòng thí nghiệm bằng cách nhiệt phân potassium chlorate với xúc tác manganes dioxide. Để thí nghiệm thành công và rút ngắn thời gian tiến hành có thể dùng một số biện pháp sau:
(1) Trộn đều bột potassium chlorate và xúc tác.
(2) Nung ở nhiệt độ cao.
(3) Dùng phương pháp dời nước để thu khí oxygen.
(4) Nghiền nhỏ potassium chlorate.
Số biện pháp dùng để tăng tốc độ phản ứng là


