Bài tập Axit cacboxylic
Kiến thức cần nhớ
Định nghĩa, phân loại, danh pháp
1. Định nghĩa
- Axit cacboxylic là những hợp chất hữu cơ mà phân tử có nhóm cacboxyl (-COOH) liên kết trực tiếp với nguyên tử cacbon hoặc nguyên tử hiđro.
- Ví dụ: H-COOH, C2H5COOH, HOOC-COOH
- Nhóm cacboxyl (-COOH) là nhóm chức của axit cacboxylic.
2. Phân loại
Dựa theo đặc điểm cấu tạo của gốc hiđrocacbon và số nhóm cacboxyl trong phân tử, các axit được chia thành:
- Axit no, đơn chức mạch hở, tổng quát (thường gặp):
CnH2n+1COOH (n ≥ 0) hay CmH2mO2 (m ≥ 1)
Ví dụ: H-COOH, C2H5COOH...
- Axit không no, đơn chức, mạch hở:
Ví dụ: CH2=CH-COOH,....
- Axit thơm, đơn chức:
Ví dụ: C6H5-COOH, CH3-C6H4-COOH,...
- Axit đa chức:
Ví dụ: HOOC-COOH, HOOC-CH2-COOH...
3. Danh pháp
a) Tên thường
Một số axit có tên thông thường liên quan đến nguồn gốc tìm ra chúng. Ví dụ:
b) Tên thay thế
Tên thay thế của các axit no, đơn chức, mạch hở được xác định như sau:
+ Mạch chính của phân tử axit là mạch dài nhất, bắt đầu từ nhóm – COOH.
+ Mạch cacbon được đánh số bắt đầu từ nguyên tử cacbon của nhóm – COOH.
+ Tên thay thế =Axit + tên hiđrocacbon no tương ứng với mạch chính + oic.
Ví dụ:
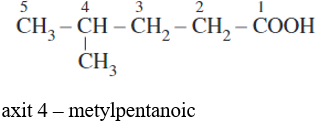
Đặc điểm cấu tạo
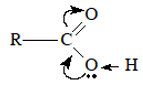
- Nhóm -COOH coi như được kết hợp bởi nhóm C = O và nhóm – OH.
- Liên kết O -H trong phân tử axit phân cực hơn liên kết O–H trong phân tử ancol, do đó nguyên tử H của nhóm COOH linh động hơn nguyên tử H của nhóm – OH ancol.
- Liên kết C- OH của nhóm cacboxyl phân cực mạnh hơn liên kết C – OH của ancol, phenol nên nhóm – OH của axit cacboxylic cũng dễ bị thay thế.
Tính chất vật lý
-Ở điều kiện thường các axit cacboxylic đều là những chất lỏng hoặc rắn.
- Nhiệt độ sôi tăng theo chiều tăng M và cao hơn các ancol có cùng M: nguyên nhân là do giữa các phân tử axit cacboxylic có liên kết hiđro bền hơn liên kết hidro giữa các phân tử ancol.
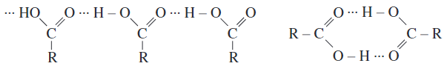
- Mỗi axit có vị riêng: axit axetic có vị giấm ăn, axit oxalic có vị chua của me …
Tính chất hóa học
1.Tính axit
- Trong dung dịch, axit cacboxylic phân li thuận nghịch:
CH3COOH ⇄ H+ + CH3COO-
Dung dịch axit cacboxylic làm quỳ tím chuyển sang màu đỏ
- Tác dụng với bazơ, oxit bazơ tạo thành muối và nước. Ví dụ:
CH3COOH + NaOH → CH3COONa + H2O
2CH3COOH + ZnO → (CH3COO)2Zn + H2O
- Tác dụng với muối:
2CH3COOH + CaCO3 → (CH3COO)2Ca + H2O + CO2
- Tác dụng với kim loại trước hiđro:
2CH3COOH + Zn → (CH3COO)2Zn + H2
2. Phản ứng thế nhóm –OH
- Phản ứng giữa axit và ancol tạo thành este và nước được gọi là phản ứng este hóa.
- Tổng quát:
RCOOH + R’OH RCOOR’ + H2O
- Đặc điểm: phản ứng thuận nghịch, xúc tác H2SO4 đặc.
- Ví dụ:
CH3COOH + C2H5OH CH3COOC2H5 + H2O
Điều chế
1. Phương pháp lên men giấm: (phương pháp cổ truyền sản xuất axit axetic)
C2H5OH + O2 CH3COOH + H2O
2. Oxi hóa anđehit axetic:
2CH3CHO + O2 2CH3COOH
3.Oxi hóa ankan:
2R-CH2-CH2-R’ + 5O2 2RCOOH + 2R’COOH + 2H2O
4.Từ metanol:
CH3OH + CO CH3COOH
Đây là phương pháp hiện đại để sản xuất axit axetic.
Ứng dụng
Các axit hữu cơ có ứng dụng trong nhiều lĩnh vực: làm nguyên liệu cho công nghiệp mĩ phẩm, công nghiệp dệt, công nghiệp hóa học …

Các dạng bài tập Axit cacboxylic
Dạng 1: Đồng đẳng, đồng phân, danh pháp, cấu tạo
Dạng 2: Tính chất, nhận biết, điều chế, ứng dụng
Dạng 3: Bài toán xác định lượng, xác định công thức phân tử, công thức cấu tạo
Bài toán 1: Phản ứng của axit với kim loại, bazơ và muối cacbonat
Phương pháp giải
- Phương trình tổng quát:
R(COOH)x + xNa → R(COONa)x + x/2H2
Theo phương trình:
- Phương trình tổng quát:
R(COOH)x + xNaOH → R(COONa)x + xH2O
Theo phương trình: nCOOH = nOH
- Phương trình tổng quát:
R(COOH)x + xNaHCO3 → R(COONa)x + xCO2 + xH2O
Theo phương trình:
Bài toán 2: Phản ứng đốt cháy
Phương pháp giải
- Đốt cháy axit no, đơn chức, mạch hở:
Nhận xét: .
Chú ý: Khi đốt axit thu được số mol nước bằng số mo khí cacbonic thì đó là axit no, đơn chức, mạch hở. Ngoài ra ta có thể áp dụng các định luật bảo toàn như bảo toàn nguyên tố, bảo toàn khối lượng,...
- Đốt cháy axit không no, một liên kết đôi C = C, đơn chức, mạch hở:
Nhận xét: .
Bài toán 3 : Phản ứng este hóa
Phương pháp giải
Công thức tính hiệu suất :
Chú ý : là số mol đề bài cho sẵn.
là số mol tính theo phương trình.
Ngoài ra, nếu cho sẵn hiệu suất phản ứng (H%) :
neste lí thuyết = neste thực tế : H%
neste thực tế = neste lí thuyết : H%
Bài tập tự luyện
Câu 1: Đun 12 gam axit axetic với 13,8 gam etanol (có H2SO4 đặc làm xúc tác), thu được 11gam este. Hiệu suất của phản ứng este hóa là
A. 44%.
B. 55%.
C. 62,5%.
D. 75 %.
Hướng dẫn giải:
Ban đầu 0,2 0,3 mol
Phản ứng 0,2 0,2 0,2 mol
Khối lượng của este theo lý thuyết là 0,2.88= 17,6 g
Hiệu suất của phản ứng este hóa là:
Đáp án C
Câu 2: Đun nóng 30 gam axit axetic với lượng dư ancol etylic (xúc tác H2SO4 đặc), thu được 26,4 gam este. Hiệu suất của phản ứng este hóa là
A. 40%.
B. 50%.
C. 60%.
D. 70%.
Hướng dẫn giải:
0,5 0,5 mol
Khối lượng của este theo lý thuyết là 0,5.88 = 44 g
Hiệu suất của phản ứng este hóa là:
Đáp án C
Câu 3: Trộn 300ml dung dịch axit axetic 1M và 50 ml ancol etylic 46º (d = 0,8g/ml) có thêm một ít H2SO4 đặc vào một bình cầu và đun nóng bình cầu một thời gian, sau đó chưng cất thu được 18,48 gam este. Hiệu suất của phản ứng este hoá là:
A. 65%
B. 70%
C. 85%
D. 90%
Hướng dẫn giải:
naxit = 0,3 mol; nancol =
Ban đầu: 0,3 0,4 mol
Phản ứng: 0,3 0,3 0,3 mol
Khối lượng este theo lý thuyết là 0,3.88 = 26,4 gam
Hiệu suất phản ứng là:
Đáp án B
Câu 4: Khi thực hiện phản ứng este hóa 1 mol CH3COOH và 1 mol C2H5OH, lượng este lớn nhất thu được là mol. Để đạt hiệu suất cực đại 90% (tính theo axit khi tiến hành este hóa 1 mol CH3COOH cần số mol C2H5OH là bao nhiêu? Biết các phản ứng este hóa thực hiện ở cùng nhiệt độ).
A. 0,342.
B. 0,456.
C. 2,412.
D. 2,925.
Hướng dẫn giải:
Ban đầu: 1 mol 1 mol
Phản ứng:
Sau phản ứng:
=>
Hiệu suất đạt cực đại H = 90% => phản ứng = 1.90% = 0,9 mol
Gọi số mol C2H5OH cần dùng = x mol
Ban đầu: 1 mol x mol
Phản ứng: 0,9 → 0,9 → 0,9 → 0,9
Sau phản ứng: 0,1 x – 0,9 0,9 0,9
Vì 2 phản ứng thực hiện ở cùng nhiệt độ => KC không đổi
=> => x = 2,925 mol
Đáp án D
Câu 5: Đốt cháy hoàn toàn m gam hỗn hợp ancol đơn chức X và Y thuộc cùng 1 dãy đồng đẳng, người ta thu được 35,84 lít CO2 (ở đktc) và 37,8 gam H2O. Nếu cho m gam hỗn hợp trên tác dụng với 24,0 gam axit axetic (hiệu suất là 50%). Khối lượng este thu được là
A. 20 gam.
B. 20,96 gam.
C. 26 gam.
D. 26,4 gam.
Hướng dẫn giải:
Gọi CTTQ của 2 ancol là ROH
nancol = 2,1 – 1,6 = 0,5 mol
Suy ra mancol = mC + mH + mO = 12.1,6 + 2,1.2 + 0,5.16 = 31,4 gam
Mancol = 31,4 : 0,5 = 62,8
Phương trình phản ứng:
Ban đầu: 0,4 0,5 mol
Phản ứng: 0,4 0,4 0,4 mol
Do hiệu suất phản ứng là 50% nên neste = 0,4.0,5 = 0,2 mol
meste = 0,2. (15 + 44 + 45,8) = 20,96 gam
Đáp án B
Câu 6: Đun nóng 6 gam axit axetic với 6 gam ancol etylic (xúc tác H2SO4 đặc, đun nóng), hiệu suất của phản ứng este hóa là 60%. Khối lượng este là
A. 4,4 g
B. 4,6 g
C. 5,2 g
D. 5,28 g
Hướng dẫn giải:
Ban đầu: 0,1 0,13 mol
Phản ứng: 0,1 0,1 0,1 mol
meste lý thuyết = 0,1.88 = 8,8 gam
Do hiệu suất của phản ứng là 60% nên meste thực tế = 5,28g
Đáp án D
Câu 7: Cho hỗn hợp X gồm ancol metylic và hai axit cacboxylic (no, đơn chức, kế tiếp nhau trong dãy đồng đẳng) tác dụng hết với Na, giải phóng 6,72 lít khí H2 (đktc). Nếu đun nóng hỗn hợp X (có xúc tác H2SO4 đặc) thì các chất trong hỗn hợp phản ứng vừa đủ với nhau tạo thành 25 gam hỗn hợp este (hiệu suất của phản ứng este hóa đều bằng 100%). Hai axit trong hỗn hợp X là
A. HCOOH và CH3COOH.
B. CH3COOH và C2H5COOH.
C. C2H5COOH và C3H7COOH.
D. C3H7COOH và C4H9COOH.
Hướng dẫn giải:
Gọi 2 axit có công thức chung là RCOOH.
Khi tham gia phản ứng với Na ta có:
nancol + naxit = 2nhiđro = 2.0,3 = 0,6 mol
Vì các chất trong hỗn hợp phản ứng vừa đủ với nhau và hiệu suất của phản ứng 100% nên naxit = nancol = neste = 0,3 mol
Suy ra Meste = (R + 12 + 32 + 15). 0,3 = 25 R = 24,333
Hai 2 axit là CH3COOH và C2H5COOH.
Đáp án B
Câu 8: Chia a gam axit axetic thành 2 phần bằng nhau:
-Phần 1: Trung hòa vừa đủ bởi 0,5 lít dung dịch NaOH 0,4 M
-Phần 2: Thực hiện phản ứng este hóa với ancol etylic dư thu được m gam este (giả sử hiệu suất phản ứng là 100%)
Vậy m có giá trị là:
A. 16,7 gam
B. 17,6 gam
C. 16,8 gam
D. 18,6 gam
Hướng dẫn giải:
Mà hiệu suất là 100% nên neste =
meste = 0,02.88=17,6 g
Đáp án B
Câu 9: Khi đun nóng 25,8 gam hỗn hợp ancol etylic và axit axetic có H2SO4 đặc làm xúc tác thu được 14,08 gam este. Nếu đốt cháy hoàn toàn lượng hỗn hợp đó thu được 23,4g H2O. Tìm thành phần trăm mỗi chất trong hỗn hợp đầu và hiệu suất của phản ứng este hoá.
A. 53,5% C2H5OH; 46,5% CH3COOH và H = 80%
B. 55,3% C2H5OH; 44,7% CH3COOH và H = 80%
C. 60,0% C2H5OH; 40,0% CH3COOH và H = 75%
D. 45,0% C2H5OH; 55,0% CH3COOH và H = 60%
Hướng dẫn giải:
= 1,3 mol
Đặt a, b là số mol C2H5OH và CH3COOH
⇒ 46a + 60b = 25,8 (1)
và = 3a + 2b = 1,3 (2)
Từ (1) và (2) ⇒ a = 0,3mol và b = 0,2 mol
= 0,16 mol
⇒ H = = 80%
Đáp án A
Câu 10: Cho 20,5 gam hỗn hợp ancol etylic và axit axetic tác dụng với kali dư thu được 4,48 lít H2 (đktc). Nếu cho hỗn hợp đó thực hiện phản ứng este hóa thì khối lượng este thu được là bao nhiêu? Biết H = 100%.
A. 10 gam
B. 12 gam
C. 13,2 gam
D. 14,2 gam
Hướng dẫn giải:
Gọi số mol của ancol và axit lần lượt là x, y mol
x 0,5x mol
y 0,5y mol
Ta có hệ phương trình:
Phản ứng este hóa:
Ban đầu 0,15 0,25 mol
Phản ứng 0,15 0,15 0,15 mol
Khối lượng este là 0,15.88= 13,2g.
Câu 11: Dung dịch axit axetic phản ứng được với tất cả các chất trong dãy nào sau đây?
A. Cu, CuO, HCl.
B. NaOH, Cu, NaCl.
C. Na, NaCl, CuO.
D. NaOH, Na, CaCO3.
Hướng dẫn giải:
CH3COOH không tác dụng với NaCl, Cu, HCl
Đáp án D
Câu 12: Cho 2,5 gam hỗn hợp X gồm HCOOH, CH3COOH, C6H5COOH tác dụng vừa đủ với 400 ml dung dịch NaOH 1M. Khối lượng muối tan có trong dung dịch thu được sau phản ứng là
A. 3,34 g.
B. 33,4 g.
C. 1,13 g.
D. 11,3 g.
Hướng dẫn giải:
nNaOH =0,4 mol
RCOOH + NaOH RCOONa + H2O
0,4 0,4 mol
Bảo toàn khối lượng ta có:
mmuối = mX + mNaOH - mnước = 2,5 + 0,4.40 – 0,4. 18 = 11,3 g
Đáp án D
Câu 13: Cho 5,76 gam axit hữu cơ X đơn chức, mạch hở tác dụng hết với CaCO3 thu được 7,28 gam muối của axit hữu cơ. Công thức cấu tạo của X là
A. HCOOH.
B. CH3COOH.
C. C2H3COOH.
D. C2H5COOH.
Hướng dẫn giải:
Đặt công thức của X là RCOOH.
x 0,5x mol
Theo phương pháp tăng giảm khối lượng ta có:
(2R + 44.2 + 40). 0,5x – (R + 45)x = 7,28 – 5,76
Vậy X là C2H3COOH.
Đáp án C
Câu 14: Cho axit axetic có nồng độ x% tác dụng vừa đủ với dung dịch NaOH có nồng độ 10% thì thu được dung dịch muối có nồng độ 10,25%. Vậy x có giá trị là:
A. 20%.
B. 16%.
C. 17%.
D. 15%.
Hướng dẫn giải:
1 1 mol
Mặt khác:
Đáp án D
Câu 15: Cho 1 gam axit axetic vào ống nghiệm thứ nhất và 1 gam axit fomic vào ống nghiệm thứ 2, sau đó cho vào cả hai ống nghiệm trên một lượng dư bột CaCO3. Khi phản ứng xảy ra hoàn toàn thì thể tích CO2 thu được ở cùng nhiệt độ, áp suất là:
A. Hai ống bằng nhau.
B. Ống 1 nhiều hơn ống 2.
C. Ống 2 nhiều hơn ống 1.
D. Cả hai ống đều nhiều hơn 22,4 lít (đktc).
Hướng dẫn giải:
Vì lượng cho vào là dư nên lượng khí sinh ra ở cả hai ống nghiệm đều tính theo axit.
Ống 1:
1/60 1/30 mol
Ống 2:
1/46 1/23 mol
Ta thấy số mol CO2 ở ống 2 nhiều hơn ống 1 nên thể tích CO2 ở ống 2 nhiều hơn ống 1.
Đáp án C
Câu 16: Cho 6,9 gam hỗn hợp X gồm axit fomic và etanol phản ứng hết với Na dư, thu được V lít khí H2 ở đktc. Giá trị của V là
A. 1,68.
B. 2,24.
C. 3,36.
D. 4,48.
Hướng dẫn giải:
Ta có:
Thể tích hiđro sinh ra là 0,075.22,4 = 1,68 lít
Đáp án A
Câu 17: Cho 16,4 gam hỗn hợp X gồm 2 axit cacboxylic đơn chức là đồng đẳng kế tiếp nhau phản ứng hoàn toàn với 200 ml dung dịch NaOH 1M và KOH 1M, thu được dung dịch Y. Cô cạn dung dịch Y, thu được 31,1 gam hỗn hợp chất rắn khan. Công thức của 2 axit là
A. C2H4O2 và C3H4O2.
B. C2H4O2 và C3H6O2.
C. C3H4O2 và C4H6O2.
D. C3H6O2 và C4H8O2.
Hướng dẫn giải:
nNaOH = 0,2 mol, nKOH = 0,2 mol
Sơ đồ: X + NaOH,KOH→ chất rắn +H2O
Bảo toàn khối lượng ta có:
16,4 + 0,2.40 + 0,2.56 = 31,1+
⇒ = 4,5g ⇒ = 0,25 mol
Do X gồm 2 axit đơn chức
⇒ nX = = 0,25 mol ⇒ MX = 16,4:0,25 = 65,6
⇒2 axit: CH3COOH và C2H5COOH
Đáp án B
Câu 18: Hỗn hợp X chứa ba axit cacboxylic đều đơn chức, mạch hở, gồm một axit no và hai axit không no đều có một liên kết đôi (C=C). Cho m gam X tác dụng vừa đủ với 150 ml dung dịch NaOH 2M, thu được 25,56 gam hỗn hợp muối. Đốt cháy hoàn toàn m gam X, hấp thụ toàn bộ sản phẩm cháy bằng dung dịch NaOH dư, khối lượng dung dịch tăng thêm 40,08 gam. Tổng số mol hai axit cacboxylic không no trong m gam X là
A. 0,1 mol.
B. 0,15 mol.
C. 0,2 mol.
D. 0,25 mol.
Hướng dẫn giải:
nNaOH = 2. 0,15 = 0,3 mol
RCOOH + NaOH → RCOONa + H2O
CnH2nO2 + O2 → n CO2 + nH2O
CnH2n-2O2 + O2 → n CO2 + (n -1) H2O
CO2 + 2NaOH → Na2CO3 + H2O
nX = 0,3 mol ⇒ mX = 25,56 – 0,3.22 = 18,96
Gọi = x và = y mol ⇒ 44x + 18 y = 40,08
mX = 18,96 = 12x + 2y + 0,6.16 ⇒ 12x + 2y = 9,36
⇒ x = 0,69 và y = 0,54
⇒ số mol 2 axit không no = 0,69 – 0,54 = 0,15 mol
Đáp án B
Câu 19: Cho 8,64 gam một axit đơn chức phản ứng với 144 ml dung dịch KOH 1M. Cô cạn dung dịch sau phản ứng được 14,544 gam chất rắn. Công thức của axit là:
A. CH3COOH.
B. C2H3COOH.
C. HCOOH.
D. C2H5COOH.
Hướng dẫn giải:
nKOH = 0,144 mol
Áp dụng ĐLBTKL ta có:
8,64 + 0,144.56 = 14,544 + mnước
mnước = 2,16 g ⇒ = 0,12 mol = naxit
⇒ Maxit = 8,64 : 0,12 = 72
Vậy axit là C2H3COOH.
Đáp án B
Câu 20: Cho một hỗn hợp gồm axit axetic và một axit (X) thuộc dãy đồng đẳng của axit axetic. Để trung hòa hoàn toàn hỗn hợp này thì cần vừa đủ 300ml dung dịch NaOH 0,2M. Cô cạn dung dịch sau phản ứng thu được 5,48 gam muối khan. Biết : nX= 1: 2. Công thức phân tử của X là:
A. HCOOH.
B. C2H5COOH.
C. CH3COOH.
D. C3H7COOH.
Hướng dẫn giải:
nNaOH = 0,06 mol
CH3COOH + NaOH CH3COONa + H2O
x mol x mol
CnH2n+1COOH + NaOH CnH2n+1COONa + H2O
2x mol 2x mol
Ta có: x + 2x = 0,06 x = 0,02 (mol)
= 0,02.(15 + 44+ 23) = 1,64 (gam).
= 0,04.(14n + 68) = (0,56n + 2,72).
Theo đề bài: 1,64 + 0,56n + 2,72 = 5,48
n = 2. Công thức của axit là C2H5COOH.
Đáp án B
Câu 21: Một axit cacboxylic có công thức tổng quát là CnH2n+2-2a-m(COOH)m. Các giá trị n, a, m lần lượt được xác định là
A. n > 0; a 0; m 1.
B. n 0; a 0; m 1.
C. n > 0; a > 0; m >1.
D. n 0; a >0; m 1.
Đáp án B
Câu 22: B là axit cacboxylic mạch hở, chứa no (1 nối đôi C=C), có công thức CxHyOz. Mỗi quan hệ giữa x, y, z là
A. y = 2x – z + 2.
B. y = 2x.
C. y = 2x – z.
D. y = 2x + z – 2.
Hướng dẫn giải:
Do A là axit mạch hở, có chứa 1 liên kết đôi nên tổng số liên kết = 1+ số nhóm (–COOH)
Suy ra:
Đáp án C
Câu 23: Hợp chất CH3CH2(CH3)CH2CH2CH(C2H5)COOH có tên thay thế là
A. axit 2 – etyl – 5 metylhexanoic.
B. axit 5 – etyl – 2 metylhexanoic.
C. axit 2 - etyl – 5 metylnonanoic.
D. Tên gọi khác.
Hướng dẫn giải:
Tên thay thế của hợp chất trên là axit 2 – etyl – 5 metyl hexanoic.
Đáp án A
Câu 24: Axit cacboxylic A có công thức đơn giản nhất là C3H4O3. A có công thức phân tử là
A. C3H4O3.
B. C18H24O18.
C. C6H8O6.
D. C12H16O12.
Hướng dẫn giải:
- Axit cacboxylic luôn có số oxi chẵn nên loại đáp án A.
- Gọi công thức A là (C3H4O3)n.
- Ta có số liên kết + vòng =
- Ta thấy đáp án C thỏa mãn vì tổng bằng 3 và bằng gốc COOH.
- Đáp án B loại do số liên kết + vòng = 7 # 9trong gốc COOH; đáp án D loại do tổng số + vòng = 5 # 6 trong gốc COOH
Đáp án C
Câu 25: Một axit no X có CTĐGN là C2H3O2. Công thức phân tử của axit X là
A. C6H9O6.
B. C2H3O2.
C. C4H6O4.
D. C8H12O8.
Hướng dẫn giải:
- Gọi công thức của X là (C2H3O2)n.
- Ta có số liên kết =
- Mặt khác do X là axit no nên tổng số = số nhóm COOH = = n
-Suy ra
Đáp án C
Câu 26: Phân tử C4H6O2 có bao nhiêu đồng phân cấu tạo mạch hở thuộc chức axit?
A. 2.
B. 3.
C. 4.
D. 5.
Hướng dẫn giải:
C4H6O2 có 3 đồng phân cấu tạo mạch hở thuộc chức axit:
CH2=CH-CH2-COOH
CH2=C(CH3)-COOH
CH3-CH=CH-COOH
Đáp án B
Câu 27: Công thức cấu tạo của axit ađipic là
A. HCOOH.
B. HOOC-CH2-COOH.
C. CH2=C(CH3)-COOH.
D. HOOC-(CH2)4-COOH.
Hướng dẫn giải:
Công thức cấu tạo của axit ađipic là HOOC-(CH2)4-COOH.
Đáp án D
Câu 28: Công thức cấu tạo của axit axetic là
A. O = CH – O – CH3
D. CH2 – O – O – CH2
Hướng dẫn giải:
Công thức cấu tạo của axit axetic là
Đáp án B
Câu 29: Axit không no, đơn chức có một liên kết đôi trong gốc hiđrocacbon có công thức phù hợp là
A. CnH2n-1-2kCOOH ( ).
B. RCOOH.
C. CnH2n-1COOH ( ).
D. CnH2n+1COOH ().
Hướng dẫn giải:
Axit không no, đơn chức có một liên kết đôi trong gốc hiđrocacbon có công thức phù hợp là CnH2n-1COOH ().
Đáp án C
Câu 30: Khi đốt cháy 1 mol X thu được dưới 6 mol CO2. CTCT của X là gì? Biết CTĐGN của axit hữu cơ X là CHO.
A. CH3COOH.
B. CH2=CHCOOH.
C. HOOCCH=CHCOOH.
D. HCOOH.
Hướng dẫn giải:
Gọi CTCT của X là (CHO)n
Theo đề bài số nguyên tử C < 6.
Do số O phải chẵn nên n = 2 hoặc n = 4.
Với n = 2 → C2H2O2 → loại
Suy ra n = 4 là phù hợp và X là HOOCCH=CHCOOH.
Đáp án C
Xem thêm các dạng câu hỏi và bài tập liên quan khác:
30 bài tập về Andehit (2024) có đáp án chi tiết nhất
30 bài tập về Sulfuric acid và muối sulfate (2024) có đáp án chi tiết nhất
30 bài tập về Ammonia. Muối ammonium (2024) có đáp án chi tiết nhất
30 Bài tập về Khái niệm về cân bằng hoá học (2024) có đáp án chi tiết nhất
30 Bài tập về Cân bằng trong dung dịch nước (2024) có đáp án chi tiết nhất