Bài tập về Phản ứng trao đổi ion trong dung dịch các chất điện li
Kiến thức cần nhớ
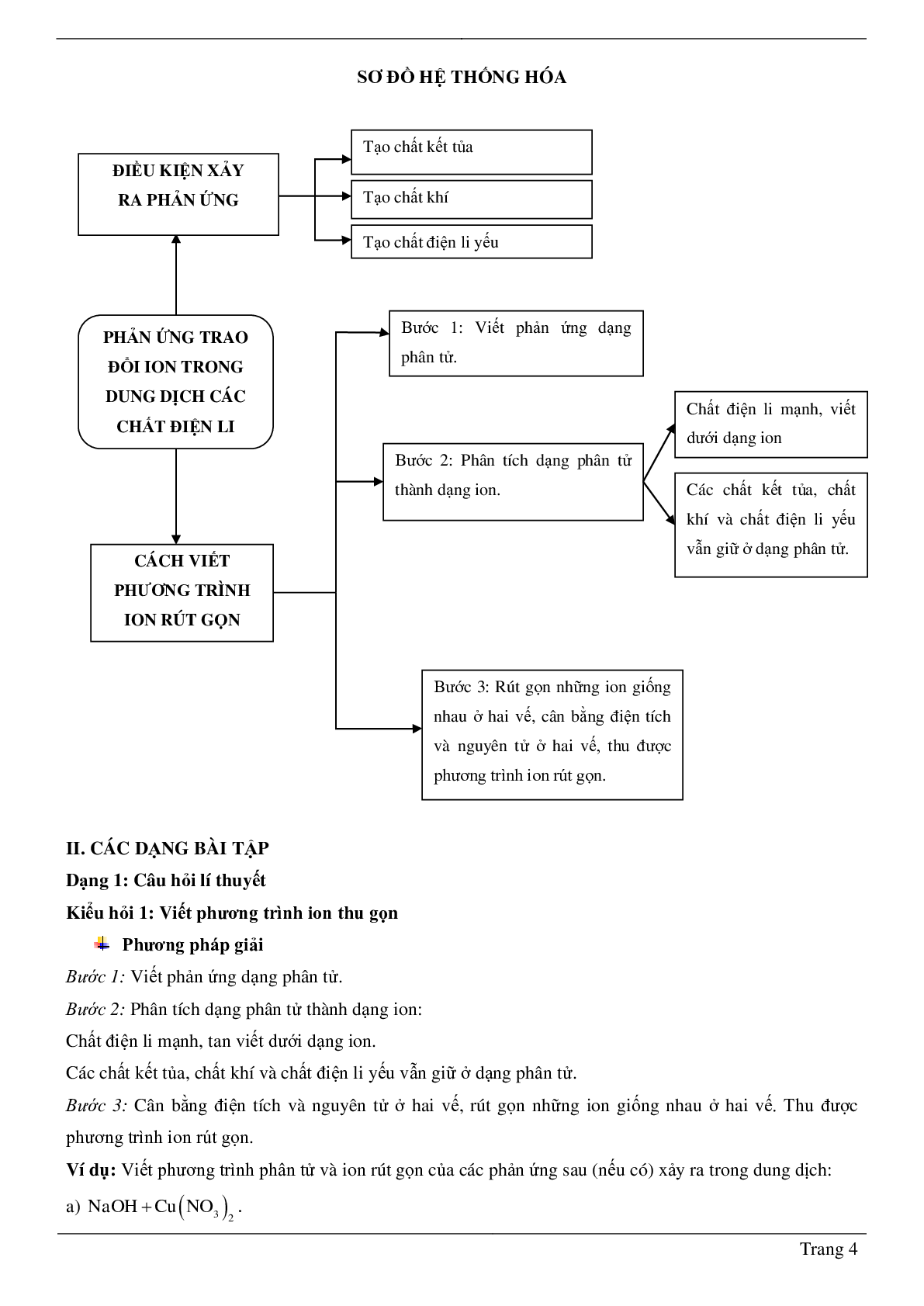
1. Điều kiện xảy ra phản ứng trao đổi ion trong dung dịch các chất điện li
Xét phản ứng:
Dung dịch A + dung dịch B → Sản phẩm.
- Phản ứng xảy ra trong dung dịch các chất điện li là phản ứng giữa các ion.
- Phản ứng trao đổi ion trong dung dịch các chất điện li chỉ xảy ra khi các ion kết hợp được với nhau tạo thành ít nhất 1 trong số các chất sau:
+ Chất kết tủa.
+ Chất điện li yếu.
+ Chất khí.
Thí dụ:
+ Phản ứng tạo thành chất kết tủa:
Na2SO4 + BaCl2 → 2NaCl + BaSO4↓

Kết tủa BaSO4
+ Phản ứng tạo thành chất điện li yếu:
HCl + NaOH → NaCl + H2O
+ Phản ứng tạo thành chất khí:
Fe + H2SO4 loãng → FeSO4 + H2↑
2. Phương trình ion rút gọn
- Phương trình ion rút gọn cho biết bản chất của phản ứng trong dung dịch các chất điện li.
- Cách chuyển từ phương trình dưới dạng phân tử thành phương trình ion rút gọn như sau:
Bước 1:
+ Chuyển các chất vừa dễ tan, vừa điện li mạnh thành ion.
+ Các chất khí, chất kết tủa, chất điện li yếu để nguyên ở dạng phân tử.
⇒ Khi này, phương trình thu được gọi là phương trình ion đầy đủ.
Thí dụ: Xét phản ứng:
Na2SO4 + BaCl2 → 2NaCl + BaSO4↓
Phương trình ion đầy đủ là:
2Na+ ++ Ba2+ + 2Cl- → BaSO4↓ + 2Na+ + 2Cl-
Bước 2: Lược bỏ những ion không tham gia phản ứng, ta được phương trình ion rút gọn.
Ba2+ +→ BaSO4↓
Từ phương trình này ta thấy rằng, muốn điều chế kết tủa BaSO4 chỉ cần trộn 2 dung dịch, một dung dịch chứa Ba2+, dung dịch kia chứa ion SO42-.
Các dạng bài tập về phản ứng trao đổi ion trong dung dịch các chất điện li
Dạng 1: Câu hỏi lí thuyết
Kiểu hỏi 1: Viết phương trình ion thu gọn
Phương pháp giải
Bước 1: Viết phản ứng dạng phân tử.
Bước 2: Phân tích dạng phân tử thành dạng ion:
Chất điện li mạnh, tan viết dưới dạng ion.
Các chất kết tủa, chất khí và chất điện li yếu vẫn giữ ở dạng phân tử.
Bước 3: Cân bằng điện tích và nguyên tử ở hai vế, rút gọn những ion giống nhau ở hai vế. Thu được phương trình ion rút gọn.
Kiểu hỏi 2: Từ phương trình ion rút gọn tìm phương trình hóa học dạng phân tử tương ứng
Phương pháp giải
Bước 1: Từ phương trình ion rút gọn nhận dạng xem đây là loại phương trình ion rút gọn thuộc dạng nào (sản phẩm có kết tủa, chất điện li yếu, khí).
Bước 2: Nhìn sản phẩm có chất kết tủa, chất điện li yếu, chất khí để tìm phương trình hóa học dạng phân tử.
Kiểu hỏi 3: Chất, ion không thể hoặc có thể chứa đồng thời hoặc không đồng thời trong cùng một dung dịch
Phương pháp giải
Chất hoặc ion có thể tồn tại trong cùng một dung dịch khi các chất hoặc ion đó kết hợp với nhau không tạo ra kết tủa hoặc bay hơi hoặc chất điện li yếu.
Chất hoặc ion không thể tồn tại trong cùng một dung dịch khi các chất hoặc ion đó kết hợp với nhau tạo ra kết tủa hoặc bay hơi hoặc chất điện li yếu.
Bước 1: Nhìn chất, hoặc ion nào kết hợp với nhau tạo ra kết tủa hoặc chất khí hoặc chất điện li yếu.
Bước 2: Từ bước 1 dùng phương pháp loại trừ tìm ra đáp án.
Dạng 2: Bài tập bảo toàn điện tích và phản ứng trao đổi ion trong dung dịch
Phương pháp giải
- Nội dung định luật bảo toàn điện tích: Trong một dung dịch, tổng giá trị điện tích âm bằng tổng giá trị điện tích dương
Tổng số mol ion dương . giá trị điện tích dương = Tổng số mol ion âm . giá trị điện tích âm.
Dạng 3: Sử dụng phương trình ion rút gọn để tính toán lượng chất trong dung dịch
Phương pháp giải
Để làm được loại bài tập này, các em chỉ cần viết phương trình ion rút gọn
=> Từ phương trình ion, áp dụng thêm định luật bảo toàn điện tích, bảo toàn nguyên tố, …..
=> lượng các ion theo yêu cầu của đề bài.
Bài tập tự luyện
Câu 1: Cho phản ứng NaOH + HCl → NaCl + H2O. Phản ứng hóa học nào sau đây có cùng phương trình ion thu gọn với phản ứng trên?
A. 2KOH + FeCl2 → Fe(OH)2 + 2KCl.
B. NaOH + NH4Cl → NaCl + NH3 + H2O.
C. KOH + HNO3 → KNO3 + H2O.
D. NaOH + NaHCO3 → Na2CO3 + H2O.
Hướng dẫn giải chi tiết:
Phương trình ion rút gọn của phản ứng NaOH + HCl → NaCl + H2O là:
OH- + H+ → H2O
A. 2OH- + Fe2+ → Fe(OH)2
B. OH- + NH4+ → NH3 + H2O
C. OH- + H+ → H2O
D. OH- + HCO3- → CO32- + H2O
Đáp án C.
Câu 2: Phản ứng trao đổi ion trong dung dịch các chất điện li chỉ xảy ra khi
A. các chất phản ứng phải là chất điện li mạnh.
B. một số ion trong dung dịch kết hợp được với nhau làm giảm nồng độ ion của chúng.
C. các chất phản ứng phải là những chất dễ tan.
D. phản ứng phải là thuận nghịch.
Hướng dẫn giải chi tiết:
Phản ứng trao đổi ion trong dung dịch các chất điện li chỉ xảy ra khi một số ion trong dung dịch kết hợp được với nhau làm giảm nồng độ ion của chúng.
Đáp án B.
Câu 3: Trong các cặp chất cho dưới đây, cặp chất nào có thể cùng tồn tại trong một dung dịch?
A. AlCl3 và CuSO4.
B. NH3 và AgNO3.
C. Na2ZnO2 và HCl.
D. NaHSO4 và NaHCO3.
Hướng dẫn giải chi tiết:
B. AgNO3 + H2O + 3NH3 → NH4NO3 + (Ag(NH3)2)OH
C. Na2ZnO2 + 2HCl → 2NaCl + Zn(OH)2
Nếu HCl dư : Zn(OH)2 + 2HCl → ZnCl2 + 2H2O
D. NaHCO3 + NaHSO4 → H2O + Na2SO4 + CO2
Đáp án A
Câu 4: Cặp chất nào sau đây không thể tồn tại trong một dung dịch?
A. NaClO và AlCl3.
B. NaOH và KCl.
C. KNO3 và HCl.
D. Ba(OH)2 và AlCl3.
Hướng dẫn giải chi tiết:
Ba(OH)2 và AlCl3 không thể cùng tồn tại trong một dung dịch vì chúng phản ứng với nhau:
3Ba(OH)2 + 2AlCl3 → 3BaCl2 + 2Al(OH)3↓
Đáp án D
Câu 5: Cho các phản ứng hoá học sau:
(1) (NH4)2SO4 + BaCl2
(2) CuSO4 + Ba(NO3)2
(3) Na2SO4 + BaCl2
(4) H2SO4 + BaSO3
(5) (NH4)2SO4 + Ba(OH)2
(6) Fe2(SO4)3 + Ba(NO3)2
Các phản ứng đều có cùng phương trình ion rút gọn là
A. (1), (2), (3), (6).
B. (1), (3), (5), (6).
C. (2), (3), (4), (6).
D. (3), (4), (5), (6).
Hướng dẫn giải chi tiết:
(1) SO42- + Ba2+ → BaSO4
(2) SO42- + Ba2+ → BaSO4
(3) SO42- + Ba2+ → BaSO4
(4) 2H+ + SO42- + BaSO3 → BaSO4 + SO2 + H2O
(5) 2NH4+ + SO42- + Ba2+ + OH- → BaSO4 + NH3 + H2O
(6) SO42- + Ba2+ → BaSO4
=> Các phản ứng có cùng phương trình ion rút gọn là: (1), (2), (3), (6).
Đáp án A
Câu 6: Một cốc nước có chứa a mol Ca2+, b mol Mg2+, c mol Cl-, d mol HCO3-. Hệ thức liên hệ giữa a, b, c, d là :
A. 2a+2b=c-d.
B. a+b=c+d.
C. 2a+2b=c+d.
D. a+b=2c+2d.
Hướng dẫn giải chi tiết:
Áp dụng định luật bảo toàn điện tích ta có:
Đáp án C.
Câu 7: Một dung dịch chứa 0,02 mol Cu2+, 0,03 mol K+, x mol Cl– và y mol SO42–. Tổng khối lượng các muối tan có trong dung dịch là 5,435 gam. Giá trị của x và y lần lượt là :
A. 0,01 và 0,03.
B. 0,02 và 0,05.
C. 0,05 và 0,01.
D. 0,03 và 0,02.
Hướng dẫn giải chi tiết:
Áp dụng định luật bảo toàn điện tích, tổng giá trị điện tích âm bằng tổng giá trị điện tích dương
=> 0,02 . 2 + 0,03 . 1 = x .1 + y . 2 (I)
Áp dụng định luật bảo toàn khối lượng ta có:
m Cu + m K + m Cl + m SO4 = 5,435
=> 0,02 . 64 + 0,03 . 39 ++ 35,5x + 96y = 5,435 (II)
Từ (I) và (II) => x = 0,03; y = 0,02
Đáp án D
Câu 8: Cho 22,4 gam hỗn hợp Na2CO3, K2CO3 tác dụng vừa đủ với dung dịch BaCl2. Sau phản ứng thu được 39,4 gam kết tủa. Lọc tách kết tủa, cô cạn dung dịch thì thu được bao nhiêu gam muối clorua khan?
Hướng dẫn giải chi tiết:
- Muối thu được chứa: Na+; K+; Cl−
Câu 9: Trộn 250 ml dung dịch chứa hỗn hợp HCl 0,08M và H2SO4 0,01M với 250 ml dung dịch NaOH aM thu được 500 ml dung dịch có pH = 12. Giá trị a là :
A. 0,13M.
B. 0,12M.
C. 0,14M.
D. 0.10M.
Hướng dẫn giải chi tiết:
Tổng số mol ion H+ trong dung dịch axit là :
Tổng số mol ion OH- trong dung dịch bazơ là :
Dung dịch sau phản ứng có pH = 12, suy ra có pOH = 2, suy ra dung dịch sau phản ứng còn bazơ dư, [OH- dư] = 10-2M = 0,01M.
Phương trình phản ứng :
(1)
mol: 0,025 → 0,025
Theo (1) và giả thiết ta thấy sau phản ứng số mol OH- dư là (0,25a – 0,025) mol.
Nồng độ OH- dư là :
Câu 10: Dung dịch X chứa các ion: Fe3+ ; SO42 ; NH4+; Cl−. Chia dung dịch thành 2 phần bằng nhau:
- Phần 1: Cho tác dụng với lượng dư dung dịch NaOH , đun nóng thu được 0,672 lít khí ở đktc và 1,07 gam kết tủa.
- Phần 2: Tác dụng với lượng dư dung dịch BaCl2 thu được 4,66 gam kết tủa.
Tổng khối lượng các muối khan thu được khi cô cạn dung dịch X là (quá trình cô cạn chỉ có nước bay hơi)
Hướng dẫn giải chi tiết:
- Phần 1: nNH3 = 0,03 mol; nFe(OH)3 = 0,01 mol => nFe3+ = 0,01 mol
NH4+ + OH- → NH3 + H2O
nNH4+ = nNH3 = 0,03 mol
Phần 2: nBaSO4 = 0,02 mol => nSO4 = 0,02 mol
- Bảo toàn điện tích:
=> 3.0,01 + 1.0,03 = 2.0,02 + nCl- => nCl- = 0,02 mol
- Bảo toàn khối lượng (trong 1 phần)
=> cô cạn dung dịch X thu được:
mmuối = 2.3,73 = 7,46 gam
Câu 11: Trộn dung dịch chứa Ba2+ ; OH− 0,06 mol và Na+ 0,02 mol với dung dịch HCO3− 0,04 mol; CO32− 0,03 mol và Na+. Khối lượng kết tủa thu được sau khi trộn là:
Hướng dẫn giải chi tiết:
-
=> => > nBa2+
Xem thêm các dạng câu hỏi và bài tập liên quan khác:
30 bài tập về Andehit (2024) có đáp án chi tiết nhất
30 bài tập về Sulfuric acid và muối sulfate (2024) có đáp án chi tiết nhất
30 bài tập về Ammonia. Muối ammonium (2024) có đáp án chi tiết nhất
30 Bài tập về Khái niệm về cân bằng hoá học (2024) có đáp án chi tiết nhất
30 Bài tập về Cân bằng trong dung dịch nước (2024) có đáp án chi tiết nhất