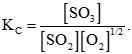Giải SBT Hoá học 11 Bài 7: Sulfur và sulfur dioxide
A. diêm sinh.
B. đá vôi.
C. phèn chua.
D. giấm ăn.
Lời giải:
Đáp án đúng là: A
Trong dân gian, sulfur có tên gọi là diêm sinh.
A.34S.
B. 32S.
C. 36S.
D. 33S.
Lời giải:
Đáp án đúng là: B
Trong tự nhiên, đồng vị của sulfur chiếm thành phần nhiều nhất là 32S (≈ 95%)
A. BaSO4.
B. CaSO4.2H2O.
C. MgSO4.
D. CaSO4.5H2O
Lời giải:
Đáp án đúng là: B
Thạch cao sống có công thức là CaSO4.2H2O.
A. 2.
B. 4.
C. 6.
D. 8.
Lời giải:
Đáp án đúng là: D
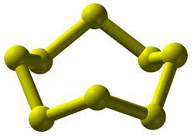
Phân tử sulfur trong trạng thái rắn tồn tại ở dạng vòng gồm có 8 nguyên tử sulfur.
A. lưu hoá cao su tự nhiên.
B. sản xuất sulfuric acid.
C. điều chế thuốc bảo vệ thực vật.
D. bào chế thuốc đông y.
Lời giải:
Đáp án đúng là: B
Trong công nghiệp, phần lớn sulfur đơn chất sau khi khai thác ở các mỏ được dùng làm nguyên liệu để sản xuất sulfuric acid.
A. sulfur trioxide.
B. sulfuric acid.
C. sulfur dioxide.
D. hydrogen sulfide.
Lời giải:
Đáp án đúng là: C
Tên gọi của SO2 là sulfur dioxide.
A. SO2.
B. H2S.
C. CO2.
D. CO.
Lời giải:
Đáp án đúng là: A
Tác nhân chính tạo ra mưa acid là SO2
A. O2.
B. CO2.
C. SO2.
D. N2
Lời giải:
Đáp án đúng là: C
Trong các khí trên, khí tan tốt trong nước ở điều kiện thường là SO2 (9,4 g/ 100 mL nước ở 25oC).
A. Fe.
B. O2.
C. H2.
D. Hg.
Lời giải:
Đáp án đúng là: B
Phương trình phản ứng
S đóng vai trò là chất khử, O2 là chất oxi hóa.
A. NO2.
B. H2S.
C. NaOH.
D. Ca(OH)2.
Lời giải:
Phương trình phản ứng:
SO2 là chất oxi hóa, H2S là chất khử.
A. Than đá.
B. Đá vôi.
C. Muối ăn.
D. Sulfur.
Lời giải:
Đáp án đúng là: D
Phương trình phản ứng :
HgS là chất kết tủa màu vàng, bền và ít độc hại hơn hơi thủy ngân.
A. 2.
B. 4.
C. 1.
D. 3.
Lời giải:
Đáp án đúng là: D
Các khoáng vật có thành phần chính chứa muối sulfide là blend, chalcopyrite, pyrite.
Bài 7.13 trang 27 Sách bài tập Hóa học 11: Cho các phản ứng:
Số phản ứng trong đó sulfur đơn chất đóng vai trò chất khử là
A. 1.
B. 2.
C. 3.
D. 4
Lời giải:
Đáp án đúng là: B
Các phản ứng trong đó sulfur đơn chất đóng vai trò chất khử là
(a)
(b)
Thể tích khí SO2 (đkc) đã phản ứng là
A. 50 mL.
B. 248 mL.
C. 124 mL.
D. 100 mL.
Lời giải:
Đáp án đúng là: C
Phương trình phản ứng:
A. Giấm ăn.
B. Muối ăn.
C. Nước vôi.
D. Nước máy.
Lời giải:
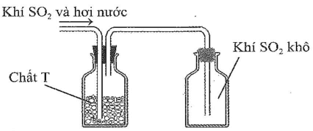
Đáp án đúng là: C
Nước vôi phản ứng với SO2 tạo thành hợp chất rắn CaSO3, ngăn SO2 bay ra ngoài môi trường.
SO2 + Ca(OH)2 → CaSO3↓ + H2O
A. KOH.
B. NaOH.
C. CaO.
D. P2O5.
Lời giải:
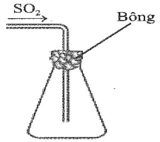
Đáp án đúng là: D
P2O5 giữ lại hơi nước, do đó có tác dụng làm khô khí SO2
P2O5 + 3H2O →2H3PO4
Bài 7.17 trang 28 Sách bài tập Hóa học 11: Xét phản ứng giữa sulfur và hydrogen ở điều kiện chuẩn:
A. -20,6 kJ/mol.
B. -41,2 kJ/mol.
C. 41,2 kJ/mol.
D. 20,6 kJ/mol.
Lời giải:
Đáp án đúng là: A
Nhiệt tạo thành của H2S(g) = biến thiên enthalpy của phản ứng = -20,6 kJ/mol
Bài 7.18 trang 28 Sách bài tập Hóa học 11: Cho các ứng dụng sau:
(3) diệt nấm mốc, thuốc đông y;
(4) diệt trùng nước sinh hoạt.
Số ứng dụng của khí sulfur dioxide trong đời sống, sản xuất là
A. 1.
B. 2.
C. 3.
D. 4.
Lời giải:
Đáp án đúng là: C
Các ứng dụng của khí sulfur dioxide trong đời sống, sản xuất là
(1) sản xuất sulfuric acid;
(2) tẩy trắng bột giấy;
(3) diệt nấm mốc, thuốc đông y;
A. 173,5.
B. 347,0.
C. 86,8.
D. 477,2.
Lời giải:
Đáp án đúng là: B
Phương trình phản ứng:
Khối lượng sulfur tối đa tạo ra khi chuyển hoá 1000 m3 khí thiên nhiên (đkc) (chứa 5 mg H2S/m3) là
A. 10,0 g.
B. 5,0 g.
C. 7,06 g.
D. 100,0 g.
Lời giải:
Đáp án đúng là: C
Phương trình phản ứng:
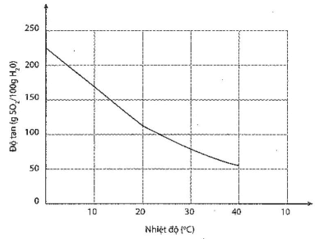
Sự phụ thuộc của độ tan khí sulfur dioxide vào nhiệt độ.
a) Độ tan của sulfur dioxide ở 20oC. Nhận xét về tính tan của sulfur dioxide ở nhiệt độ này.
b) Nồng độ phần trăm của dung dịch sulfur dioxide bão hoà ở 20oC.
c) Nhiệt độ tại đó độ tan của khí sulfur dioxide là 10 g trong 100 g nước.
Lời giải:
a) Ở 20oC, độ tan của sulfur dioxide khoảng 112 g SO2/1 kg nước.
Nhận xét: ở nhiệt độ này, sulfur dioxide tan tốt trong nước.
b) Nồng độ phần trăm của sulfur dioxide bão hòa:
c) Ở 23oC, độ tan của khí sulfur dioxide là 10 g trong 100 gam nước.
a) Viết biểu thức tính hằng số cân bằng KC của phản ứng.
b) Hãy cho biết phản ứng trên là toả nhiệt hay thu nhiệt.
Lời giải:
a)
b) < 0 nên phản ứng trên là phản ứng tỏa nhiệt.
c) Ở 25oC, tốc độ phản ứng rất nhỏ, hiệu suất không đáng kể; ở 600oC, cân bằng chuyển dịch mạnh theo chiều nghịch, làm giảm hiệu suất.
Lời giải:
= 91,3.1-395,7.1-33,2.1-(-296,8.1) = -40,8 (kJ) < 0
Vậy phản ứng trên là phản ứng tỏa nhiệt.
Lời giải:
Áp dụng định luật bảo toàn khối lượng, ta có:
my = mx = 64.1 + 32.1 = 96 (g)
x →0,5x →x
Hỗn hợp khí Y gồm :SO2 1-x (mol), O2 1-0,5x (mol), SO3 x(mol)
x = 0,8 mol
Trong một ngày, một làng nghề đốt cháy 20 kg sulfur để tạo thành sulfur dioxide.
a) Viết phương trình hoá học và tính thể tích khí SO2 (đkc) tối đa tạo ra?
- Viết các phương trình hoá học theo sơ đồ trên.
- Tính thể tích nước mưa bị nhiễm acid nếu nồng độ H2SO4 trong nước mura là 1,25.10-5 M.
Lời giải:
a) S + O2 → SO2
Mol: 625 625
Thể tích khí SO2 (đkc) tối đa tạo ra là:
V = 24,79.625 = 15 493,75 (lit)
b) 2SO2 + O2 → 2SO3
Mol: 125 125
SO3 + H2O → H2SO4
Mol: 125 125
Vậy thể tích nước mưa bị nhiễm acid là:
Xem thêm lời giải bài tập SBT Hoá học lớp 11 Kết nối tri thức hay, chi tiết khác:
Bài 6: Một số hợp chất của nitrogen với oxygen