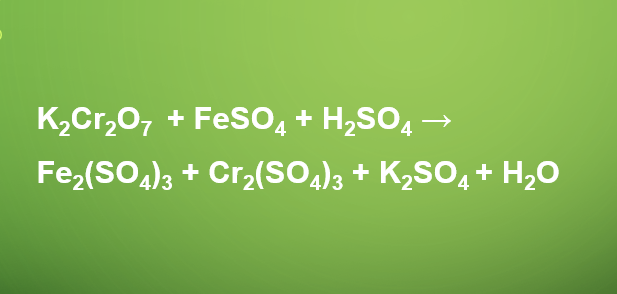K2Cr2O7 + FeSO4 + H2SO4 → Fe2(SO4)3 + Cr2(SO4)3 + K2SO4 + H2O
1. Phương trình phản ứng hóa học
K2Cr2O7 + 6FeSO4 + 7H2SO4 → 3Fe2(SO4)3 + Cr2(SO4)3 + K2SO4 + 7H2O
2. Hiện tượng nhận biết phản ứng
Dung dịch chuyển từ màu cam sang màu xanh lục.
3. Điều kiện phản ứng
Không có
4. Mở rộng tính chất hoá học của các chất tham gia
4.1. Tính chất hoá học của H2SO4
a. Axit sunfuric loãng
- Axit sunfuric là một axit mạnh, hóa chất này có đầy đủ các tính chất hóa học chung của axit như:
- Axit sunfuric H2SO4 làm chuyển màu quỳ tím thành đỏ.
- Tác dụng với kim loại đứng trước H (trừ Pb)
Fe + H2SO4 → FeSO4 + H2
- Tác dụng với oxit bazo
FeO + H2SO4 → FeSO4 + H2O
- Tác dụng với bazo
H2SO4 + NaOH → NaHSO4 + H2O
H2SO4 + 2NaOH → Na2SO4 + 2H2O
- Tác dụng với muối
Na2CO3 + H2SO4 → Na2SO4 + H2O + CO2
H2SO4 + 2KHCO3 → K2SO4 + 2H2O + 2CO2
b. Axit sunfuric đặc
- Axit sunfuric đặc có tính axit mạnh, oxi hóa mạnh với tính chất hóa học nổi bật như:
- Tác dụng với kim loại:
Cu + 2H2SO4 → CuSO4 + SO2 + 2H2O
- Tác dụng với phi kim
C + 2H2SO4 → CO2 + 2H2O + 2SO2 (nhiệt độ)
2P + 5H2SO4 → 2H3PO4 + 5SO2 + 2H2O
- Tác dụng với các chất khử khác.
2FeO + 4H2SO4 → Fe2(SO4)3 + SO2 + 4H2O
- H2SO4 còn có tính háo nước đặc trưng
C12H22O11 + H2SO4 → 12C + H2SO4.11H2O
4.2. Tính chất hoá học của muối cromat CrO42- và dicromat Cr2O72-
- Trong dung dịch có cân bằng:
2CrO42- + 2H+ ⇆ Cr2O72- + H2O
- Khi thêm H+ vào muối cromat thì sẽ chuyển từ màu vàng sang màu da cam
K2CrO4 + H2SO4 → K2CrO7 + K2SO4 + H2O
- Khi thêm OH- vào muối đicromat thì sẽ chuyển từ da cam sang vàng
K2CrO7 + KOH → K2CrO4 + H2O
- Tính chất của muối cromat và đicromat là tính oxi hoá mạnh, đặc biệt trong môi trường axit.
Cho FeSO4 và axit sunfuric vào dung dịch kali dicromat.
K2Cr2O7 + 6FeSO4 + 7H2SO4 → Cr2(SO4)3 + 3Fe2(SO4)3 + K2SO4 + 7H2O
Các phản ứng hóa học khác
K2Cr2O7 + 14HCl → 2KCl + 2CrCl3 + 3Cl2 + 7H2O
K2Cr2O7 + 6KI + 7H2SO4 → Cr2(SO4)3 + 4K2SO4 + 3I2 + 7H2O
4.3. Tính chất hoá học của FeSO4
- Mang đầy đủ tính chất hóa học của muối.
- Có tính khử và tính oxi hóa:
Tính khử: Fe2+ → Fe3+ + 1e
Tính oxi hóa: Fe2+ + 1e → Fe
- Tính chất hóa học của muối:
- Tác dụng với dung dịch kiềm:
FeSO4 + KOH → K2SO4 + Fe(OH)2
- Tác dụng với muối:
FeSO4 + BaCl2 → BaSO4 + FeCl2.
- Tính khử:
FeSO4 + Cl2 → FeCl3 +Fe2(SO4)3
2FeSO4 + 2H2SO4 đặc nóng → Fe2(SO4)3 + SO2 + 2H2O
10FeSO4 + 2KMnO4 + 8H2SO4 → 5Fe2(SO4)3 + K2SO4 + 2MnSO4 + 8H2O
- Tính oxi hóa:
FeSO4 + Mg → MgSO4 + Fe
5. Cách thực hiện phản ứng
Nhỏ vào ống nghiệm vài giọt dung dịch K2Cr2O7. Nhỏ tiếp vài giọt dung dịch H2SO4 loãng lắc nhẹ sau đó cho thêm vài giọt dung dịch FeSO4, lắc nhẹ.
6. Bạn có biết
K2Cr2O7 là chất oxi hóa mạnh trong môi trường axit muối Cr(VI) bị khử thành muối Cr(III).
7. Bài tập liên quan (có đáp án)
Câu 1: Khối lượng K2Cr2O7 cần lấy để tác dụng đủ với 0,6 mol FeSO4 trong dung dịch (có H2SO4 làm môi trường) là
A. 26,4 g.
B. 27,4 g.
C. 28,4 g.
D. 29,4 g.
Lời giải:
Đáp án: A
K2Cr2O7 + 6FeSO4 + 7H2SO4 → 3Fe2(SO4)3 + Cr2(SO4)3 + K2SO4 + 7H2O
0,1 ← 0,6 (mol)
→ mK2Cr2O7 = 0,1.294 = 29,4 (g)
Câu 2: Cho sơ đồ phản ứng:
FeSO4 + K2Cr2O7+ H2SO4 → Fe2(SO4)3 + Cr2(SO4)3 + K2SO4 + H2O
Hệ số cân bằng của FeSO4 là
A. 10
B. 6
C. 8
D. 4
Lời giải:
Đáp án: B
Câu 3: Cho phản ứng sau:
FeSO4 + K2Cr2O7 + H2SO4 → Fe2(SO4)3 + Cr2(SO4)3 + K2SO4 + H2O
Tổng hệ số cân bằng của các chất tham gia phản ứng là
A. 12
B. 14
C. 18
D. 26
Lời giải:
Đáp án: B
Quá trình oxi hóa: +2Fe→+3Fe+1e
Quá trình khử: +6Cr+3e→+3Cr
Phương trình phản ứng:
6FeSO4 + K2Cr2O7 + 7H2SO4 → 3Fe2(SO4)3 + Cr2(SO4)3 + K2SO4 + 7H2O
Tổng hệ số cân bằng của các chất tham gia phản ứng: 6 + 1 + 7 = 14
Câu 4: Nhỏ vào ống nghiệm vài giọt dung dịch K2Cr2O7. Nhỏ tiếp vài giọt dung dịch H2SO4 loãng lắc nhẹ sau đó cho thêm vài giọt dung dịch FeSO4, lắc ống nghiệm ta thấy:
A. Dung dịch chuyển từ không màu sang màu da cam
B. Dung dịch chuyển từ màu da cam sang màu vàng nhạt
C. Dung dịch chuyển từ không màu sang màu vàng nhạt
D. Dung dịch chuyển từ màu da cam sang màu xanh
Lời giải:
Đáp án: D
Hiện tượng: Dung dịch chuyển từ màu cam sang màu xanh.
Phương trình hóa học:
6FeSO4 + K2Cr2O7 + 7H2SO4 → 3Fe2(SO4)3 + Cr2(SO4)3 + K2SO4 + 7H2O
Câu 5: Phát biểu nào sau đây là sai?
A. Dung dịch K2Cr2O7 có màu da cam
B. CrO3 là oxit axit
C. Trong hợp chất, crom có số oxi hóa đặc trưng là +2, +3, +6
D. Cr2O3 tan được trong dung dịch NaOH loãng
Lời giải:
Đáp án: D
Cr2O3 là oxit lưỡng tính nhưng tan trong axit và kiềm đặc, không tan trong NaOH loãng.
Xem thêm các phương trình hóa học hay khác:
FeSO4 + KMnO4 + H2SO4 → Fe2(SO4)3 + MnSO4 + K2SO4 + H2O l FeSO4 ra Fe2(SO4)3
FeS + H2SO4 → FeSO4 + H2S | FeS ra FeSO4
Fe3O4 + H2SO4 → FeSO4 + Fe2(SO4)3 + H2O | Fe3O4 ra Fe2(SO4)3