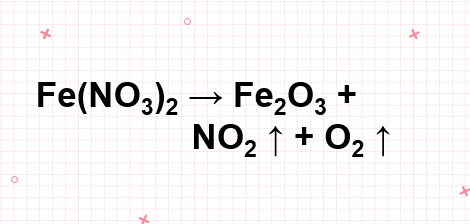4Fe(NO3)2 → 2Fe2O3 + 8NO2 ↑ + O2 ↑
1. Phương trình hoá học của phản ứng nhiệt phân Fe(NO3)2
4Fe(NO3)2 2Fe2O3 + 8NO2 + O2
2. Điều kiện để nhiệt phân Fe(NO3)2
- Nhiệt độ cao.
3. Cách lập phương trình hoá học của phản ứng nhiệt phân Fe(NO3)2
Bước 1: Xác định các nguyên tử có sự thay đổi số oxi hoá, từ đó xác định chất oxi hoá – chất khử:
Đây là phản ứng oxi hoá – khử nội phân tử; Fe(NO3)2 vừa là chất khử, vừa là chất oxi hoá.
Bước 2: Biểu diễn quá trình oxi hoá, quá trình khử
- Quá trình oxi hoá:
Cộng hai vế với nhau ta được:
- Quá trình khử:
Bước 3: Tìm hệ số thích hợp cho chất khử và chất oxi hoá
Bước 4: Điền hệ số của các chất có mặt trong phương trình hoá học. Kiểm tra sự cân bằng số nguyên tử của các nguyên tố ở hai vế.
4Fe(NO3)2 2Fe2O3 + 8NO2 + O2
4. Mở rộng về bài toán nhiệt phân muối nitrat
Các muối nitrat dễ bị phân hủy khi đun nóng:
+ Muối nitrat của các kim loại hoạt động (trước Mg):
Muối nitrat muối nitrit + O2
Ví dụ:
+ Muối nitrat của các kim loại từ Mg đến Cu:
Muối nitrat oxit kim loại + NO2 + O2
Ví dụ:
+ Muối của những kim loại kém hoạt động (sau Cu):
Muối nitrat kim loại + NO2 + O2
Ví dụ:
- Để giải dạng bài tập này ta thường sử dụng phương pháp tăng giảm khối lượng.
- Một số phản ứng đặc biệt:
NH4NO3 N2O + 2H2O
4Fe(NO3)2 2Fe2O3 + 8NO2 + O2.
5. Bài tập vận dụng liên quan
Câu 1. Nhiệt phân hoàn toàn Fe(NO3)2 trong không khí thu được sản phẩm gồm
A. FeO, NO2, O2.
B. Fe2O3, NO2.
C. Fe2O3, NO2, O2.
D. Fe, NO2, O2.
Hướng dẫn giải
Đáp án C
Vì Fe là kim loại trung bình nên sản phẩm thu được gồm oxit kim loại + NO2 + O2
4Fe(NO3)2 → 2Fe2O3 + 8NO2 + O2
Câu 2: Nhiệt phân hoàn toàn m gam Fe(NO3)2 trong bình kín không có không khí thu được V lít khí (đktc) và 8 gam Fe2O3. Giá trị của V, m là
A. 5,04 lít, 36 gam
B. 10,08 lít, 3,6 gam
C. 5,04 lít, 18 gam
D. 10,8 lít, 3,6 gam
Hướng dẫn giải
Đáp án C
Phương trình nhiệt phân Fe(NO3)2
2Fe(NO3)2 → Fe2O3 + 4NO2 + 1/2O2
0,1 ← 0,05 → 0,2 → 0,025
=> nkhí = =0,2 + 0,025 = 0,225 mol
=> Vkhí = 0,225.22,4 = 5,04 lít
mmuối = 180.0,1 = 18 gam
Câu 3. Nhiệt phân hoàn toàn KNO3 thu được sản phẩm
A. K, NO2, O2.
B. KNO2, O2, NO2.
C. KNO2, O2.
D. K2O, N2O.
Hướng dẫn giải
Đáp án C
2KNO3 2KNO2 + O2
Câu 4. Nhiệt phân hoàn toàn Cu(NO3)2 thu được các sản phẩm là
A. CuO, O2.
B. CuO, NO2, O2.
C. Cu, NO2, O2.
D. Cu2O, O2.
Hướng dẫn giải
Đáp án B
Phương trình nhiệt phân
2Cu(NO3)2 2CuO+ 4NO2 + O2.
Câu 5:Nhiệt phân hoàn toàn Fe(NO3)3 trong không khí thu được sản phẩm gồm
A. FeO, NO2, O2.
B. Fe2O3, NO2.
C. Fe, NO2, O2.
D. Fe2O3, NO2 , O2.
Hướng dẫn giải:
Đáp án D
4Fe(NO3)3 2Fe2O3 + 12NO2↑ + 3O2↑
Câu 6:Có các mệnh đề sau :
(1) Các muối nitrat đều tan trong nước và đều là chất điện li mạnh.
(2) Ion có tính oxi hóa trong môi trường axit.
(3) Khi nhiệt phân muối nitrat rắn ta đều thu được khí NO2.
(4) Hầu hết muối nitrat đều bền nhiệt.
Trong các mệnh đề trên, những mệnh đề đúng là
A. (1) và (3).
B. (2) và (4).
C. (2) và (3).
D. (1) và (2).
Hướng dẫn giải:
Đáp án D
(1), (2) đúng.
(3) sai vì các muối nitrat của kim loại mạnh (kali, natri,…) khi bị nhiệt phân sinh ra muối nitrit và O2.
(4) sai vì các muối nitrat dễ bị nhiệt phân hủy.
Câu 7: Khi nhiệt phân, dãy muối nitrat nào đều cho sản phẩm là oxit kim loại, khí nitơ đioxit và khí oxi
A. Cu(NO3)2, Fe(NO3)2, Mg(NO3)2
B. Cu(NO3)2, NaNO3, Pb(NO3)2
C. Hg(NO3)2, AgNO3
D. Zn(NO3)2, AgNO3, Pb(NO3)2
Hướng dẫn giải
Đáp án A
Nhiệt phân các muối của các kim loại từ Mg đến Cu trong dãy hoạt động hóa học thu được oxit kim loại, khí NO2 và O2
Phương trình hóa học phản ứng minh họa:
2Cu(NO3)2 2CuO + 4NO2 + O2↑
4Fe(NO3)2 2Fe2O3 + 8NO2 + O2.
2Mg(NO3)2 2MgO + 4NO2 + O2↑
Câu 8: Để điều chế Fe(NO3)2 ta có thể dùng phản ứng nào sau đây?
A. Fe + dung dịch AgNO3 dư
B. Fe + dung dịch Cu(NO3)2
C. FeO + dung dịch HNO3
D. FeS + dung dịch HNO3
Hướng dẫn giải
Đáp án B
Fe + Cu(NO3)2 → Fe(NO3)2 + Cu
Câu 9: Cho 8,4g sắt vào 300 ml dung dịch AgNO3 1,3M. Lắc kĩ cho phản ứng xảy ra hoàn toàn thu được m gam chất rắn. Giá trị của m là
A. 16,2. B. 42,12.
C. 32,4. D. 48,6.
Hướng dẫn giải
Đáp án B
nFe = 0,15 mol; = 0,39 mol
→ m = mAg = 0,39.108 = 42,12 gam
Câu 10:Khi nhiệt phân hoàn toàn hỗn hợp NH4NO3, Cu(NO3)2, AgNO3, Fe(NO3)2 thì chất rắn thu được sau phản ứng gồm:
A. CuO, FeO, Ag
B. CuO, Fe2O3, Ag
C. CuO, Fe2O3, Ag2O
D. NH4NO2, CuO, Fe2O3, Ag
Hướng dẫn giải:
Đáp án B
A sai vì có Fe2O3
C sai vì không thể tạo ra Ag2O
D sai vì không tạo ra NH4NO2
Câu 11. Dãy chất nào sau đây bị nhiệt phân hủy ở nhiệt độ cao
A. CaCO3, Zn(OH)2, KNO3, KMnO4
B. BaSO3, BaCl2, KOH, Na2SO4
C. AgNO3, Na2CO3, KCl, BaSO4
D. Fe(OH)3, Na2SO4, BaSO4, KCl
Hướng dẫn giải
Đáp án A
Phương trình phản ứng minh họa
CaCO3 CaO + CO2
Zn(OH)2 ZnO + H2O
2KNO3 2KNO2 + O2
2KMnO4 K2MnO4 + MnO2 + O2
Câu 12. Trong các nhận xét dưới đây về muối nitrat của kim loại, nhận xét nào không đúng?
A. Tất cả các muối nitrat đều dễ tan trong nước
B. Các muối nitrat đều dễ bị phân huỷ bởi nhiệt
C. Các muối nitrat chỉ được sử dụng làm phân bón hoá học trong nông nghiệp
D. Các muối nitrat đều là chất điện li mạnh, khi tan trong nước phân li ra cation kim loại và anion nitrat
Hướng dẫn giải
Đáp án C
Muối nitrat được dùng như một chất nguyên liệu; trong phân bón, nghề làm pháo hoa, nguyên liệu của bom khói, chất bảo quản, và như một tên lửa đẩy, cũng như thuỷ tinh và men gốm.
Xem thêm các phương trình hóa học khác:
Fe(NO3)2 + HNO3 → Fe(NO3)3 + NO2 + H2O l Fe(NO3)2 ra Fe(NO3)3
FeCl2 + AgNO3 → Fe(NO3)2 + AgCl |FeCl2 ra AgCl
Fe3O4 + HNO3 → Fe(NO3)3 + NO + H2O | Fe3O4 ra Fe(NO3)3