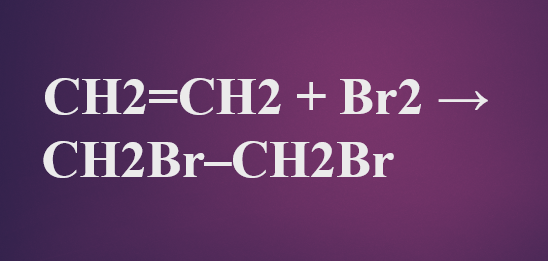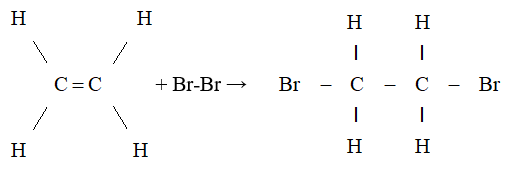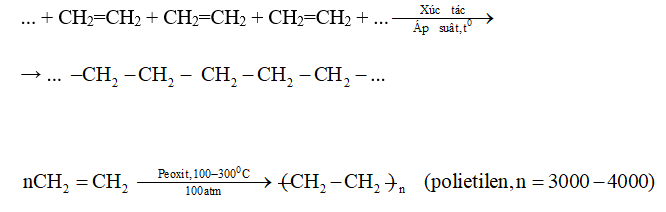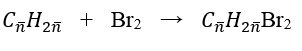Phản ứng:
CH2=CH2 + Br2 → CH2Br–CH2Br
1. Cách thực hiện phản ứng
- Dẫn khí etilen từ từ qua dung dịch brom thấy màu nâu đỏ của dung dịch nhạt dần.
2. Điều kiện phản ứng
- Phản ứng xảy ra ở điều kiện thường,
3. Hiện tượng nhận biết phản ứng
- Màu nâu đỏ của dung dịch nhạt dần.
4. Mở rộng kiến thức về tính chất hóa học của CH2=CH2 (etilen)
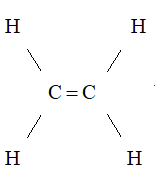
- Trong phân tử etilen, mỗi nguyên tử cacbon liên kết với hai nguyên tử hiđro, hai hóa trị còn lại dùng để liên kết hai nguyên tử cacbon với nhau.
- Công thức cấu tạo của etilen:
Viết gọn: CH2=CH2.
- Giữa hai nguyên tử cacbon có hai liên kết. Những liên kết như vậy được gọi là liên kết đôi.Trong liên kết đôi có một liên kết kém bền. Liên kết này dễ bị đứt ra trong các phản ứng hóa học.
4.1. Phản ứng cộng
- Phản ứng cộng halogen (phản ứng halogen hóa)
- Cộng brom
- Dẫn khí etilen qua dung dịch brom màu da cam
- Hiện tượng: Dung dịch brom bị mất màu.
- Nhận xét: Etilen đã phản ứng với brom trong dung dịch.
- Liên kết kém bền trong liên kết đôi bị đứt ra và mỗi phân tử etilen đã kết hợp thêm một phân tử brom. Phản ứng trên được gọi là phản ứng cộng.
- Ngoài brom, trong những điều kiện thích hợp, etilen còn có phản ứng cộng với một số chất khác. Ví dụ hiđro, clo.
- Nhìn chung, các chất có liên kết đôi (tương tự như etilen) dễ tham gia phản ứng cộng.
- Cộng clo
- Phản ứng cộng hiđro (phản ứng hiđro hóa)
- Phản ứng cộng axit
- Hiđro halogenua (HCl, HBr, HI), axit sunfuric đậm đặc ,... có thể cộng vào etilen.
CH2=CH2 + HCl (khí ) → CH3CH2Cl : (etyl clorua)
CH2=CH2 + H-OSO3H → CH3CH2OSO3H : (etyl hiđrosunfat )
- Phản ứng cộng nước (phản ứng hiđrat hóa)
- Ở nhiệt độ thích hợp và có xúc tác axit, etilen có thể cộng nước.
4.2. Phản ứng trùng hợp
- Ở điều kiện thích hợp (nhiệt độ, áp suất, xúc tác), liên kết kém bền trong phân tử etilen bị đứt ra. Khi đó, các phân tử etilen kết hợp với nhau tạo thành phân tử có kích thước và khối lượng rất lớn, gọi là polietilen (viết tắt là PE).
- Phản ứng trên được gọi là phản ứng trùng hợp.
- Polietilen là chất rắn, không tan trong nước, không độc. Nó là nguyên liệu quan trọng trong công nghiệp chất dẻo.
4.3. Phản ứng oxi hóa
- Etilen cháy hoàn toàn tạo ra CO2, H2O và tỏa nhiều nhiệt:
C2H4 + 3O2 → 2CO2 + 2H2O
- Etilen làm mất màu dung dịch KMnO4:
2 CH2=CH2 + 2KMnO4 + 4H22O → + 2MnO2 + 2KOH (etylen glicol)
- Phản ứng làm mất màu dung dịch thuốc tím kali pemanganat được dùng để nhận ra sự có mặt của liên kết đôi của anken.
5. Bạn có biết
- Phản ứng trên gọi là phản ứng cộng.
- Các đồng đẳng của etilen đều làm mất màu dung dịch brom.
- Phản ứng trên dùng để phân biệt anken với ankan.
6. Bài tập vận dụng
Câu 1: Dãy đồng đẳng nào sau đây tham gia phản ứng cộng với theo tỉ lệ 1:1?
A. Ankin.
B. Anken.
C. Ankan.
D. Ankađien.
Hướng dẫn
Trong phân tử anken chứa một liên kết pi, có thể tham gia phản ứng cộng với brom theo tỉ lệ 1:1.
Đáp án B.
Câu 2: Để phân biệt etan và etilen có thể dùng
A. dung dịch Br2.
B. dung dịch AgNO3.
C. quỳ tím.
D. dung dịch NaOH.
Hướng dẫn
Để phân biệt etan và etilen có thể dùng dd Br2 (màu vàng nâu), do etilen có thể phản ứng cộng với dd Br2 (tạo sản phẩm không màu) còn etan thì không.
Đáp án A.
Câu 3: Cho 0,448 lít hỗn hợp khí gồm metan và etilen đi qua dung dịch brom dư, thấy dung dịch nhạt màu và còn 0,112 lít khí thoát ra. Biết các thể tích khí đo ở đktc, thành phần % thể tích khí metan có trong hỗn hợp là
A. 25%.
B. 50%.
C. 60%.
D. 37,5%.
Hướng dẫn
Do dd brom dư, nên khí thoát ra là metan.
Đáp án A.
Câu 4: 2,8 gam anken X làm mất màu vừa đủ dung dịch chứa 8 gam Br2. Hiđrat hóa X chỉ thu được một ancol duy nhất. X có tên là
A. etilen.
B. but-2-en.
C. hex-2-en.
D. 2,3-đimetylbut-2-en.
Hướng dẫn
nBr2
Vì hiđrat hóa A chỉ thu được 1 ancol duy nhất A là CH3-CH=CH-CH3 (but-2-en)
Đáp án B
Câu 5: Dẫn 3,36 lít hỗn hợp X gồm 2 anken là đồng đẳng kế tiếp vào bình nước brom dư, thấy khối lượng bình tăng thêm 7,7 gam. Tìm CTPT của 2 anken?
A. C3H6 và C4H8
B. C4H8 và C5H10
C. C5H10 và C6H12
D. C3H6 và C5H10
Hướng dẫn
CnH2n + Br2 → CnH2nBr2
Khối lượng bình brom tăng bằng khối lượng của 2 anken:
CTPT của 2 anken kế tiếp là: C3H6 và C4H8
Đáp án A
Câu 6: Cho 3,36 lít hỗn hợp etan và etilen (đktc) đi chậm qua qua dung dịch brom dư. Sau phản ứng khối lượng bình brom tăng thêm 2,8 gam. Số mol etan và etilen trong hỗn hợp lần lượt là
A. 0,05 và 0,1
B. 0,1 và 0,05
C. 0,12 và 0,03
D. 0,03 và 0,12
Hướng dẫn
Khối lượng bình brom tăng = khối lượng etilen
Đáp án A
Câu 7: Dẫn 3,36 lít (đktc) hỗn hợp X gồm 2 anken là đồng đẳng kế tiếp vào bình nước brom dư, thấy khối lượng bình tăng thêm 7,7 gam. Thành phần phần % về thể tích của hai anken là
A. 25% và 75%
B. 33,33% và 66,67%
C. 40% và 60%
D. 35% và 65%
Hướng dẫn
CnH2n + Br2 → CnH2nBr2
Khối lượng bình brom tăng bằng khối lượng của 2 anken:
CTPT của 2 anken kế tiếp là: C3H6 và C4H8
Đáp án B
Câu 8: Cho hiđrocacbon X phản ứng với brom (trong dung dịch) theo tỉ lệ mol 1 : 1, thu được chất hữu cơ Y (chứa 74,08% Br về khối lượng). Khi X phản ứng với HBr thì thu được hai sản phẩm hữu cơ có cấu tạo khác nhau. Tên gọi của X là
A. but-1-en
B. etilen
C. but-2-en
D. propilen
Hướng dẫn
X là C4H8
Mà X + HBr thu được 2 sản phẩm
Đáp án A
Câu 9: Trộn 1 mol anken X với 1,6 mol H2 rồi dẫn hỗn hợp qua Ni nung nóng thu được hỗn hợp Y. Dẫn hỗn hợp Y vào brom dư thấy có 0,2 mol Br2 đã phản ứng. Hiệu suất phản ứng hiđro hóa là
A. 20%.
B. 50%.
C. 80%.
D. 70%.
Hướng dẫn
Y phản ứng với dung dịch Br2 anken dư
nanken dư = = 0,2 mol
nanken phản ứng = 1 – 0,2 = 0,8 mol
- hiệu suất phản ứng tính theo anken
Đáp án C
Câu 10: Dẫn 3,36 lít hỗn hợp X gồm 2 anken là đồng đẳng kế tiếp vào bình nước brom dư, thấy khối lượng bình tăng thêm 7,7 gam. Tìm CTPT của 2 anken ?
Hướng dẫn
Số mol hỗn hợp X là: nX = 3,36/22,4 = 0,15 mol
Phương trình phản ứng:
Khối lượng bình brom tăng là khối lượng của 2 anken:mX = 7,7 gam => M ̅X = mX/nX = 7,7/0,15 = 154/3 => n ̅ = 3,67.
Vậy CTPT của 2 anken kế tiếp là: C3H6 và C4H8
Xem thêm các phương trình hóa học khác:
C2H4 + H2O → C2H5OH | C2H4 ra C2H5OH
C6H5NH2 + Br2 → C6H2Br3NH2 + HBr | C6H5NH2 ra C6H2Br3NH2
C6H5OH + Br2 → C5H2Br3OH + HBr | C6H5OH ra C5H2Br3OH
C6H5-CH=CH2 + Br2 → C6H5-CHBr-CH2Br | C6H5-CH=CH2 ra C6H5-CHBr-CH2Br