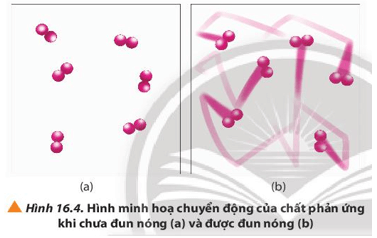
Quan sát Hình 16.4 và phương trình hóa học của phản ứng, giải thích vì sao tốc độ mất màu của KMnO4 trong 2 cốc không giống nhau
321
17/04/2023
Câu hỏi 4 trang 100 Hóa học 10: Quan sát Hình 16.4 và phương trình hóa học của phản ứng, giải thích vì sao tốc độ mất màu của KMnO4 trong 2 cốc không giống nhau.
Trả lời
Phương trình hóa học của phản ứng:
2KMnO4(aq) + 5H2C2O4(aq) + 3H2SO4(aq) → 2MnSO4(aq) + K2SO4(aq) + 10CO2(g) + 8H2O(l)
Ở nhiệt độ thường, các chất phản ứng chuyển động với tốc độ nhỏ.
Khi tăng nhiệt độ, các chất sẽ phản ứng với tốc độ lớn hơn, dẫn đến số va chạm hiệu quả tăng nên tốc độ phản ứng tăng.
Xem thêm các bài giải SGK Hoá học lớp 10 Chân trời sáng tạo hay, chi tiết khác:
Bài 13: Enthalpy tạo thành và biến thiên enthalpy của phản ứng hóa học
Bài 14: Tính biến thiên enthalpy của phản ứng hóa học
Bài 15: Phương trình tốc độ phản ứng và hằng số tốc độ phản ứng
Bài 16: Các yếu tố ảnh hưởng đến tốc độ phản ứng hóa học
Bài 17: Tính chất vật lí và hóa học các đơn chất nhóm VIIA
Bài 18: Hydrogen halide và một số phản ứng của ion halide

